乳腺癌是女性群体中较为常见的恶性肿瘤之一,近年来,年轻乳腺癌患者的比例持续上升。年轻乳腺癌患者通常表现出更具侵袭性的生物学特点,这对治疗提出了更高的要求。对于年轻乳腺癌患者的综合治疗策略,不仅要确保患者能够获得良好的疗效,还要帮助患者维持较好的生活质量,使其能够在治疗与日常生活之间实现更好的平衡。本期特别分享一例年轻的人表皮生长因子受体2(HER2)阳性多发转移乳腺癌患者的诊疗经历。该患者确诊时已处于Ⅳ期,一线治疗采用曲帕双靶方案,治疗过程中最佳疗效达到了部分缓解(PR)。然而,在治疗6个周期后,复查发现肝转移瘤出现增大,由于考虑到窦道转移的风险,未进行肝穿刺。该患者的一线无进展生存期(PFS1)为4.3个月。随后,二线治疗换用多西他赛+曲妥珠单抗+吡咯替尼方案,治疗2个周期后,疗效评估为部分缓解(PR)。综合考虑指南推荐、患者既往用药情况、临床疗效以及药物的可及性和便利性等因素,临床团队为患者制定了长春瑞滨软胶囊+曲妥珠单抗+吡咯替尼方案进行维持治疗。在维持治疗期间,患者于2021年1月21日接受了左乳全切+左腋窝淋巴结清扫术,术后病理结果显示达到了完全缓解(pCR)。术后,患者继续采用原方案维持治疗,并进行了局部放疗(2021-04-26至2021-5-18)。此后,由于患者病情保持稳定,于2024年01月10日进行了乳房Ⅱ期再造术,术后继续采用原方案维持治疗。目前,患者的肝部病灶已达到完全缓解(CR),胸骨转移也得到了稳定控制,一般状况良好。
病例分享
中国医学科学院肿瘤医院深圳医院肿瘤内科乳腺组
深圳市女医师协会乳腺保健专委会常务委员
深圳市抗癌协会靶向治疗与个体化治疗专业委员会委员
深圳市乳腺癌防治中心乳腺肿瘤内科专家组组员
深汕乳腺肿瘤防治联盟委员
专长:擅长乳腺癌等常见恶性肿瘤的诊断及内科综合治疗,参与多项课题和临床研究,以第一作者身份发表SCI论文5篇
病例介绍
患者:女,年龄37岁。
主诉:发现左乳肿物2月余,确诊左乳癌1周。
家族史、既往史、个人史:青霉素过敏。
月经史、婚育史:孕4产2,母乳喂养3个月。
现病史:2020年2月,患者扪及左乳肿物,因疫情未予特殊诊治,后肿物逐渐增大。2020年4月,于外院行钼靶示:左乳肿物54×66mm,BI-RADS 4B类;彩超示:左乳见一7.4×3.6cm低回声,BI-RADS 4类,左腋窝多个低回声结节考虑淋巴结肿大;乳腺MRI示:左乳腺癌BI-RADS 4级,大小7.1×6.4×4.1cm,伴左腋下淋巴结、左乳外侧皮肤受侵;左乳肿物空心针穿刺活检示:乳腺浸润性癌,非特殊型,Ⅲ级,ER-、PR-,HER-2(3+),Ki-67 75%+,E-cadherin+,P120 细胞膜;左腋窝淋巴结穿刺细胞学涂片示:见多灶恶性肿瘤细胞。后前往我院,于我科就诊。
辅助检查:
胸腹盆增强CT示:左乳癌伴左锁骨上、左腋窝、左胸小肌后、左内乳链区多发淋巴结转移;胸骨体左缘骨转移(直径0.6cm);双肺多发小结节性质待定;肝S3、S4段多发转移瘤(大者2.9×2.7cm);双侧髂外组淋巴结增大,大者9×5mm。
全身骨ECT示:胸骨上段左侧局灶性骨盐代谢活跃,不除外转移。
临床诊断:左乳浸润性癌cT4N3M1 Ⅳ期 HER2阳性型
多发淋巴结转移
多发肝转移
骨转移
双肺结节
治疗过程
一线治疗:
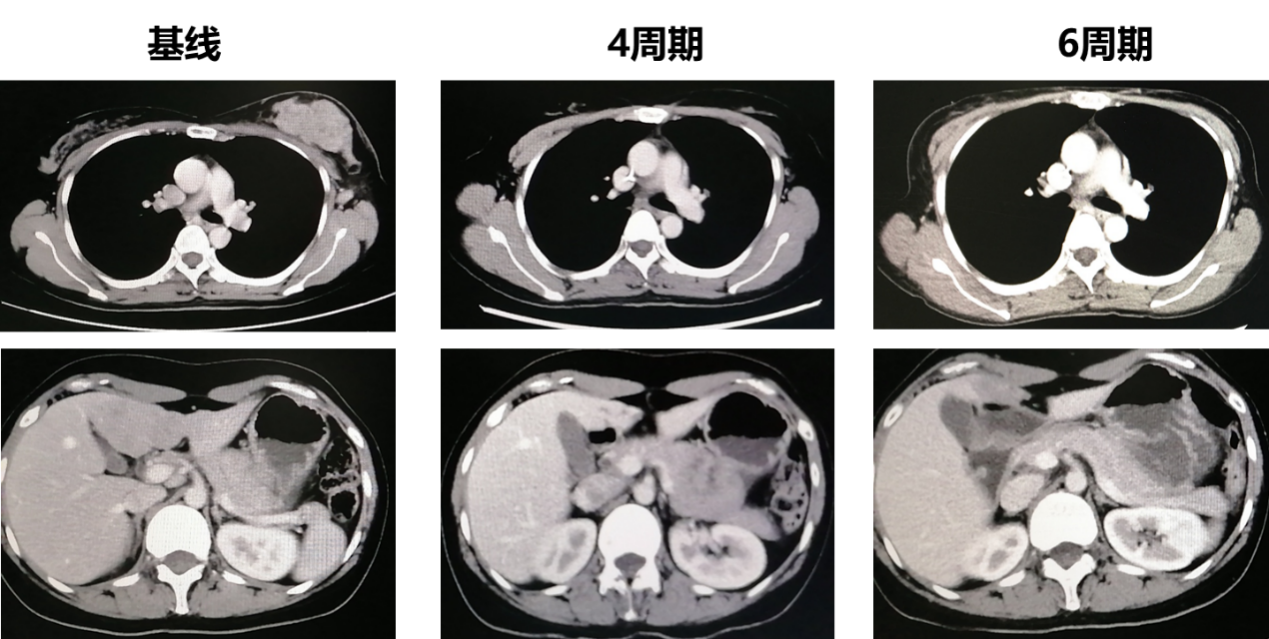
2020年4月15日至2020年8月24日,行曲妥珠单抗+帕妥珠单抗+多西他赛110mg/q3w×6周期治疗。
最佳疗效:PR。
6周期治疗结束后复查,提示肝转移瘤增大,余病灶维持PR。
PFS1:4.3个月。
二线治疗:
2020年8月25日至2020年10月9日,行多西他赛110mg+曲妥珠单抗+吡咯替尼/q3w×2周期治疗。
疗效:PR。
二线维持治疗:
2020年10月30日开始,行长春瑞滨软胶囊110mg d1、8 po+曲妥珠单抗+吡咯替尼/q3w×4维持治疗。
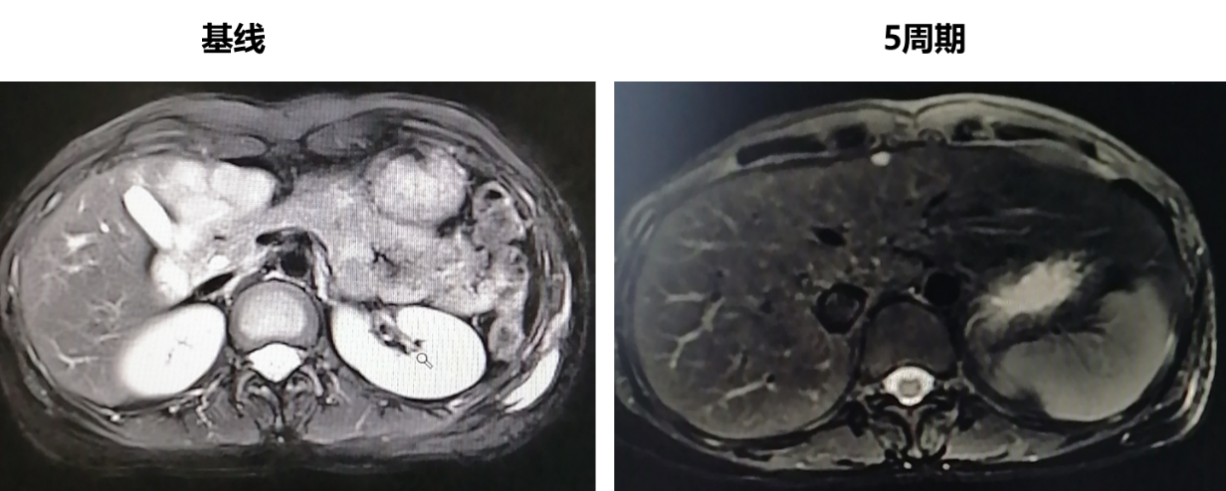
2021年1月14日,复查胸腹CT示:左乳原发灶、肝脏转移瘤未见显示,骨转移灶稳定伴成骨,双肺结节同前相仿,多发淋巴结稳定。彩超示:左乳未见肿物。
疗效:PR。
手术治疗及术后维持治疗:
2021年1月21日,行左乳全切+左腋窝淋巴结清扫术。术后病理诊断:“左乳癌化疗联合靶向后,维持治疗后”(1)(左乳癌改良根治标本)经充分取材,乳腺组织内局部见大量泡沫状组织细胞聚集及炎细胞浸润、间质纤维化伴含铁血黄素沉积,未见明确肿瘤组织残存,符合重度治疗反应(Miller and Payne 5级)。乳头、皮肤及胸肌筋膜未见癌。余周围乳腺组织未见明显病变。腋窝淋巴结未见转移癌(0/40),其中4枚淋巴结内见泡沫样组织细胞聚集伴纤维化,另于周围脂肪组织内见泡沫样组织细胞聚集,均考虑治疗后改变。
2021年2月10日复查肝脏MRI示:“左乳腺癌自2020-04-15化疗联合靶向治疗后,维持治疗中”复查,与2021-01-19上腹部MRI对比:1.原2020-04-15肝左叶S3、4段多发转移瘤现显示不具体,建议追随;2.原DWI序列示S4段见小片状稍高信号影,较前显示不具体,建议追随。原肝S7段可见小斑片肝胆期信号稍减低灶,现扫描序列未见显示,建议追随;3.肝脏S4段前缘被膜下小囊肿,无强化,直径约0.6cm,同前相仿。
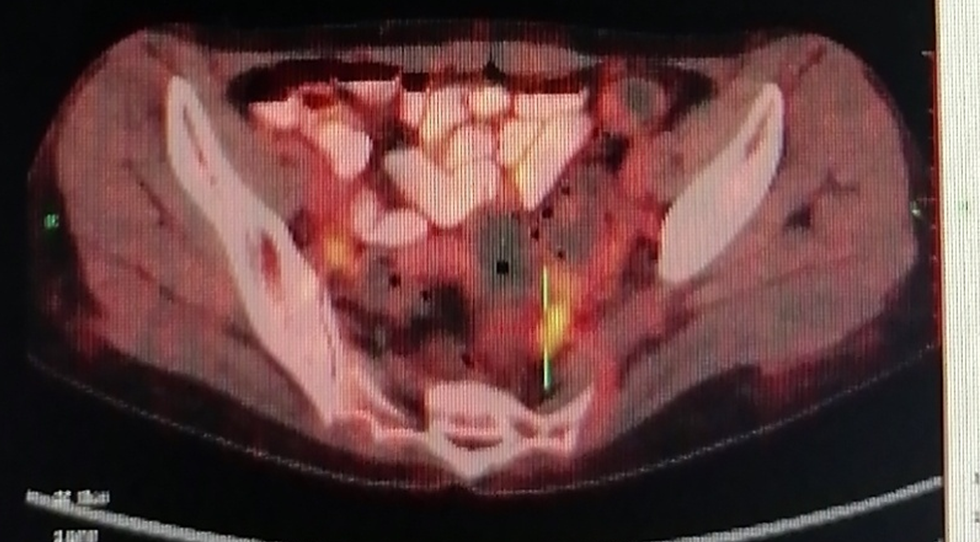
2021年3月复查胸上腹部PET-CT示:1.左侧乳腺缺如,左侧胸壁、腋窝条片影,伴代谢增高,考虑以术后改变为主,请随诊。左侧肩胛下肌深面条状代谢增高,考虑良性摄取。2.胸骨体左缘骨转移瘤,目前未见代谢增高,请随诊。3.双肺多发小结节,同前相仿,未见代谢增高,请薄层 CT 随诊。双侧胸膜局限性增厚,未见代谢增高。4.肝S4段低密度影,同前相仿,未见代谢增高,考虑囊肿。5.左侧盆腔髂内区类结节,伴代谢增高,左侧附件摄取?必要时结合超声检查。子宫内见节育器置入,周围内膜代谢增高,倾向良性,请结合超声。右侧附件区饱满,双侧附件区代谢增高,倾向良性,请同上一并结合超声。6.双侧咽鼓管隆突、咽隐窝代谢增高,考虑良性,请随诊。双侧下颌下腺、舌下腺代谢增高:双侧颈部(Ⅱ区)淋巴结代谢增高,上述考虑良性摄取,请随诊。甲状腺轻度代谢增高,考虑良性。双侧筛窦粘膜增厚,伴代谢增高,考虑炎性。7.脊椎弥漫性代谢增高,请随诊。8.双侧颞肌代谢增高,考虑良性摄取。
妇科彩超:未见异常。
盆腔MRI:因有节育环无法进行。
术后继续予长春瑞滨软胶囊110mg d1、8 po+曲妥珠单抗+吡咯替尼/q3w×4维持治疗。并于2021-04-26至2021-5-18于我院放疗科行放疗(胸壁+锁上及胸骨转移灶)。
乳房再造术及术后维持治疗:
2024年01月10日,患者于我院乳腺外科行左侧胸壁疤痕结节切除+疤痕松解+乳房下皱襞重建+脐整形+腹壁整形+显微镜下血管吻合+游离腹壁下动脉穿支皮瓣(DIEP)乳房Ⅱ期再造术。术前至2024年2月停用所有抗肿瘤药物。
2024年2月8日至2025年4月16日,患者继续使用长春瑞滨软胶囊+吡咯替尼+曲妥珠单抗方案维持治疗。
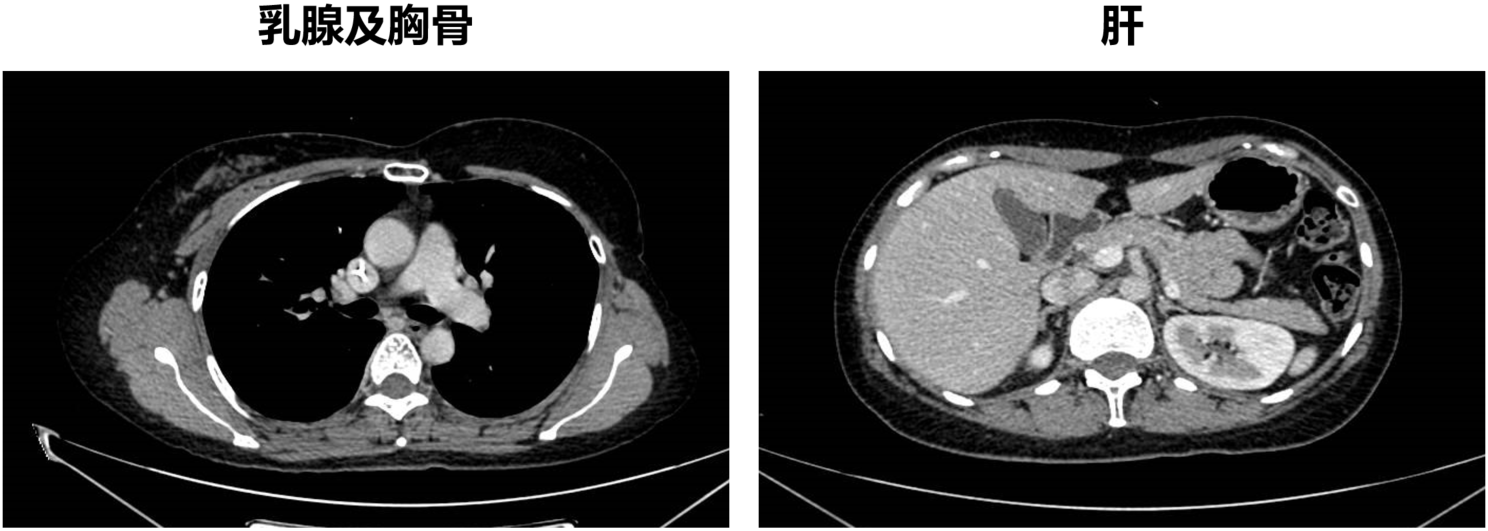
2025年3月18日,复查全身增强CT提示:肿瘤控制稳定(乳腺原发灶已切除,肝部病灶CR,胸骨转移控制稳定,2021年3月PET/CT已提示胸骨病灶无代谢活性)。
2025年5月8日至今,患者使用长春瑞滨软胶囊+吡咯替尼方案进行维持治疗。
治疗流程图
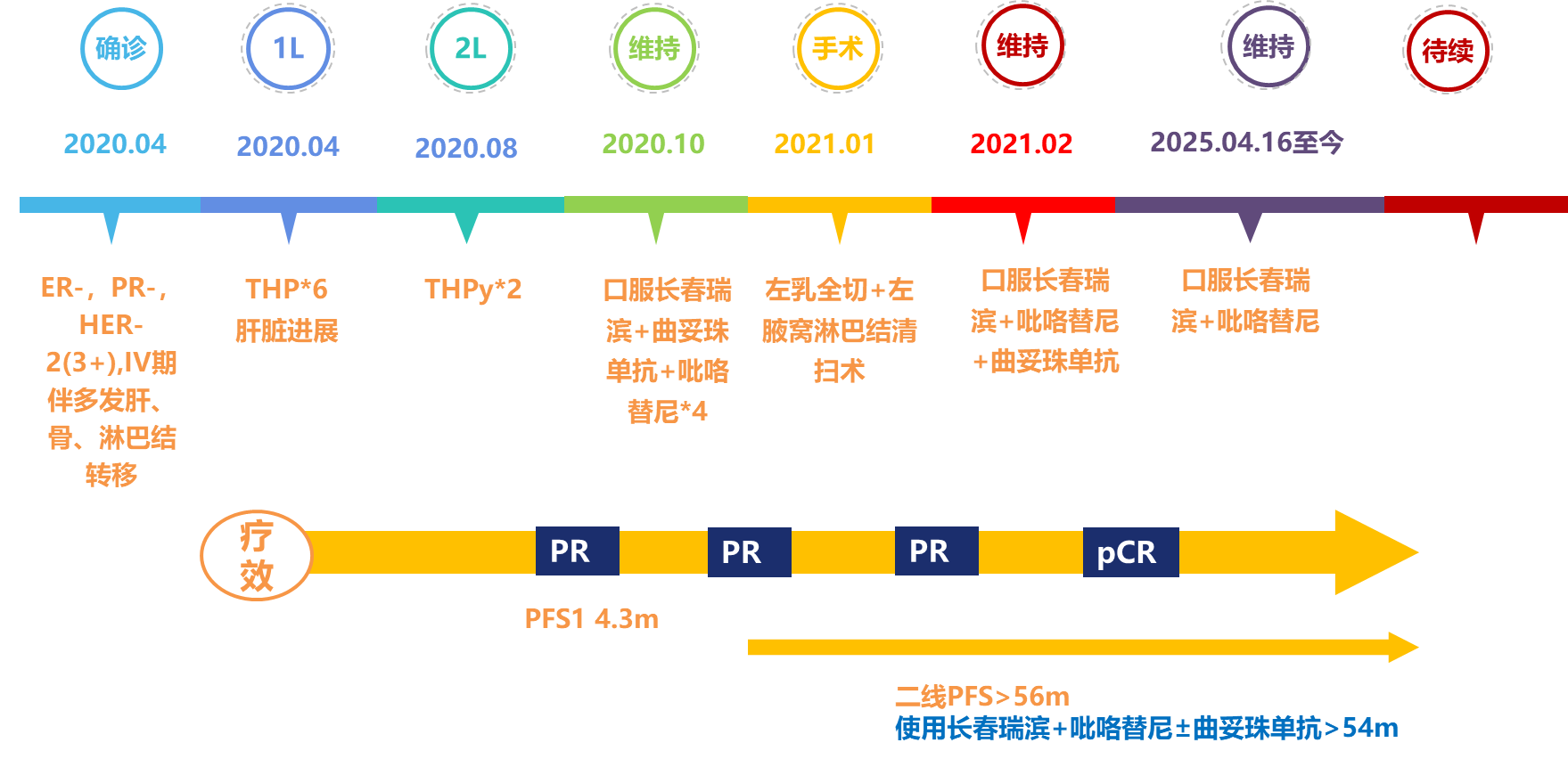
专家点评
中国医学科学院肿瘤医院深圳医院乳腺内科学科带头人、乳腺病区主任
主持国家自然科学基金项目、省级课题多项
“乳腺癌内脏转移的研究”获“中国抗癌协会科技奖二等奖”“广东省科技进步奖三等奖”“汕头市科技进步奖一等奖”
入选肿瘤内科和乳腺科“岭南名医”录、深龙英才B类、深圳实用型临床医学人才
已发表SCI论文10余篇
深圳市抗癌协会靶向治疗与个体化治疗专业委员会主任委员
深汕乳腺肿瘤防治联盟主任委员
中国抗癌协会肿瘤靶向治疗专业委员会委员
广东省抗癌协会乳腺癌专业委员会委员
广东省保健协会乳腺保健分会副主任委员
广东省医师协会肿瘤科医师分会第三届委员
广东省女医师协会乳腺癌专业委员会副主任委员
北京中西医慢病防治促进会中医乳腺癌防治全国专委会副主委
CSCO乳腺癌专委会委员
直面困境,探索年轻HER2阳性乳腺癌治疗之法
年轻乳腺癌患者诊断时往往临床分期较晚,且三阴性乳腺癌、HER2阳性型乳腺癌的占比相对更高,更具侵袭性[1]。在生存率方面,年轻乳腺癌患者的表现也相对较差。研究数据显示,在中国,年龄小于40岁的乳腺癌患者,其5年无病生存率和10年总生存率分别为85.5%和85.0%,而40至49岁的患者则分别为88.1%和88.7%[2]。而年轻乳腺癌患者由于发病时年龄相对较轻,其对治疗、预后及生活质量等方面均有着独特的需求。患者往往承担着更为复杂多样的社会和家庭角色,治愈后亦有更多的机会和需求参与职场活动,因此对生活质量的要求也更高。此外,年轻乳腺癌患者在抗肿瘤治疗过程中,还存在着生育力保护、保留乳房外形等个性化需求[2]。
本例患者确诊时年仅37岁,正处于母乳喂养期,但其病理类型为HER2阳性,且合并多发淋巴结转移、肝转移、骨转移。CLEOPATRA研究比较了抗HER2抗体曲妥珠单抗+帕妥珠单抗与曲妥珠单抗单药分别联合紫杉类化疗药物的疗效与安全性。结果显示[3],曲帕双靶一线治疗HER2阳性晚期乳腺癌显著延长了中位无进展生存期(mPFS:18.7个月 vs 12.4个月)和中位总生存期(mOS:57.1个月 vs 40.8个月)。PUFFIN研究[4,5]作为CLEOPATRA研究在中国的桥接试验,再次验证了曲帕双靶治疗的显著生存优势。基于此,国内外指南一致推荐曲妥珠单抗联合帕妥珠单抗及紫杉类药物的双靶方案作为HER2阳性晚期乳腺癌的标准一线治疗方案[6,7]。本例患者一线治疗采用的便是曲妥珠单抗联合帕妥珠单抗及多西他赛方案。然而,在完成6个周期的治疗后,患者出现了肝转移瘤增大的情况。面对这一新的挑战,二线治疗方案的选择显得尤为关键。
优中择优,制定个性化维持治疗方案
在HER2阳性转移性乳腺癌中,吡咯替尼单药或联合卡培他滨治疗已展现出良好的抗肿瘤活性和可控的安全性。PHOEBE研究探索了吡咯替尼联合卡培他滨 vs 拉帕替尼联合卡培他滨用于HER2阳性晚期乳腺癌患者二线治疗的疗效。研究结果显示[8],在曲妥珠单抗耐药人群,吡咯替尼组的中位PFS为12.5个月,拉帕替尼组为6.8个月,HR值为0.39(95%CI 0.27-0.56),显示出小分子TKI在我国HER2阳性二线治疗中较好的PFS和OS获益趋势。PHILA研究创新性选择大分子曲妥珠单抗联合小分子TKI再联合化疗与曲妥珠单抗联合化疗比较。期中分析显示[9],吡咯替尼联合曲妥珠单抗和多西他赛(PyroHT组),与安慰剂联合曲妥珠单抗和多西他赛(HT组)相比,显著改善了未经治的HER2阳性转移性乳腺癌患者的PFS(24.3个月 vs 10.4个月)。可见,大分子单抗与小分子TKI的结合位点与作用机制存在差异,联合治疗在一定程度上可克服耐药,为晚期乳腺癌临床治疗提供了更新、更优的解题思路。基于此,本例患者二线治疗采用PyroHT方案,疗效取得PR。
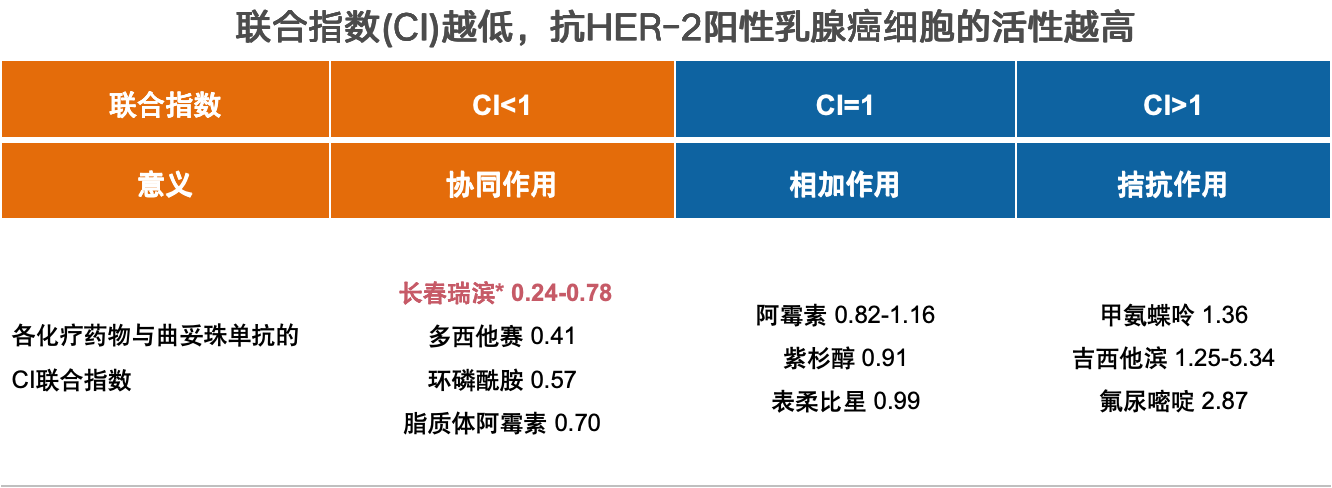
在长期维持治疗过程中,化疗作为乳腺癌综合治疗的重要组成部分,其选择需要综合考虑药物耐受性、便利性等多方面因素,以实现最佳的治疗效果和生活质量。既往研究显示[10-14],长春瑞滨与曲妥珠单抗联合具有良好的协同作用。相比其他化疗药物,长春瑞滨和曲妥珠单抗的联合指数(CI值)显著更低(图1)[10-14]。此外,其口服剂型与静脉注射剂型具有生物等效性[15-17],且耐受性更好,用药更便利性。NorBreast-231研究显示[18],口服长春瑞滨软胶囊 vs 紫杉醇治疗意向治疗人群(ITT)的疾病控制率(DCR)分别是75.8% vs 75.4%,OS分别为27.6和22.3个月。且与静脉注射紫杉醇相比,口服长春瑞滨软胶囊组脱发、周围神经病变等不良反应的发生频率和严重程度更低[18]。口服剂型因其用药便利性,也更易被患者接受,降低患者的患病主观感受,提高患者的生活治疗[19],为临床提供了更佳选择。
综合考虑患者的病情及需求,临床团队为患者制定了长春瑞滨软胶囊联合曲妥珠单抗与吡咯替尼的方案进行维持治疗。在维持治疗期间,患者顺利接受了左乳全切术及左腋窝淋巴结清扫术,术后疗效保持PR。3年后,患者进行了乳房再造术,术程顺利。至今,患者的二线PFS已超过56个月,维持治疗方案的使用时间也已超过54个月,且患者已达到临床完全缓解(CR)的状态。
[1] Yanis Hassaine,et al. Breast Cancer Res. 2022 Dec 5;24(1):87.doi: 10.1186/s13058-022-01581-5.
[2]中国临床肿瘤学会乳腺癌专家委员会, 中国抗癌协会乳腺癌专业委员会, 中华医学会外科学分会乳腺外科学组. 中国年轻乳腺癌诊疗专家共识(2022) [J] . 中华医学杂志, 2023, 103(6) : 387-403. DOI: 10.3760/cma.j.cn112137-20220907-01895.
[3] Swain SM, Miles D, Kim SB, et al. Lancet Oncol, 2020, 21(4): 519-530.DOI: 10.1016/S1470-2045(19)30863-0
[4] XU B H, LI W, ZHANG Q Y, et al. Breast Cancer Res Treat, 2023, 197(3): 503-513.
[5] XU B H, LI W, ZHANG Q Y, et al. Breast Cancer Res Treat, 2020, 182(3): 689-697.
[6]CSCO乳腺癌指南 2025.
[7] NCCN指南2025.
[8] Xu Binghe,Yan Min,Ma Fei et al. Lancet Oncol, 2021.
[9] MA F, YAN M, LI W, et al. BMJ, 2023, 383: e076065.
[10]Foucquier J, Guedj M.Pharmacd. Res Perspect. 2015 Jun;3[3]:e00149.
[11]Fujimoto-Ouchi Kaori. Cancer Chemother Pharmacol 2002;49:211-216.
[12]Pegram M, et al. Oncogene 1999;18:2241-2251.
[13]Pietras RJ, et al. Oncogene 1998;17:2235-2249.
[14]Farhat F, et al. Cancer Chemother Pharmacol 2016; 77(5):1069-77.
[15]Bonneterre J, et al. Ann Oncol.2001;12(12):1683-91.
[16]Marty M, et al. Ann Oncol.2001;12(11):1643-9.
[17]Variol P, et al. Eur J Clin Pharmacol.2002;58(7):467-76
[18]Aapro M, et al. Randomized phase II study evaluating weekly oral vinorelbine versus weekly paclitaxel in estrogen receptor-positive, HER2-negative patients with advanced breast cancer (NorBreast-231 trial)[J]. Breast. 2019;45:7-14.
[19] Catania C, et al. Breast Cancer Res Treat. 2005,92(3):265-272.
排版编辑:TanRongbing











 苏公网安备32059002004080号
苏公网安备32059002004080号


