基于ALTA-1L、ALEX等研究结果,ALK-TKI已成为ALK阳性晚期非小细胞肺癌(NSCLC)一线治疗的标准用药,患者可获得长期的一线无进展生存期(PFS)获益。然而,如何优化患者全程管理模式,以保障患者在更长时间维度下的整体获益,成为当下值得思考的新问题。特别是对于因ALK通路继发突变而耐药的患者,如何通过对ALK-TKI的合理排兵布阵,使患者持续从靶向治疗中获益,将成为影响其总生存获益的关键。本期【肿瘤资讯】将基于循证医学证据探讨ALK阳性NSCLC全程管理模式,并特邀中山大学附属第五医院肿瘤中心王志辉教授分享、点评一例ALK阳性晚期NSCLC,从循证医学与临床实践双重视角,探讨如何通过精准治疗,为一线ALK-TKI耐药的ALK阳性NSCLC患者延续生存希望。
ALK-TKI一线治疗后可继发多种ALK通路突变,临床研究及真实世界数据提示布格替尼序贯治疗可行性
随着ALK慢病时代的到来,全程管理对ALK阳性晚期NSCLC患者而言至关重要,需要关注一线及后线治疗的方案选择和患者管理。布格替尼的ALTA-1L研究长期随访真实世界研究中,布格替尼耐药序贯洛拉替尼,真实世界全程中位PFS2可达到74.7个月[1],提示了ALK阳性NSCLC患者在一线ALK-TKI耐药后二线继续尝试序贯其它ALK-TKI的可行性与重要性。如何针对性应对ALK-TKI耐药后的新发On-target突变,选择精准的后线治疗策略,同样是保障患者全程治疗获益的关键。在2期、单臂开放标签、多中心J-ALTA研究中[2,3],对于阿来替尼±克唑替尼一线治疗进展后接受布格替尼治疗的ALK阳性晚期NSCLC患者,经独立评审委员会(BIRC)评估确认的客观缓解率(ORR)为34%,中位持续缓解时间(DoR)为14.8个月,中位PFS达到7.3个月。另一项分析ALTA-2和J-ALTA研究中阿来替尼治疗进展后使用布格替尼的综合疗效和安全性的临床研究[4],共纳入133例患者(ALTA-2研究,阿来替尼治疗后患者,n = 86;J-ALTA研究,主要队列,n = 47),确认的ORR为30.8%,中位 DOR 为9.2个月,BIRC评估的中位 PFS 为5.2个月。一项评估接受ALK-TKI治疗后序贯使用布格替尼治疗的全球多中心真实世界研究中[5],布格替尼对于既往接受过1种ALK-TKI治疗的患者,中位至治疗中止时间(TTD)达到11.8个月。提示布格替尼用于ALK-TKI经治患者同样具有临床潜力。
布格替尼应用于二线治疗的临床潜力来源于其对ALK通路继发突变位点的抑制能力。在体外研究中[6,7],针对ALK通路的常见继发突变如G1269A、I1171T、L1196M、C1156Y、G1202R等,布格替尼显示了对比其他ALK-TKI更好的抑制敏感性(IC50更低);针对ALK-TKI耐药的17种ALK通路突变,布格替尼均显示了抑制活性[8]。
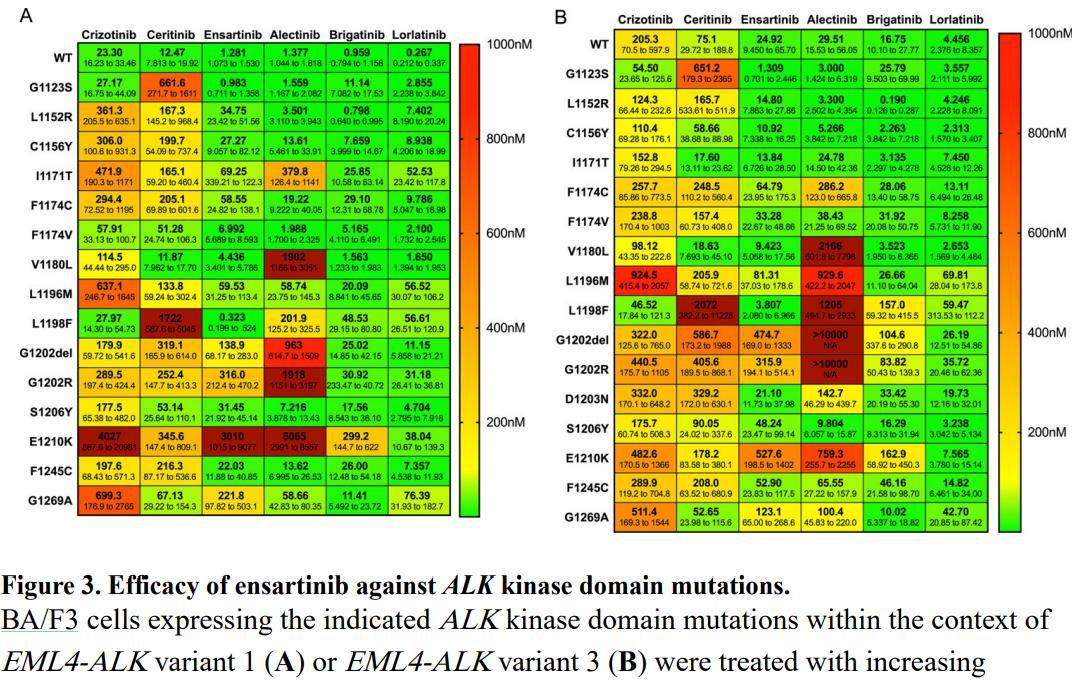
针对具体的继发突变位点,布格替尼已有一些临床病例报道:
L1196Q[9]:一例60岁美国患者确诊为IV期肺腺癌,EML4-ALK融合阳性,经一线克唑替尼(PFS=7个月)和二线阿来替尼(PFS=15个月)治疗后,经检测新发L1196Q突变,三线接受布格替尼治疗后,疾病进展得到有效控制,PFS超17个月。
L1196M[3]:J-ALTA研究中,一例阿来替尼经治的L1196M突变患者接受布格替尼治疗的PFS达到18.5个月,疗效评估PR。
G1202R[10]:ALTA-2研究中,一例阿来替尼经治的G1202R突变患者接受布格替尼治疗的PFS达到12个月;一例塞瑞替尼经治的G1202R突变患者接受布格替尼治疗的PFS达到7.5个月。
V1180L[10]:ALTA-2研究中,一例阿来替尼经治的V1180L突变患者接受布格替尼治疗的PFS达到11个月。
G1269A[11]:一例71岁男性患者诊断为IV期肺腺癌,EML4-ALK阳性,一线克唑替尼治疗(PFS=11个月),后经检测新发G1296A突变,二线使用布格替尼治疗两个月后,ctDNA样本中G1296A水平显著下降至无法检测(PFS=9个月)。
I1171S[12]:一例57岁白人女性患者诊断为肺腺癌伴脑转移,EML4-ALK阳性,一线接受全脑放疗与培美曲塞和卡铂治疗,培美曲塞维持治疗(PFS=14个月),二线克唑替尼治疗(PFS=19个月),三线阿来替尼治疗(PFS=24个月),后检测新发I1171S突变,四线使用布格替尼治疗后,转移病灶缩小,肿瘤进展得到控制,PFS已经超9个月,仍在持续缓解。
I1171N[10,13]:一项评估阿来替尼经治患者接受布格替尼治疗的治疗结局的多中心、回顾性研究中,2例I1171N突变患者均达到疾病稳定(SD);ALTA-2研究中,一例阿来替尼经治的I1171N突变患者接受布格替尼治疗的PFS达到5.2个月,疗效评估部分缓解(PR)。
I1171N临床案例分享:一线ALK-TKI耐药后新发I1171N突变,患者接受布格替尼治疗,获得了较好的缓解。
基本信息:患者男,46岁。既往史无特殊,否认高血压、糖尿病、冠心病等病史。无吸烟史。
主诉:反复咳嗽、咳血丝痰4月。
现病史:患者于2020-12因“反复咳嗽、咳痰4月”就诊于当地医院,行CT检查示:左下肺癌伴双肺、胸膜多转移;左侧胸腔积液;右颈部根部、双肺门多发淋巴转移。后外院行颈部淋巴结穿刺活检及基因检测等,现就诊于我院。
病理诊断:(左侧颈部淋巴结)结合形态及免疫组化符合肺黏液腺癌。
基因检测:EML4-ALK 融合阳性
诊断结果:左肺腺癌伴肺内、胸膜、锁骨上淋巴结转移(cT3N3M1c,IVB期),EML4 exon13-ALK exon19(V1亚型)
一线治疗:
2021-01起,行“阿来替尼,600mg bid”治疗,期间出现1度胆红素升高及便秘。2024-12 疗效评估为疾病进展(PD)。一线治疗PFS=47个月。
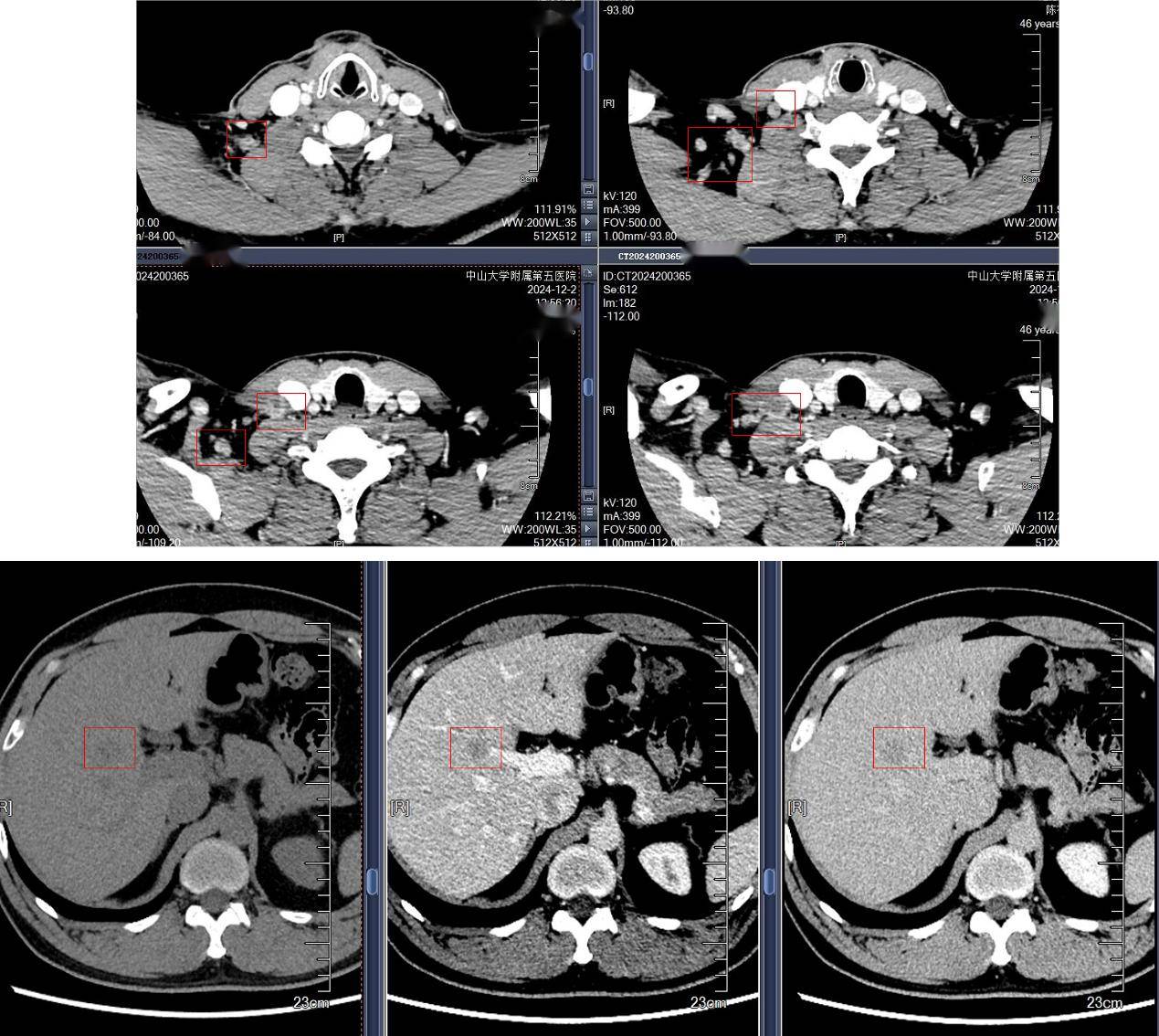
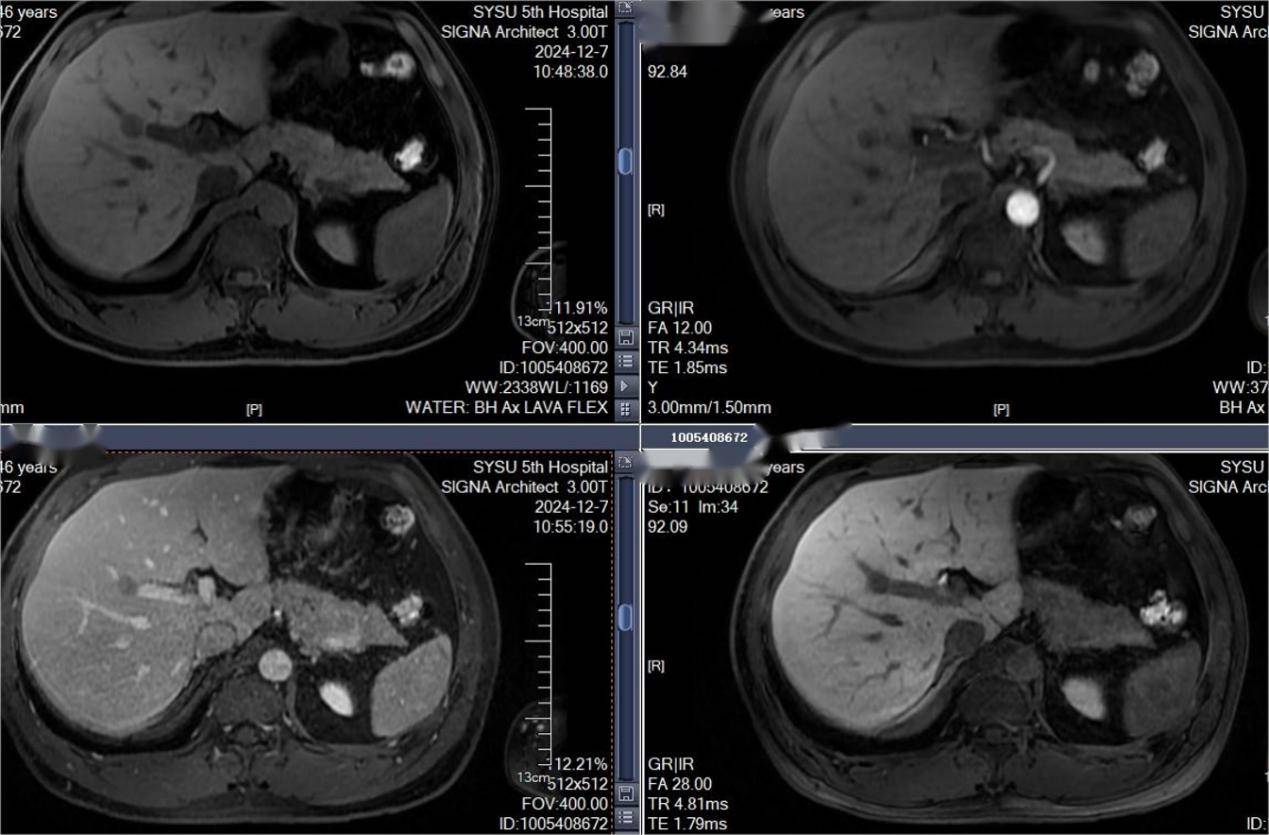
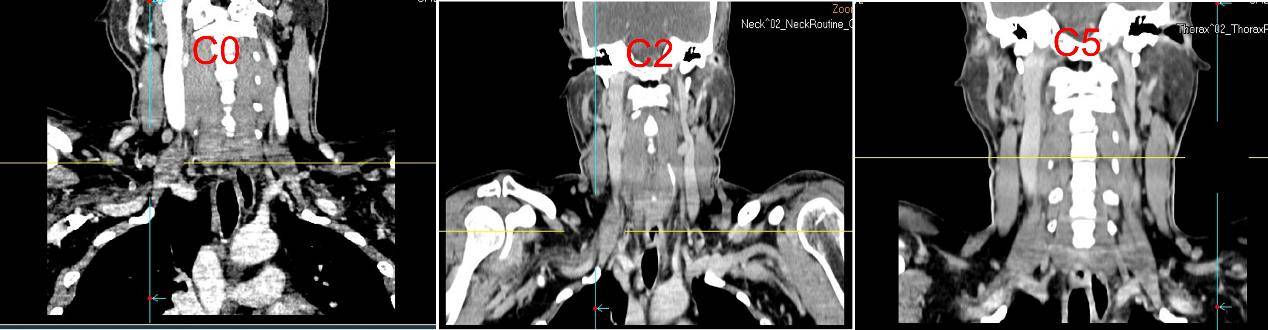
2024-12-09行超声引导下颈部淋巴结穿刺活检,病理诊断:(右颈部淋巴结)增生的纤维组织内见腺癌浸润灶,结合HE形态、免疫组化结果及临床病史,符合转移性腺癌,首先考虑肺来源。
基因检测:ALK I1171N、EML4 exon13-ALK exon19融合;TP53-G245S
二线治疗:
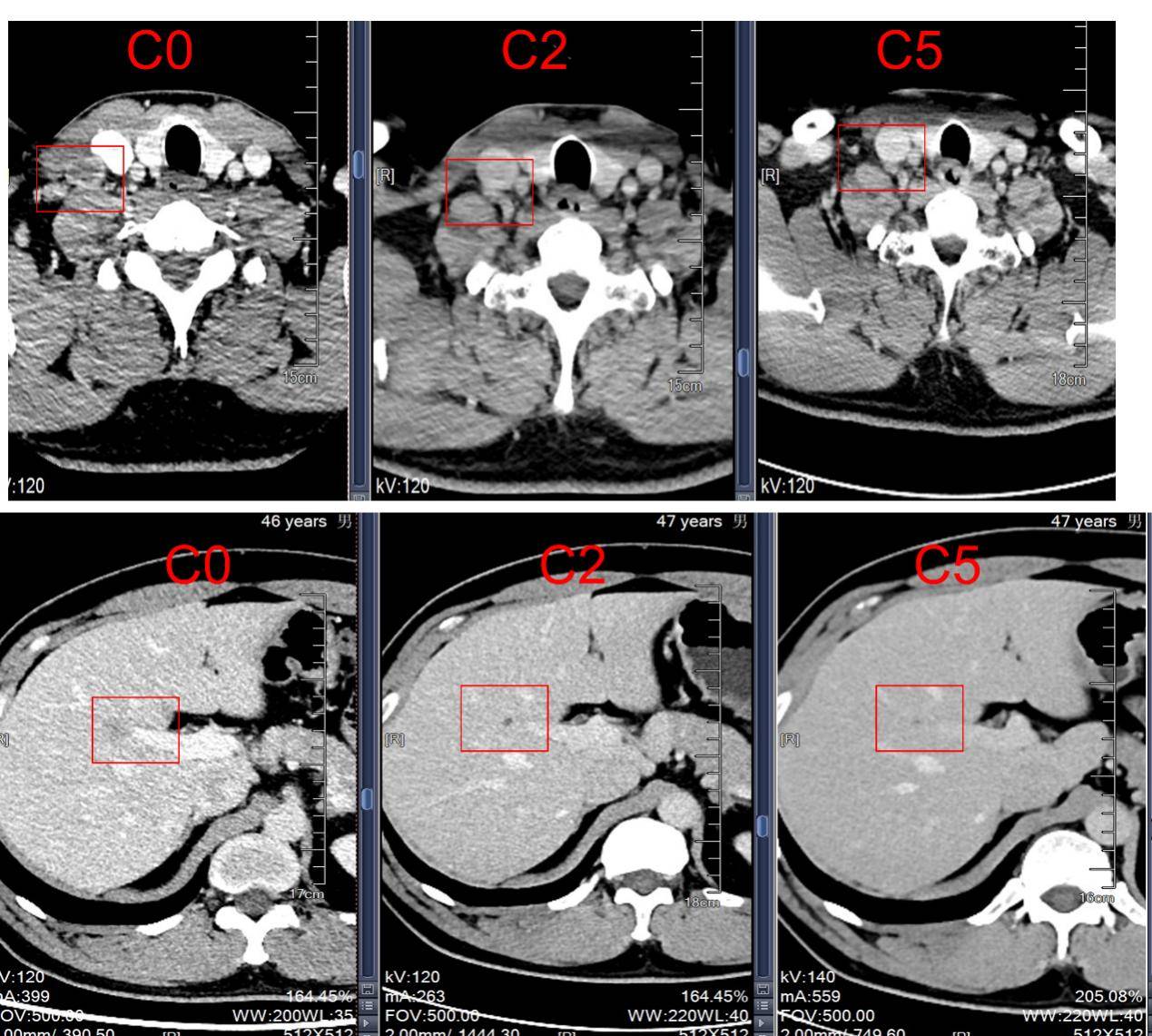
2024-12起,行“布格替尼 180mg qd”治疗,期间未观察到胆红素升高及便秘等不良反应。
专家点评
中山大学附属第五医院胸部肿瘤科 副主任医师
肿瘤学博士 硕士研究生导师
珠海市医学高层次人才
广东省精准医学应用学会肿瘤综合治疗分会 常委
广东省器官医学与技术学会肿瘤精准医学分会 常委
广东省医疗行业协会肺部肿瘤分会 常委
广东省医师协会肿瘤内科分会 委员
广东省医师协会肿瘤重症专委会 委员
广东省呼吸与健康学会肿瘤专委会 委员
主持国自然及珠海市科技局等科研项目多项
王志辉教授:目前,针对ALK阳性晚期NSCLC患者,随着ALK-TKI的快速发展,患者的一线PFS已经大大延长。例如在布格替尼的ALTA-1L研究中,布格替尼一线治疗ALK阳性晚期NSCLC患者,中位PFS可达到24.0个月,远超以往非精准治疗时代的PFS表现。随着而来的新问题是,如何在患者治疗全程中,通过精准、个体化的全程管理,保障患者在一线PFS之外的治疗获益,其中关键便在于通过识别耐药机制,实行精准化全程管理。
对于一线ALK-TKI治疗的患者,常见的ALK通路耐药机制为包括本病例患者的I1171N突变在内的各类突变形式,例如G1202R、L1196M、、I1171S、E1210K等。对于此类患者,应选择仍能有效针对此类ALK继发突变的ALK-TKI。本病例后续治疗中选择的布格替尼便是可有效针对此类耐药突变的ALK-TKI,在2期、单臂开放标签、多中心J-ALTA研究中[3],对于47例阿来替尼±克唑替尼一线治疗进展后接受布格替尼治疗的患者经IRC和研究者评估的ORR分别达到34%和38%,IRC评估的中位持续缓解时间(DoR)和中位PFS分别为14.8个月和7.3个月,中位OS则达到了28.4个月。这一结果提示了布格替尼在全程管理中的重要临床应用价值。本病例患者在接受布格替尼治疗后,同样持续获益,目前仍在继续使用布格替尼。
该患者的治疗经过验证了全程精准管理模式的有效性,通过对耐药突变的检测,指导后线治疗方案的选择,是患者后续持续获益的第一关键因素;第二关键因素则是对可有效抑制ALK通路继发突变的布格替尼的选择。双重因素的共同作用,促成了患者在一线ALK-TKI治疗后仍然可从精准治疗中持续获益。
未来,全程精准管理模式将成为临床标准,为更多患者带来获益。
[1] AHN, M.-J., et al. P1. 12B. 03. Journal of Thoracic Oncology, 2024, 19.10: S200.
[2] Kumagai T, et al. ASCO 2022. Abstract 9075.
[3] Yoshida T, et al. Cancer Sci. 2023;114(9):3698-3707.
[4] Sai-Hong l. ou, et al. 2022 WCLC. MA13.03.
[5] Lin HM, et al. Future Oncol. 2020;16:1031–41.
[6] Horn L, et al. J Thorac Oncol. 2019;14(11):1901-1911.
[7] M.Johnson, et al. 2023 ELCC. 81TiP.
[8] Zhang, S, et al. Clin Cancer Res. 2016; 22:5527-5538.
[9] Latif H. Transl Lung Cancer Res. 2020 Oct;9(5):2145-2148.
[10] Ou SI, et al. J Thorac Oncol. 2022 Dec;17(12):1404-1414.
[11] Ding M, et al. Clin Lung Cancer. 2019 May;20(3):e229-e232.
[12] Sehgal K . J Thorac Oncol. 2019 Jan;14(1):e1-e3.
[13] Lin JJ. J Thorac Oncol. 2018 Oct;13(10):1530-1538.

审批编号:VV-MEDMAT-124200
审批日期:2025年7月
仅供医疗卫生专业人士使用
排版编辑:肿瘤资讯-LWT












 苏公网安备32059002004080号
苏公网安备32059002004080号


