
随着CLDN18.2靶点的发现与深入研究,胃癌精准治疗迈入新阶段。佐妥昔单抗作为全球首个上市的CLDN18.2靶向药物,在SPOTLIGHT和GLOW两项Ⅲ期研究中联合化疗展现出良好的疗效和安全性,为CLDN18.2阳性晚期胃癌患者带来新的治疗选择。临床数据显示,佐妥昔单抗的不良反应总体可控,部分患者在治疗初期可能出现以恶心、呕吐为主的胃肠道反应,通过规范管理可有效缓解。本文将系统梳理佐妥昔单抗的安全性特征,结合共识指南与临床经验,为临床优化管理策略、提升治疗依从性和患者获益提供参考。
本期特邀专家——徐瑞华 教授
国家百千万领军人才
中国医学科学院学术咨询委员会 学部委员
中山大学附属肿瘤医院 院长
华南恶性肿瘤防治全国重点实验室 主任
中国临床肿瘤学会 第四届理事长
中国抗癌协会 副理事长
中国抗癌协会肿瘤内科学专委会 主任委员
中国临床肿瘤学会肠癌专业委员会 第二届主任委员
中国抗癌协会肿瘤靶向治疗专委会 首任主任委员 Cancer Communications IF 24.9 主编
· 以第一完成人获得国家科技进步二等奖2项、全国创新争先奖1项、省部级一等奖7项、何梁何利基金科学与技术奖、吴阶平医药创新奖、谈家桢临床医学奖及CSCO年度成就奖
·入选国家百千万人才工程、全国先进工作者、国务院特殊津贴专家、南粤百杰人才培养工程、国家卫生计生突出贡献中青年专家等人才项目
·以最后通讯作者在 NEJM、JAMA(2篇)、Cell、Nat Med(5篇)、BMJ、Ann Oncol(2篇)、Lancet Oncol(2篇)、Lancet G&H(2篇)、Cancer Cell(3篇)、JAMA Oncol(2篇)等发表论文200余篇(62篇IF>30)
本期特邀专家——李 进 教授
中国药科大学附属上海高博肿瘤医院 院长
同济大学附属东方医院 主任、终身教授
亚洲肿瘤联盟(FACO)主席
希思科基金会 理事长
中国药促会肿瘤临床研究专委会 主任委员
国家卫健委能建与继教肿瘤专家委员会 副主任委员
中国临床肿瘤学会(CSCO) 前理事长
中国临床肿瘤学会结直肠癌专家委员会 主任委员
中国临床肿瘤学会胃癌专家委员会前任 主任委员
Cancer Science副主编
本期特邀专家——梁 军 教授
北京大学国际医院 执行院长、肿瘤医学中心主任
北京大学肿瘤医院 大内科副主任、主任医师、博士生导师、二级教授
原中国临床肿瘤学会(CSCO)副理事长、现指导委员会 副主任委员
CSCO胃癌专家委员会副主任委员
中国抗癌协会胃癌专委会 副主任委员
中国抗癌协会胃癌专委会 内科学组 副组长
中国抗癌协会首届整合胃癌委员会 副主任委员
CSCO抗肿瘤药物安全管理专家委员会 主任委员
CSCO肝癌专家委员会、胰腺癌专家委员会 副主任委员
国家卫生健康委能力建设和继续教育肿瘤学专家委员会副主任委员
中华医学会肿瘤学分会肿瘤内科专家委员会副主任委员
科技部重大专项评审专家
佐妥昔单抗的总体安全性特征
![]() SPOTLIGHT 和 GLOW 是确立佐妥昔单抗在晚期胃癌一线治疗标准地位的两项关键Ⅲ期研究。这两项研究中,佐妥昔单抗联合化疗表现出良好的耐受性和可管理的安全性,其治疗期间不良事件(TEAE)总体发生率与安慰剂联合化疗相似,恶心和呕吐是佐妥昔单抗组中最常见的TEAE[1,2]。SPOTLIGHT 和 GLOW 研究综合分析显示,约一半提前停药的患者是因TEAE所致,而恶心与呕吐则是其中最常见的原因[3]。值得关注的是,SPOTLIGHT研究最终公布的总生存期(OS)数据表明,在符合方案分析集(排除了大多数提前停药的患者)中,佐妥昔单抗组的OS获益更加显著[4]。这一发现强有力地提示:佐妥昔单抗的生存获益可能因不良反应导致的早期停药而被低估。
SPOTLIGHT 和 GLOW 是确立佐妥昔单抗在晚期胃癌一线治疗标准地位的两项关键Ⅲ期研究。这两项研究中,佐妥昔单抗联合化疗表现出良好的耐受性和可管理的安全性,其治疗期间不良事件(TEAE)总体发生率与安慰剂联合化疗相似,恶心和呕吐是佐妥昔单抗组中最常见的TEAE[1,2]。SPOTLIGHT 和 GLOW 研究综合分析显示,约一半提前停药的患者是因TEAE所致,而恶心与呕吐则是其中最常见的原因[3]。值得关注的是,SPOTLIGHT研究最终公布的总生存期(OS)数据表明,在符合方案分析集(排除了大多数提前停药的患者)中,佐妥昔单抗组的OS获益更加显著[4]。这一发现强有力地提示:佐妥昔单抗的生存获益可能因不良反应导致的早期停药而被低估。
![]() 因此,优化恶心和呕吐的管理策略,对于延长治疗持续时间、提高依从性、实现患者最大生存获益至关重要。
因此,优化恶心和呕吐的管理策略,对于延长治疗持续时间、提高依从性、实现患者最大生存获益至关重要。
佐妥昔单抗引起恶心呕吐的特点
佐妥昔单抗所致的恶心和呕吐具有如下特征。
![]() 发生率及时间:SPOTLIGHT 和 GLOW研究的综合分析[3]显示,恶心和呕吐的发生率在佐妥昔单抗首次输注期间达到高峰,此后随着治疗周期的推进逐渐下降。具体而言,首次输注期间,62%的患者报告恶心,52%的患者报告呕吐。首次出现恶心或呕吐的中位时间约为输注开始后的50分钟。这提示医护人员在首次输注时需特别警惕,并做好充分的预防和干预准备。
发生率及时间:SPOTLIGHT 和 GLOW研究的综合分析[3]显示,恶心和呕吐的发生率在佐妥昔单抗首次输注期间达到高峰,此后随着治疗周期的推进逐渐下降。具体而言,首次输注期间,62%的患者报告恶心,52%的患者报告呕吐。首次出现恶心或呕吐的中位时间约为输注开始后的50分钟。这提示医护人员在首次输注时需特别警惕,并做好充分的预防和干预准备。
![]() 输注速率的影响:研究观察到,首次输注时采用较高初始输注速率的患者,更容易因不良事件而需要调整输注速率。约有28%的患者因各种不良事件进行了输注速率调整[3]。这强调了在佐妥昔单抗输注过程中,根据患者耐受情况动态调整输注速率的重要性。
输注速率的影响:研究观察到,首次输注时采用较高初始输注速率的患者,更容易因不良事件而需要调整输注速率。约有28%的患者因各种不良事件进行了输注速率调整[3]。这强调了在佐妥昔单抗输注过程中,根据患者耐受情况动态调整输注速率的重要性。
![]() 胃切除术的影响:SPOTLIGHT和GLOW研究中,佐妥昔单抗组接受过胃切除术的患者发生恶心呕吐的频率显著低于未行切除者[1,2]。这可能与药物在胃黏膜局部作用的病理机制相关。
胃切除术的影响:SPOTLIGHT和GLOW研究中,佐妥昔单抗组接受过胃切除术的患者发生恶心呕吐的频率显著低于未行切除者[1,2]。这可能与药物在胃黏膜局部作用的病理机制相关。
![]() 对生活质量的影响:针对SPOTLIGHT和GLOW研究所做的健康相关生活质量综合分析显示,尽管最初恶心/呕吐评分有所恶化,但在化疗基础上加用佐妥昔单抗并未对患者整体生活质量产生负面影响[5]。
对生活质量的影响:针对SPOTLIGHT和GLOW研究所做的健康相关生活质量综合分析显示,尽管最初恶心/呕吐评分有所恶化,但在化疗基础上加用佐妥昔单抗并未对患者整体生活质量产生负面影响[5]。
佐妥昔单抗恶心呕吐管理共识指南与经验
![]() 为提高临床管理的规范化与有效性,国际多国专家通过德尔菲法建立了佐妥昔单抗恶心呕吐的预防与管理共识,内容涵盖了预处理方案、输注调整和动态应对策略[6]。
为提高临床管理的规范化与有效性,国际多国专家通过德尔菲法建立了佐妥昔单抗恶心呕吐的预防与管理共识,内容涵盖了预处理方案、输注调整和动态应对策略[6]。
1. 预防性止吐方案
![]() 高致吐风险止吐药物方案:参考NCCN(美国国家综合癌症网络)指南[6],建议在佐妥昔单抗首次输注和随后输注前,预防性给予高致吐风险止吐药物方案:包括NK-1受体拮抗剂+5-HT3受体拮抗剂+地塞米松±奥氮平,或帕洛诺司琼+地塞米松+奥氮平的组合。
高致吐风险止吐药物方案:参考NCCN(美国国家综合癌症网络)指南[6],建议在佐妥昔单抗首次输注和随后输注前,预防性给予高致吐风险止吐药物方案:包括NK-1受体拮抗剂+5-HT3受体拮抗剂+地塞米松±奥氮平,或帕洛诺司琼+地塞米松+奥氮平的组合。
![]() 胃黏膜保护:对于未进行全胃切除术的消化不良患者,建议在佐妥昔单抗治疗开始前几天到一周内开始服用抗溃疡药物,如质子泵抑制剂或H2受体拮抗剂,以最大限度地保护胃黏膜。
胃黏膜保护:对于未进行全胃切除术的消化不良患者,建议在佐妥昔单抗治疗开始前几天到一周内开始服用抗溃疡药物,如质子泵抑制剂或H2受体拮抗剂,以最大限度地保护胃黏膜。
2. 输注期间的动态速率调整
![]() 首次输注管理:在佐妥昔单抗首次输注期间,医护人员应密切监测患者的症状。如果出现任何呕吐症状,应考虑增加止吐治疗(如解救性止吐治疗),并立即停止输注30~60分钟,在症状明显改善后,再以较慢的速度重新开始输注。对于仅有恶心症状的患者,可考虑不做任何调整,或暂停输注30~60分钟,如果症状有所改善,随后以暂停前的速率重新开始输注。
首次输注管理:在佐妥昔单抗首次输注期间,医护人员应密切监测患者的症状。如果出现任何呕吐症状,应考虑增加止吐治疗(如解救性止吐治疗),并立即停止输注30~60分钟,在症状明显改善后,再以较慢的速度重新开始输注。对于仅有恶心症状的患者,可考虑不做任何调整,或暂停输注30~60分钟,如果症状有所改善,随后以暂停前的速率重新开始输注。
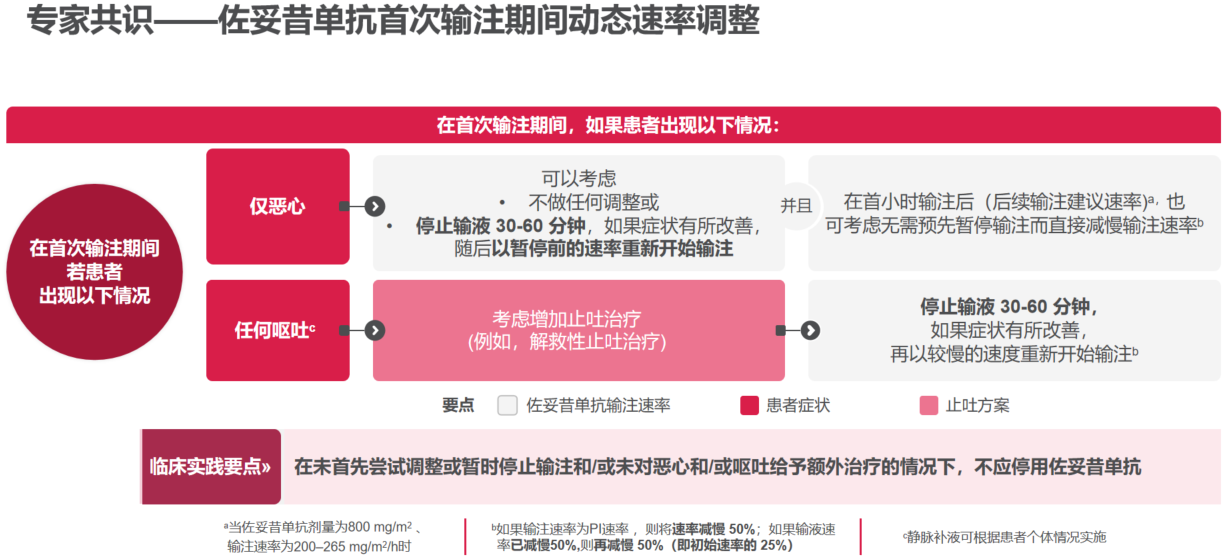
![]() 后续输注调整:在后续的治疗周期中,应根据患者在前次输注时出现的恶心呕吐的严重程度和频率,动态调整止吐方案和佐妥昔单抗的输注速率。对于出现过严重呕吐的患者,可考虑在后续周期中进一步加强预防性止吐措施或持续采用较低的输注速率。
后续输注调整:在后续的治疗周期中,应根据患者在前次输注时出现的恶心呕吐的严重程度和频率,动态调整止吐方案和佐妥昔单抗的输注速率。对于出现过严重呕吐的患者,可考虑在后续周期中进一步加强预防性止吐措施或持续采用较低的输注速率。
需要强调的是:在未首先尝试调整或暂时中断输注和/或未针对恶心和/或呕吐提供额外治疗的情况下,不应停用佐妥昔单抗。


3. 真实世界经验的启示
![]() 一项来自日本的真实世界研究[8]为佐妥昔单抗的安全性管理提供了宝贵经验。该研究表明,通过优化预防性止吐药物的使用和精细化的输注方案,佐妥昔单抗联合化疗组的呕吐发生率可以降低到与单独化疗方案相似的水平。此外,该研究还观察到,既往接受过全胃切除术的患者在佐妥昔单抗输注期间均未出现恶心或呕吐。
一项来自日本的真实世界研究[8]为佐妥昔单抗的安全性管理提供了宝贵经验。该研究表明,通过优化预防性止吐药物的使用和精细化的输注方案,佐妥昔单抗联合化疗组的呕吐发生率可以降低到与单独化疗方案相似的水平。此外,该研究还观察到,既往接受过全胃切除术的患者在佐妥昔单抗输注期间均未出现恶心或呕吐。
CLDN靶向治疗其他不良事件及管理
![]() 除了恶心和呕吐,佐妥昔单抗与化疗联用还可能引起其他不良事件,需要临床医生进行识别和管理。
除了恶心和呕吐,佐妥昔单抗与化疗联用还可能引起其他不良事件,需要临床医生进行识别和管理。
1. 超敏反应(HSR)和输液相关反应(IRR)
![]() 发生率:HSR的发生率相对较低,包括0.5%的速发严重过敏反应和1.6%的药物性超敏反应,至首次发生的中位时间分别为22天和113天。IRR的发生率为3.2%,至首次发生的中位时间为22天。
发生率:HSR的发生率相对较低,包括0.5%的速发严重过敏反应和1.6%的药物性超敏反应,至首次发生的中位时间分别为22天和113天。IRR的发生率为3.2%,至首次发生的中位时间为22天。
![]() 管理:对于速发严重过敏反应,如果是3级或4级,应立即永久停止佐妥昔单抗的输注;如果是2级,则中断输注直至<1 级,后续输注时降低输注速率,下一次输注时,应预先使用组胺药并按推荐输注速率给药,同时密切监测患者超敏反应症状和体征,可根据耐受情况逐渐增加输注速率。IRR的常见症状包括恶心、呕吐、腹痛、唾液分泌过多、发热、胸部不适、寒战、背痛、咳嗽和高血压等,多数在中断输注后可逆。对于3级或4级和2级IRR,按照剂量调整部分进行调整;下一次输注前预先使用抗组胺药,并按照推荐输注速率给药,同时密切监测患者的输液相关反应症状和体征,可根据耐受情况逐渐增加输注速率。
管理:对于速发严重过敏反应,如果是3级或4级,应立即永久停止佐妥昔单抗的输注;如果是2级,则中断输注直至<1 级,后续输注时降低输注速率,下一次输注时,应预先使用组胺药并按推荐输注速率给药,同时密切监测患者超敏反应症状和体征,可根据耐受情况逐渐增加输注速率。IRR的常见症状包括恶心、呕吐、腹痛、唾液分泌过多、发热、胸部不适、寒战、背痛、咳嗽和高血压等,多数在中断输注后可逆。对于3级或4级和2级IRR,按照剂量调整部分进行调整;下一次输注前预先使用抗组胺药,并按照推荐输注速率给药,同时密切监测患者的输液相关反应症状和体征,可根据耐受情况逐渐增加输注速率。
2. 血液学毒性
![]() 佐妥昔单抗联合化疗可能引起的血液学毒性包括贫血、血小板减少症和中性粒细胞减少症。针对这些不良事件,SPOTLIGHT和GLOW研究方案中提供了详细的管理指南,通常包括以下策略:
佐妥昔单抗联合化疗可能引起的血液学毒性包括贫血、血小板减少症和中性粒细胞减少症。针对这些不良事件,SPOTLIGHT和GLOW研究方案中提供了详细的管理指南,通常包括以下策略:
![]() 暂停治疗:根据毒性等级暂停佐妥昔单抗的治疗,直至毒性恢复到可接受的水平(如恢复至≤1级)。
暂停治疗:根据毒性等级暂停佐妥昔单抗的治疗,直至毒性恢复到可接受的水平(如恢复至≤1级)。
![]() 剂量调整:对于某些持续性或复发性血液学毒性,可能需要考虑减低佐妥昔单抗的剂量。
剂量调整:对于某些持续性或复发性血液学毒性,可能需要考虑减低佐妥昔单抗的剂量。
![]() 重启标准:在毒性缓解并达到安全重启标准后,方可考虑重新开始佐妥昔单抗的治疗。同时,可能需要对化疗方案进行相应的剂量调整或支持治疗(如使用粒细胞集落刺激因子G-CSF)。
重启标准:在毒性缓解并达到安全重启标准后,方可考虑重新开始佐妥昔单抗的治疗。同时,可能需要对化疗方案进行相应的剂量调整或支持治疗(如使用粒细胞集落刺激因子G-CSF)。
3. 其他CLDN18.2靶向药物应关注的毒性
![]() 目前,包括单抗、双抗、ADC、CAR-T在内的CLDN18.2相关产品管线已全面铺开,不同形式的CLDN18.2靶向药物在毒性谱方面存在差异,应根据药物机制和患者特征进行个体化管理。比如, CMG901(ADC)常见血液学和胃肠道毒性;AMG910和IBI389(CLDN18.2/CD3双抗)需关注肝脏毒性和CRS(细胞因子释放综合征);CT041(CAR-T)需关注血液学毒性及CRS。
目前,包括单抗、双抗、ADC、CAR-T在内的CLDN18.2相关产品管线已全面铺开,不同形式的CLDN18.2靶向药物在毒性谱方面存在差异,应根据药物机制和患者特征进行个体化管理。比如, CMG901(ADC)常见血液学和胃肠道毒性;AMG910和IBI389(CLDN18.2/CD3双抗)需关注肝脏毒性和CRS(细胞因子释放综合征);CT041(CAR-T)需关注血液学毒性及CRS。
总结
![]() 佐妥昔单抗作为首个靶向CLDN18.2的单克隆抗体,用于晚期胃癌的一线治疗显著改善了患者预后。尽管恶心和呕吐其是最常见的不良反应,但通过优化止吐方案与输注速率调整,可大幅降低其发生率,避免不必要的停药,提升患者治疗体验与依从性。
佐妥昔单抗作为首个靶向CLDN18.2的单克隆抗体,用于晚期胃癌的一线治疗显著改善了患者预后。尽管恶心和呕吐其是最常见的不良反应,但通过优化止吐方案与输注速率调整,可大幅降低其发生率,避免不必要的停药,提升患者治疗体验与依从性。
![]() 此外,佐妥昔单抗整体安全性良好,超敏与输液相关反应发生率低。其他CLDN18.2靶向药物在未来推广中也需关注其特异性毒性特征。随着真实世界经验的积累,临床管理策略将日益成熟,为患者带来更长远的生存获益与生活质量改善。
此外,佐妥昔单抗整体安全性良好,超敏与输液相关反应发生率低。其他CLDN18.2靶向药物在未来推广中也需关注其特异性毒性特征。随着真实世界经验的积累,临床管理策略将日益成熟,为患者带来更长远的生存获益与生活质量改善。
专家观点
![]() 徐瑞华教授:佐妥昔单抗作为全球首个上市的CLDN18.2靶向抗体药物,在SPOTLIGHT与GLOW研究中展现了良好的疗效和可控的安全性。我们在临床中发现,预防性使用止吐药、优化输注速率,以及充分的患者教育,是提升患者依从性、确保治疗顺利推进的关键。通过规范化的管理措施,绝大多数患者都能顺利完成治疗并从中获益。
徐瑞华教授:佐妥昔单抗作为全球首个上市的CLDN18.2靶向抗体药物,在SPOTLIGHT与GLOW研究中展现了良好的疗效和可控的安全性。我们在临床中发现,预防性使用止吐药、优化输注速率,以及充分的患者教育,是提升患者依从性、确保治疗顺利推进的关键。通过规范化的管理措施,绝大多数患者都能顺利完成治疗并从中获益。
![]() 李进教授:CLDN18.2靶点药物的研发成功是胃癌精准治疗的重要突破,佐妥昔单抗联合化疗已成为国内外指南中CLDN18.2阳性、HER2阴性晚期胃癌一线治疗的新标准。治疗过程中,患者初期可能会经历轻中度胃肠道不适,但大多可通过调整输注速度与预防性止吐方案有效控制。随着治疗的推进,患者的耐受性明显提升。积极沟通、及时干预,是保障疗效的重要保障。
李进教授:CLDN18.2靶点药物的研发成功是胃癌精准治疗的重要突破,佐妥昔单抗联合化疗已成为国内外指南中CLDN18.2阳性、HER2阴性晚期胃癌一线治疗的新标准。治疗过程中,患者初期可能会经历轻中度胃肠道不适,但大多可通过调整输注速度与预防性止吐方案有效控制。随着治疗的推进,患者的耐受性明显提升。积极沟通、及时干预,是保障疗效的重要保障。
![]() 梁军教授:临床实践表明,佐妥昔单抗引起的胃肠道反应具有一定规律性,通常发生在初次输注阶段,后续逐渐减轻。通过优化给药流程、加强医护培训,以及制定清晰的管理流程,可显著提升患者体验和治疗连续性。在安全管理日趋成熟的基础上,我们有理由期待该药在更广泛人群中发挥更大价值。
梁军教授:临床实践表明,佐妥昔单抗引起的胃肠道反应具有一定规律性,通常发生在初次输注阶段,后续逐渐减轻。通过优化给药流程、加强医护培训,以及制定清晰的管理流程,可显著提升患者体验和治疗连续性。在安全管理日趋成熟的基础上,我们有理由期待该药在更广泛人群中发挥更大价值。
参考文献
[1]Shitara K, Shah MA, Lordick F, et al. Zolbetuximab in Gastric or Gastroesophageal Junction Adenocarcinoma. N Engl J Med. 2024;391(12):1159-1162.
[2]Shitara K, Pophale R, Matsangou M, et al. Management of nausea and vomiting (N/V) following first-line (1L) zolbetuximab + chemotherapy treatment in claudin-18.2 (CLDN18.2)+, HER2−, locally advanced (LA) unresectable or metastatic gastric or gastroesophageal junction (mG/GEJ) adenocarcinoma: Analysis from the phase 3 SPOTLIGHT and GLOW studies. 2024 ASCO GI, abstr 372.
[3]Shitara K, Van Cutsem E, Lordick F, et al. Final overall survival results from phase 3 SPOTLIGHT study evaluating zolbetuximab + mFOLFOX6 as first-line (1L) treatment for patients (pts) with claudin 18 isoform 2 (CLDN18.2)+, HER2−, locally advanced (LA) unresectable or metastatic gastric or gastroesophageal junction (mG/GEJ) adenocarcinoma. 2024 ASCO, abstr 4036.
[4]Kinugasa F, Kajikawa S, Weng J, et al. Effect of antiemetics on zolbetuximab-induced gastric injury and emesis in ferrets. J Pharmacol Sci. 2024;156(3):161-170.
[5]Lordick F, Van Cutsem E, Shitara K, et al. Health-related quality of life in patients with CLDN18.2-positive, locally advanced unresectable or metastatic gastric or gastroesophageal junction adenocarcinoma: results from the SPOTLIGHT and GLOW clinical trials. ESMO Open. 2024;9(8):103663.
[6]Klempner SJ , Pazo-Cid RA , Lonardi S ,et al. Consensus guidance for prevention and management of nausea and vomiting in patients treated with zolbetuximab+ chemotherapy: a RAND/UCLA modified Delphi panel study. ESMO Gastrointestinal Oncology, 7[2025-07-15].
[7]NCCN Clinical Practice Guidelines in Oncology for Antiemesis V.2.2024.
[8]Shimozaki K, Ooki A, Yamahata Y, et al. Managing zolbetuximab-induced nausea and vomiting: a proposal for a pragmatic approach in clinical practice. ESMO Gastrointest Oncol. 2025,7: 100128.
本文由安斯泰来提供,仅供医疗卫生等专业人士参考
审批编号:MAT-CN-VYL-2025-00210
排版编辑:肿瘤资讯-王俊澔
往期回顾:
CLDN18.2微课堂|徐瑞华教授:GLOW研究证实佐妥昔单抗的治疗潜力,胃癌晚期一线治疗迎来新高峰!
CLDN18.2微课堂|徐建明教授:SPOTLIGHT研究最终中位OS长达18.2个月!佐妥昔单抗重塑晚期胃癌一线治疗格局!
CLDN18.2微课堂|李进教授:SPOTLIGHT&GLOW研究,照亮胃癌精准治疗之路
CLDN18.2微课堂丨薛俊丽教授:透视SPOTLIGHT&GLOW的中国亚组数据,剖析佐妥昔单抗在中国晚期胃癌一线的临床价值
CLDN18.2微课堂丨刘天舒教授:免疫靶向时代,晚期胃癌一线治疗如何布局
CLDN18.2微课堂丨梁寒教授:新兴靶点潜力巨大,胃癌晚期一线靶向策略革新
CLDN18.2微课堂丨陈凛教授:聚焦CLDN18.2,精准靶向如何重塑晚期胃癌一线治疗?
CLDN18.2微课堂丨曲秀娟教授:靶向CLDN18.2,佐妥昔单抗开启胃癌精准治疗新时代
CLDN18.2微课堂丨季加孚教授:CLDN18.2的前世今生
CLDN18.2微课堂 | 张小田教授:胃癌年度十大热词榜发布,前四项中CLDN18.2及相关研究霸榜三项
CLDN18.2微课堂丨袁响林教授:权威认可!佐妥昔单抗联合化疗以1类证据获最新版NCCN胃癌指南一线治疗优先推荐
CLDN18.2微课堂 | 梁军教授:从日本到欧美再到中国,佐妥昔单抗的全球获批之旅
CLDN18.2微课堂丨毕锋教授:从实验室到临床——CLDN18.2靶向治疗如何改变胃癌治疗范式?
CLDN18.2微课堂丨龙健婷教授:从HER2到Claudin 18.2,胃癌靶向治疗渐入佳境
CLDN18.2微课堂丨林小燕教授:一线曙光,佐妥昔单抗为CLDN18.2阳性晚期胃癌患者带来优质新选择
CLDN18.2微课堂 | 赵岩教授:创新驱动,揭秘佐妥昔单抗从靶点发现到胃癌一线获批背后的故事
CLDN18.2微课堂丨应杰儿教授:从佐妥昔单抗的疗效剖析CLDN18.2作为胃癌一线药物开发的关键靶点
CLDN18.2微课堂 | 刘宝瑞教授:注重CLDN18.2检测, 实现胃癌一线精准治疗新突破
CLDN18.2微课堂丨魏嘉教授:胃癌一线精准治疗新纪元——CLDN18.2检测如何助力个体化治疗?
CLDN18.2微课堂丨束永前教授:晚期胃癌一线治疗的新靶点,聚焦CLDN18.2
CLDN18.2微课堂丨曾珊教授:揭秘佐妥昔单抗研发背后的故事,CLDN18.2引领晚期胃癌一线靶向治疗新格局
CLDN18.2微课堂|杨菊教授:胃癌患者生存之旅,佐妥昔单抗助力CLDN18.2阳性晚期胃癌患者重获治愈生机
CLDN18.2微课堂 | 张艳桥教授:基于CSCO指南,看佐妥昔单抗一线治疗的临床获益
CLDN18.2微课堂丨34个月PFS!通过一则病例看佐妥昔单抗在晚期胃癌精准治疗的惊人潜力
CLDN18.2微课堂丨高危不等于无解,一则胃癌腹膜转移一线佐妥昔单抗联合化疗案例PFS长达12个月
CLDN18.2微课堂丨SPOTLIGHT全球首席研究者Kohei Shitara教授介绍佐妥昔单抗在全球及日本的安全性管理经验
CLDN18.2微课堂 | 河北大学附院王志宇教授团队一例晚期胃癌佐妥昔单抗助力转化成功案例,重获根治希望
CLDN18.2微课堂 | 刘天舒教授团队介绍一例佐妥昔单抗联合化疗方案动态调整下胃癌肝转移患者PFS仍达11个月的案例
CLDN18.2微课堂 | 国风教授解读佐妥昔单抗从基础研究到临床转化的研发之旅
CLDN18.2微课堂 | 一线有“靶”,生存可期:佐妥昔单抗助力胃癌术后复发患者实现37个月长生存











 苏公网安备32059002004080号
苏公网安备32059002004080号


