套细胞淋巴瘤(MCL)是一种起源于成熟B细胞的非霍奇金淋巴瘤亚类,占非霍奇金淋巴瘤(NHL)的6%~8%。诊断时80%以上的患者处于疾病晚期。MCL兼具侵袭性淋巴瘤疾病进展迅速和惰性淋巴瘤不可治愈的特点[1]。大剂量化疗是晚期MCL的主要治疗手段,明显延长患者的生存期[2]。但是,化疗导致的血小板减少症是临床常见的血液系统毒性反应,可能造成患者的化疗药物剂量降低、化疗时间延迟甚至终止化疗,增加出血风险,从而危及患者生命,并影响治疗效果、增加治疗费用[3]。
病例分享专家
中山大学肿瘤防治中心王华医生分享了一例MCL患者在多疗程联合化疗后出现血小板减少症的诊疗思路。广东省人民医院李文瑜教授据此进行了精彩点评。CCMTV血液科特别整理报道,以期为血液科医生践行淋巴瘤规范临床诊疗带来更多思考与启示。
中国抗癌协会肿瘤与微生态专业委员会青委副主委
中国抗癌协会康复会血液分会委员
广东省预防医学会血液肿瘤专委会常委
广州抗癌协会肿瘤复发与转移专业委员会常委
广东省抗癌协会化疗专业委员会委员
广东省抗癌协会靶向与个体化治疗专业委员会委员
广东省抗癌协会肿瘤姑息与康复治疗青委会常委
广东省医学会血液病分会青年委员
以第一或通讯作者发表SCI论文30余篇,主持国家自然基金、广东省自然基金等6项科研项目
专业方向:淋巴造血系统肿瘤的综合诊治
对多发性骨髓瘤和侵袭性淋巴瘤有较丰富经验
病例资料
基本信息
一般资料:患者男性,48岁。
主诉:乏力,体重下降半年余。
现病史:患者半年前(2022.10)无诱因出现乏力、体重下降约6 KG,无头晕、头痛,无发热、盗汗,遂患者就诊于南方医科大学南方医院。
血常规检查(2023.2.27):WBC 24.81×109/L,Hgb 119 g/L,PLT 85×109/L。
骨髓穿刺活检病理(2023.3.10):免疫表型符合套细胞淋巴瘤侵犯骨髓。
PET/CT检查(2023.2.27):1、脾脏明显增大、代谢弥漫中度增高,考虑为血液系统恶性肿瘤侵犯;2、全身骨髓代谢弥漫性中度增高(以第一腰椎椎体为著),考虑为血液系统恶性肿瘤侵犯;3、双侧颈部、双侧肩颈部、双侧锁骨上窝、双侧腋窝、胸骨两旁、双肺门、纵膈内、右侧第9后肋前方、右侧心膈角、双侧横膈上、双侧膈肌角深面、肝门区、脾门区、胰头周围、腹膜后区、双侧髂血管旁及双侧腹股沟区见多发淋巴结增大,代谢不同程度增高,考虑为血液系统恶性肿瘤侵犯全身多处淋巴结。
辅助检查
入院检查
血常规检查(2023.2.27):WBC 24.81×109/L,Hgb 119 g/L,PLT 85×109/L
骨髓穿刺活检病理(2023.3.10):免疫表型符合套细胞淋巴瘤侵犯骨髓。
PET/CT检查(2023.2.27):
1、脾脏明显增大、代谢弥漫中度增高,考虑为血液系统恶性肿瘤侵犯;
2、全身骨髓代谢弥漫性中度增高(以第一腰椎椎体为著),考虑为血液系统恶性肿瘤侵犯;
3、双侧颈部、双侧肩颈部、双侧锁骨上窝、双侧腋窝、胸骨两旁、双肺门、纵膈内、右侧第9后肋前方、右侧心膈角、双侧横膈上、双侧膈肌角深面、肝门区、脾门区、胰头周围、腹膜后区、双侧髂血管旁及双侧腹股沟区见多发淋巴结增大,代谢不同程度增高,考虑为血液系统恶性肿瘤侵犯全身多处淋巴结。
骨髓涂片检查:行骨髓穿刺示:骨髓取材血稀,不典型淋巴细胞占 29%,免疫表型倾向套细胞淋巴瘤侵犯骨髓。
PET/CT 检查:1、脾大、代谢弥漫中度增高,考虑为血液系统恶性肿瘤侵犯;2、全身骨髓代谢弥漫性中度增高,考虑为血液系统恶性肿瘤侵犯;3、全身多发淋巴结肿大,考虑为血液系统恶性肿瘤侵犯全身多处淋巴结。
经入院后检查诊断为套细胞淋巴瘤IV期(sMIPI评分:4分,中危)
治疗经过
诱导治疗阶段

在ZR-DHAOX方案的第一疗程(C4)化疗后,该病例出现3级血小板减少症(PLT计数45×109/L),给予海曲泊帕7.5 mg/d(d1~7),PLT计数升高至186×106/L。在后续化疗期间(C5、C6和C8),继续采用海曲泊帕7.5 mg/d(d1~7)进行二级预防,未再次出现血小板减少症,血小板计数维持在正常范围内。
血小板计数变化情况
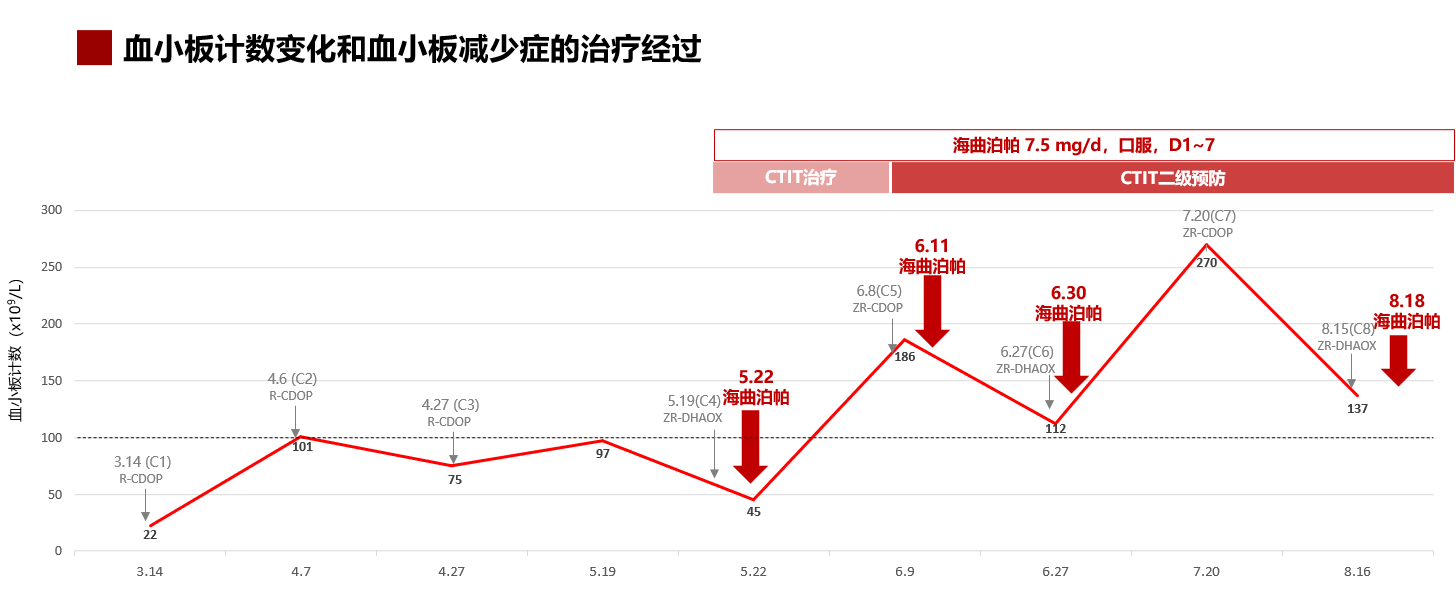
诊疗思考
抗肿瘤方案的选择
对于年轻MCL患者(本病例为IV期,sMIPI评分4分,中危),NCCN指南推荐了R-CHOP/R-DHAP交替方案,继以移植(即AB交替+移植方案)。该治疗方案的风险/获益较为平衡,目前是大多数MCL患者的首选治疗方案[1,5]。
对于本病例的治疗,为了降低心脏毒性,将R-CHOP方案中的多柔比星改为含聚乙二醇脂质体多柔比星,即采用R-CDOP方案治疗(C1~C3)[6]。
根据欧洲MCL协作组发起的针对年轻初治II~IV期MCL患者的Triangle研究,发现与标准治疗(R-CHOP/R-DHAP+ASCT,A组)相比,标准治疗联合伊布替尼(A+I组)疗效显著更优,中位随访31个月的无失败生存率(FFS)显著更高(88% vs 72%,P=0.0008,HR=0.52),且毒性反应可接受[5]。
另外,为保证抗肿瘤疗效的同时,降低阿糖胞苷的毒性,采用了ZR-CDOP/ZR-DHAOX 交替方案。CHESS chemo-less研究显示ZR-DHAOX方案(ZR诱导序贯R-DHAOX方案4周期短期化疗)对初治MCL疗效好,ZR诱导治疗(中位4周期)CR率88.2%[7,8]。
因此,从第4周期改为ZR-CDOP/ZR-DHAOX交替方案(免疫化疗联合泽布替尼)。本病例在采用ZR-CDOP/ZR-DHAOX 交替方案之后达到完全缓解,提示为其制定的治疗方案疗效佳。
抗肿瘤治疗期间血小板减少症的防治
本病例开始化疗时(C1)PLT计数为22×109/L,考虑为肿瘤侵犯骨髓所致。C2之前PLT计数恢复至正常水平。在ZR-DHAOX第一疗程化疗后(C4)出现3级血小板减少症(45×109/L),经过检查和评估,考虑为肿瘤治疗所致血小板减少症(CTIT)。
研究显示,血液系统恶性肿瘤患者化疗后血小板减少症的3个月累积发生率高达28%[9]。化疗所致血小板减少症的发生率因使用不同药物有很大差异,其中吉西他滨和铂类为基础方案发生率最高[3]。
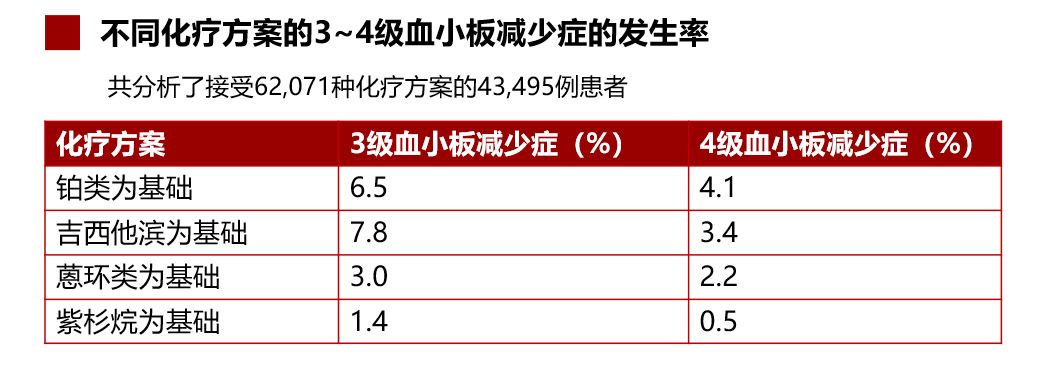
结合治疗经过和循证证据,考虑本病例发生CTIT可能有如下原因:ZR-DHAOX方案含有的铂类和泽布替尼均可以引起血小板减少症,阿糖胞苷可能导致严重骨髓抑制[3,10]。另外,既往发现R-CHOP方案的3~4级血小板减少症发生率为5%~9%。本病例在C1~C3应用了R-CDOP方案,在开始C3治疗时血小板计数降低(75×109/L),因此该方案也可能与3级血小板减少症发生相关[3]。
针对本病例发生的CTIT,立即给予TPO受体激动剂(TPO-RA)海曲泊帕治疗,血小板计数迅速恢复正常,说明海曲泊帕在该淋巴瘤患者大剂量化疗后可以快速、有效提升血小板计数。
海曲泊帕是我国自主研发的新一代口服、小分子、非肽类TPO-RA,化学结构与艾曲泊帕、阿伐曲泊帕等同类产品不同,其结构有所升级,增强了亲脂性,提高了药效,降低了肝脏毒性。此外,海曲泊帕作为口服制剂具有给药便捷的优势。
在2023年欧洲内科医学大会(ECIM)现场,哈尔滨血液病肿瘤研究所马军教授以口头报告的形式公布了一项海曲泊帕(起始剂量7.5 mg/d)治疗CTIT患者的多中心、随机对照II期研究结果。与安慰剂相比,海曲泊帕可显著提高CTIT患者的治疗有效率(60.7% vs 12.9%;OR=10.4;95%CI2.8~36.7P=0.0001),且耐受性良好[11]。
《CSCO肿瘤治疗所致血小板减少症诊疗指南2023》推荐,无论CTIT是否伴有出血,均可应用海曲泊帕或海曲泊帕联合rhTPO治疗。指南同时推荐海曲泊帕用于CTIT的二级预防[3]。
在本病例的后续化疗期间,考虑到具有CTIT出血高危因素(接受含铂类、阿糖胞苷、蒽环类方案治疗),CTIT二级预防指征明确,因此继续给予海曲泊帕进行CTIT的二级预防。该病例未再发生CTIT,血小板计数一直稳定在正常水平。
回顾整个治疗过程,采用新一代TPO-RA海曲泊帕及时治疗CTIT和后续进行二级预防保障了抗肿瘤治疗的顺利进行,最终患者取得了满意的疗效。
1.中国抗癌协会血液肿瘤专业委员会等.套细胞淋巴瘤诊断与治疗中国指南(2022年版)》.中华血液学杂志.中华血液学杂志.2022;43(7):529-536.
2.Fischer L, et al. The addition of rituximab to chemotherapy improves overall survival in mantle cell lymphoma-a pooled trials analysis. Ann Hematol. 2023;102(10):2791-2801.
3.中国临床肿瘤学会指南工作委员会.中国临床肿瘤学会(CSCO)肿瘤治疗所致血小板减少症诊疗指南2023.人民卫生出版社.
4.中国临床肿瘤学会指南工作委员会.中国临床肿瘤学会(CSCO)淋巴瘤诊疗指南2022.人民卫生出版社.
5.NCCN guideline B cell lymphoma 2023 v6.
6.常莹莹等.含聚乙二醇脂质体多柔比星的R-CDOP方案治疗弥漫性大B细胞淋巴瘤的临床应用评价.实用肿瘤杂志.2021;36(05):429-434.
7.Cai Q, et al. Frontline Treatment with Zanubrutinib Plus Rituximab (ZR) Followed By Short Course R-Dhaox Shows Potent Efficacy in Patients with Mantle Cell Lymphoma (MCL) - Preliminary Results of Phase II CHESS Clinical Trial. Blood (2022) 140 (Supplement 1): 9356–9357.
8. https://clinicaltrials.gov/study/NCT04624958
9.Shaw JL, et al. The incidence of thrombocytopenia in adult patients receiving chemotherapy for solid tumors or hematologic malignancies. Eur J Haematol. 2021;106(5):662-672.
10.泽布替尼胶囊(百悦泽)中文说明书.
11. Jun Ma, et al. A multicenter, randomized phase II trial on the efficacy and safety of hetrombopag for the treatment of chemotherapy-induced thrombocytopenia in patients with advanced solid tumors. 2023 European Congress of Internal Medicine, Abstract 2360.
12. 中国抗癌协会肿瘤临床化疗专业委员会,中国抗癌协会肿瘤支持治疗专业委员会. 中国肿瘤药物相关血小板减少诊疗专家共识(2023版). 中华医学杂志,2023,103(33):2579-2590.
13.刘福佳等.血液系统恶性肿瘤疾病患者接受造血干细胞移植期间血小板减少症相关新进展.国际输血及血液学杂志.2020;43(5):383-390.
排版编辑:肿瘤资讯-王俊澔











 苏公网安备32059002004080号
苏公网安备32059002004080号


