病史摘要:患者,男性,39岁,1年余前因“右肝癌术后15月”前来我院治疗。
症状体征:患者ECOG评分为0分,神志清楚,腹部平坦。在右上腹肋缘下可见一条18厘米长的J型手术瘢痕,愈合良好。腹部软,无压痛或反跳痛,全腹未触及明显肿块,Murphy征阴性,肝脾肋下未触及肿大,肝肾区无叩击痛,腹部叩诊呈鼓音,移动性浊音为阴性。肠鸣音频率为每分钟4次。
诊断方法:患者有乙肝病史,根据AFP升高,CT及MR影像学呈现典型的“快进快出”表现,临床诊断为原发性肝癌。
治疗方法:患者的治疗方法包括靶向治疗和免疫治疗。其中,靶向治疗采用了仑伐替尼,而免疫治疗采用了替雷利珠单抗。
临床转归:好转
适合阅读人群:肝胆胰外科,肿瘤内科
关键词:原发性肝癌,中性粒细胞减少,粒细胞减少性发热,预防性G-CSF使用
引言
化疗引发的中性粒细胞减少(CIN)是指在接受骨髓抑制性化疗药物后,外周血中的中性粒细胞绝对值(ANC)降低至低于正常水平,即血液检查显示ANC<2.0×10^9/L。当中性粒细胞减少到严重程度并伴随发热时,我们称之为中性粒细胞减少性发热(FN)。严重中性粒细胞减少是指ANC<0.5×10^9/L或ANC<1.0×10^9/L但预计在接下来的48小时内会下降到<0.5×10^9/L;而发热是指口腔温度单次测量≥ 38.3℃或持续高于38.0℃超过1小时。CIN会增加患者发生感染的风险,尤其是粒细胞减少性发热(FN),这些可能导致治疗费用的增加、抗生素的使用、住院时间的延长,严重者可导致感染性休克、脓毒综合征等危及生命的并发症,甚至导致患者死亡。该患者患有肝癌,并接受多种疗程的靶向免疫治疗,但由于肝硬化严重,脾功能亢进,治疗过程中常伴有三系细胞减少,导致治疗不得不中断。本文我们将分享关于硫培非格司亭在预防肿瘤患者化疗相关中重度中性粒细胞减少方面的所取得的积极成果。希望这些治疗经验为患者提供了更多的治疗选择,并对他们的生存和生活质量产生了积极的影响。
临床资料
一般资料
患者,男性,39岁,患者于一年多前因右肝占位到我院就诊,随后在2022年3月15日接受了肝VIII段切除术和左肝活检术。术后病理诊断为右肝结节型中分化肝细胞癌(pT2N0M0,II期)。随后在2022年4月29日接受了术后预防性TACE治疗。2022年6月6日复查肝脏MR报告显示肝S8段、S7包膜处有新增病灶,考虑为复发/转移并伴有肝中静脉及部分肝右静脉癌栓形成的可能性。自2022年6月22日开始至今,患者接受了“仑伐替尼 8mg qd”的靶向治疗。期间在2022年6月30日至2022年7月26日期间诊断为复发灶进行放射治疗。此外,在2022年6月13日、2022年8月19日、2022年9月9日、2022年9月30日、2022年10月21日、2023年1月17日、2023年2月8日、2023年3月7日、2023年3月30日、2023年4月30日、2023年5月28日、2023年6月27日接受了“替雷利珠单抗”免疫治疗(200mg q3w)。现在患者因继续治疗而来就诊,门诊拟为“肝癌术后复发多程治疗中”收入住院。既往史无特殊。查体显示腹平坦,右上腹肋缘下可见一18厘米J型手术瘢痕,愈合良好。腹部软,无压痛或反跳痛。
检查
血常规(2023.07.18):白细胞计数 1.38×10^9/L,红细胞计数 4.49×10^12/L,血红蛋白 138g/L,血小板计数 50×10^9/L
常规生化全套(2023.07.18);白蛋白 67.6g/L,谷丙转氨酶 54U/L,谷草转氨酶 127U/L,尿素 4.25mmol/L,肌酐 77umol/L;
AFP(2023.07.18):2.41ng/ml,PIVKA-II 80mAU/ml
PCT、CRP、心肌酶谱、甲状腺功能未见明显异常。
影像学检查(2023.07.21)
胸部CT:双肺下叶少许纤维增殖灶,扫描范围内肝脏见低密度灶内伴团块状致密灶。
上腹部CT:原发性肝细胞癌术后介入治疗后改变,建议必要时MRI检查;肝周少量积液与前相仿;肝硬化并门脉高压、脾肿大;慢性胆囊炎;胆囊结石;腹膜增厚与前相仿。(见图1)
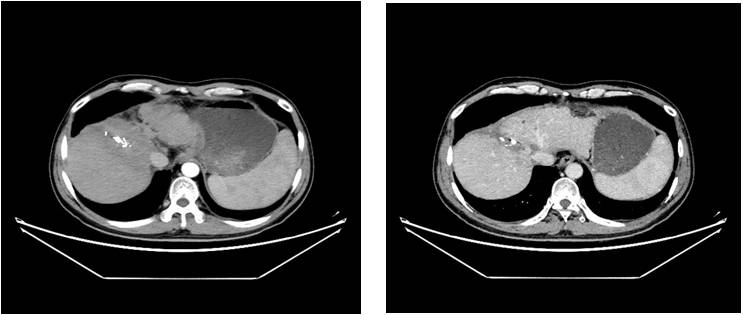
诊断与鉴别诊断
患者诊断为右肝结节型中分化肝细胞癌(pT2N0M0,II期),术后经TACE治疗后复发,伴有肝中静脉及部分肝右静脉癌栓形成。随后接受放射治疗和免疫治疗,目前正在进行靶向治疗。根据医学证据,无需进行鉴别诊断,因为患者的临床表现和检查结果已经明确了肝癌的诊断和治疗方案。
治疗
在科室的一致讨论下,决定为患者制定了仑伐替尼 8mg qd 和替雷利珠单抗 200mg 的靶向治疗和免疫治疗方案,第一周期治疗于2023年1月16日开始。基线血常规检查显示白细胞计数为 2.57×10^9/L,中性粒细胞绝对值为 2.0×10^9/L,红细胞计数为 4.05×10^12/L,血红蛋白为 120g/L,血小板计数为 127×10^9/L。在2023年1月4日开始使用硫培非格司亭6mg进行治疗,4天后的血常规复查显示白细胞计数显著上升至 9.86×10^9/L,中性粒细胞绝对值同样显著上升至 8.83×10^9/L。红细胞计数轻微增加至 4.26×10^12/L,血红蛋白轻微上升至 133g/L。然而,血小板计数下降至 41×10^9/L,需要进一步监测和评估。第二周期治疗前的血常规检查(2023年2月7日)显示白细胞计数为 3.13×10^9/L,中性粒细胞绝对值为 2.40×10^9/L,红细胞计数增加至 5.18×10^12/L,血红蛋白升至 158g/L,血小板计数为 102×10^9/L,治疗过程顺利进行,未出现明显不良反应。在治疗过程中,未发现合并使用其他升白药物的情况。这些结果表明患者在接受药物治疗后,白细胞计数和中性粒细胞绝对值均有明显上升,而血小板计数下降,但在第二周期治疗前,血常规指标基本恢复到正常范围,显示出治疗的有效性和耐受性。
治疗结果、随访及转归
在接下来的治疗过程中,患者于2023年3月7日、2023年4月30日和2023年5月28日进行了后续3个周期的靶向免疫治疗,足剂量足疗程的完成。治疗期间患者病情好转。
讨论
本文讨论了中性粒细胞减少症(CIN)在化疗中的影响及其预防和治疗。CIN是化疗常见的副作用之一,可能导致化疗剂量的延迟和减少,对患者的生存期和无进展生存期有显著影响。特别是中性粒细胞减少伴发热(FN),会显著增加患者的并发症风险。预防性使用硫培非格司亭已被证实可以有效降低3/4级中性粒细胞减少及FN的发生率,其中一级预防比二级预防更有效。
CIN的定义是化疗后外周血中性粒细胞绝对计数(ANC)的降低,ANC < 2.0×10^9/L。根据美国国家癌症研究所不良事件通用术语标准5.0版,中性粒细胞减少分为四级。CIN的谷值通常出现在化疗后第7~14天。中性粒细胞的发育成熟过程是一个复杂的生理现象,从原始粒细胞到成熟中性粒细胞的整个过程约需7~14天。化疗引起的骨髓抑制包括急性和潜在骨髓损伤,中性粒细胞减少的程度与化疗药物的种类和剂量有关。FN是指严重的中性粒细胞减少合并发热,发热定义为单次口腔温度≥38.3℃或≥38.0℃持续超过1小时。FN发生风险评估涉及特定化疗药物的骨髓毒性、剂量强度、患者自身因素及联合用药。
本研究报告了一名39岁男性肝细胞癌患者接受综合治疗的病例。患者接受了肝切除术、预防性TACE治疗、放射治疗、靶向治疗和免疫治疗。在治疗过程中,患者使用了硫培非格司亭,结果显示白细胞计数和中性粒细胞绝对值均有显著上升,而血小板计数有所下降,但在第二周期治疗前,血常规指标基本恢复至正常范围,显示出治疗的有效性和耐受性[1]。
总结来说,CIN是化疗中常见的副作用,对患者的治疗进程和预后有显著影响。预防性使用硫培非格司亭可以有效降低CIN的发生率,改善患者的治疗效果和预后。同时,本研究的病例报告也显示了硫培非格司亭在实际临床治疗中的有效性和耐受性。临床治疗中,个体化医疗可能通过更精准地识别患者的风险因素,为每位患者提供定制化的预防和治疗方案。对CIN患者进行长期随访,评估不同预防和治疗策略的晚期效果,有助于进一步优化治疗方案,并为未来的临床实践提供更多的证据支持。CIN的预防和治疗是一个多方面的挑战,需要综合考虑药物干预、个体化医疗、生活方式调整等多种因素。未来的研究需要在这些领域进行更深入的探索,以期为患者提供更有效、更安全、更经济的治疗方案。
利益冲突声明:所有作者均声明本研究不存在利益冲突。
[1] 中国抗癌协会肿瘤临床化疗专业委员会,中国抗癌协会肿瘤支持治疗专业委员会. 肿瘤化疗导致的中性粒细胞减少诊治中国专家共识(2023版). 中华肿瘤杂志,2023,45(07):575-583. DOI:10.3760/cma.j.cn112152-20230224-00076
排版编辑:肿瘤资讯-王俊澔











 苏公网安备32059002004080号
苏公网安备32059002004080号


