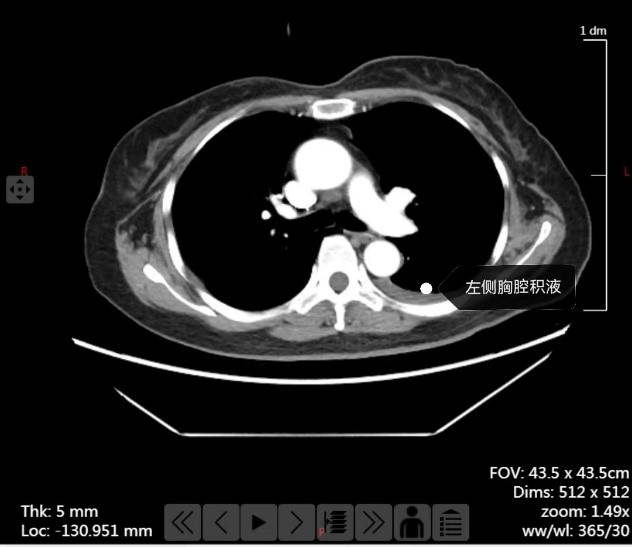
病史摘要:患者女,60岁,因“卵巢癌术后2年余,下腹胀痛15天”于2023年12月入院。2年前(2021-08-10)因卵巢癌IIIC期于我科在全麻下行经腹全子宫+双附件+大网膜切除术。术后病理结果回报(B202134624):“双侧卵巢”高级别乳头状浆液性癌,侵及局部区卵巢表面。术后BRCA基因胚系及体系均未检测到突变,HRD阴性。术后予以顺铂腹腔热灌注化疗+紫杉醇脂质体全身静脉化疗1次、紫杉醇脂质体+卡铂全身静脉化疗5周期。术后动态监测肿瘤标志物及影像学未见异常。15天前患者出现下腹胀痛,就诊外院提示CA125 443.4 U/mL HE4 309.3pmol/L,胸部CT:右肺上叶微结节,右肺下叶新发条索影,左侧胸腔积液形成,左侧膈肌抬高,左肺下叶稍膨胀不全。
症状体征:妇科检查:外阴:已婚经产式,阴毛呈女性分布。阴道:通畅,粘膜萎缩,无异常分泌物,盲端可触及质硬结节。盆腔:空虚,无压痛,无反跳痛。
诊断方法:根据病史、体征、肿瘤标志物、影像可确诊,初步诊断:复发性卵巢癌。
治疗方法:考虑患者系铂敏感复发,术前诊断卵巢癌IIIC期,予以TC方案加贝伐珠单抗化疗。具体:2023-12-15紫杉醇脂质体270mg+卡铂650mg+贝伐珠单抗600mg。后分别于2024-01-05、2024-01-26序贯2周期同剂量化疗,2024-02-21行力扑素270mg+卡铂650mg+贝伐珠单抗997.50mg全身静脉化疗。前3周期化疗后24h给予硫培非格司亭6mg,ih。
临床转归:TC方案+贝伐珠单抗辅助化疗后24h给予硫培非格司亭后复查三系细胞计数均处于大致正常范围。硫培非格司亭可预防复发性卵巢癌辅助化疗后中性粒细胞减少症的发生。
适合阅读人群:妇科;妇科肿瘤
关键词:硫培非格司亭;TC方案;贝伐珠单抗;复发性卵巢癌;中性粒细胞减少症
引言
流行病学数据显示,卵巢癌(ovarian cancer, OC)在妇科恶性肿瘤中死亡率位居第一,其5年生存率约为47%,主要死亡原因是复发和化疗耐药[1]。大约70%的晚期OC患者在一线治疗后3年内出现复发。复发性卵巢癌(recurrent ovarian cancer, ROC)是指初诊时行肿瘤减灭术联合化疗等方法治疗并达到完全缓解,在停止治疗后重新出现病灶(主要位于上腹部及盆腹腔脏器,主要涉及膈肌、肝脏、脾脏、膀胱、输尿管、乙状结肠、直肠等),临床多表现为CA125升高,影像学检查提示有肿块,且出现不明原因肠梗阻、胸水和腹水等。目前针对ROC的临床主要应用的治疗方案包括:二次细胞减灭术(secondary cytoreduction surgical, SCS);化疗,以铂类为基础的各种化疗组合;靶向治疗,应用聚腺苷二磷酸核糖多聚酶(PARP)抑制剂等,或免疫检查点抑制剂(immune checkpoint inhibitors, ICI)及抗血管生成药贝伐珠单抗等进行维持治疗。
对铂敏感ROC患者,推荐以铂类为基础的联合化疗作为标准化疗方案,包括卡铂或顺铂与紫杉醇、吉西他滨、聚乙二醇化脂质体多柔比星(PLD)加或不加贝伐珠单抗的组合,其中联合治疗已被证明比单一铂类药物具有更好的PFS和OS。而卡铂的普遍不良反应是血液学毒性表现,如贫血、中性粒细胞减少症和血小板减少症,多在化疗后第3天-第2周发生。据文献报道,Ⅲ-Ⅳ度白细胞减少和中性粒细胞减少的发生率为10-50%[2],而化疗后发生III级及以上中性粒细胞减少性发热(febrile neutropenia, FN)或持续时间>10d的中性粒细胞减少易导致肺炎败血症、侵袭性真菌感染或其他临床感染,严重影响患者预后及生活质量。
目前,临床针对化疗相关的中性粒细胞减少症常使用重组人粒细胞集落刺激因子(rhG-CSF)等短效药物,需严密监测血常规三系细胞计数,必要时多次注射。ROC化疗期间监测肿瘤标志物,需根据动态监测结果及影像学评估及时评估疗效,应用长效G-CSF预防中性粒细胞减少更有益于降低患者不良反应发生风险、预防继发性感染等。在这一类药物中,硫培非格司亭作为新一代长效G-CSF,通过其独特的硫醚基团连接体结构,展现了更高的稳定性和药效,成为目前唯一在化疗结束后24小时内可使用的长效G-CSF产品。本研究报道1例复发性卵巢癌患者使用硫培非格司亭预防TC方案+贝伐珠单抗化疗过程中性粒细胞减少症的发生,保证了医疗质量的前提下尽早使用,减少不必要的住院时间,以加快病床周转,减少恶性肿瘤患者的经济负担。现展示如下。
临床资料
一般资料
患者王**,女,60岁,因“卵巢癌术后2年余,下腹胀痛15天”入院。2年前(2021-08-10)因卵巢癌IIIC期于我科在全麻下行经腹全子宫+双附件+大网膜切除术。术后病理结果回报(B202134624):“双侧卵巢”高级别乳头状浆液性癌,侵及局部区卵巢表面。“双侧”输卵管组织;子宫肌萎缩性子宫内膜;子宫肌壁间平滑肌瘤(2个)伴玻变;宫颈慢性炎;大网膜纤维脂肪组织。术后BRCA基因胚系及体系均未检测到突变,HRD阴性。术后予以顺铂腹腔热灌注化疗+紫杉醇脂质体全身静脉化疗1次、紫杉醇脂质体+卡铂全身静脉化疗5周期。术后动态监测肿瘤标志物及影像学未见异常。15天前患者出现下腹胀痛,就诊外院提示CA125 443.4 U/mL HE4 309.3pmol/L,胸部CT:右肺上叶微结节,右肺下叶新发条索影,左侧胸腔积液形成,左侧膈肌抬高,左肺下叶稍膨胀不全。我院全腹+盆腔CT示:1.子宫及附件术后缺如,同前;术区可见条状致密影,盆腔右侧类圆形结节,其内可见液液平面,血肿?复发?建议MRI进一步检查。2.腹腔、盆腔积液;肠系膜增厚。综合考虑“复发性卵巢癌”,收住入院。
既往史: 36年前行右侧乳房脂肪瘤切除术(具体不详),否认肝炎、结核、疟疾病史,否认高血压、心脏病史,否认糖尿病、脑血管疾病、精神疾病史,否认外伤、输血史,药物过敏史:无,食物过敏史:无,其他过敏史:无,预防接种史不详。
个人史: 生于陕西,久居宝鸡,无疫区、疫情、疫水接触史,无牧区、矿山、高氟区、低碘区居住史,无化学性物质、放射性物质、有毒物质接触史。无吸毒史,无吸烟史,无饮酒史,无冶游史。月经婚育史:初潮13岁,(7)/(30)天,月经量中等,无血块、无痛经;23岁结婚,配偶健康;生产史1-0-2-1,34年前自然流产1次,33年前足月顺产一男活婴,25年前因计划外妊娠行人工流产1次,宫内节育器避孕。
家族史: 父健在,有心脏病史,母健在,有糖尿病、高血压、结肠癌病史,否认家族性遗传病史。
检查
查体:T36.2℃,P87次/分,R18次/分,Bp124/67mmHg,身高163cm,体重65.3kg。心肺腹查体未及明显异常。妇科检查:外阴:已婚经产式,阴毛呈女性分布。 阴道:通畅,粘膜萎缩,无异常分泌物,盲端可触及质硬结节。盆腔:空虚,无压痛,无反跳痛。
辅助检查:
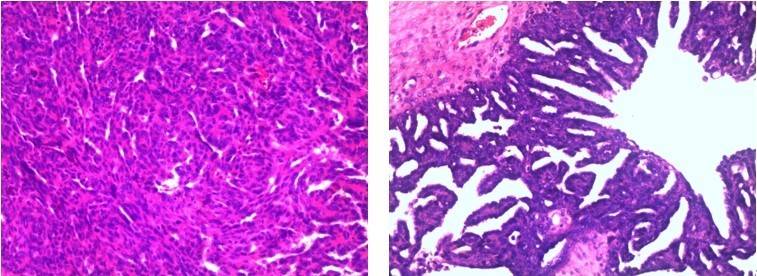
1.术后病理结果回报(B202134624):“双侧卵巢”高级别乳头状浆液性癌,侵及局部区卵巢表面。“双侧”输卵管组织,另送“?部位”小块高级别浆液性癌组织;子宫肌萎缩性子宫内膜;子宫肌壁间平滑肌瘤(2个)伴玻变;宫颈慢性炎;大网膜纤维脂肪组织(图1)。
2.术后肿瘤标志物监测情况
表1. 术后至本次入院期间肿瘤标志物变化

3.影像学检查:①胸部CT:右肺上叶微结节,右肺下叶新发条索影,左侧胸腔积液形成,左侧膈肌抬高,左肺下叶稍膨胀不全(图2)。②全腹+盆腔CT示:1.子宫及附件术后缺如,同前;术区可见条状致密影,盆腔右侧类圆形结节,其内可见液液平面,血肿?复发?建议MRI进一步检查。2.腹腔、盆腔积液;肠系膜增厚。③影像会诊:1.近日片新发左侧胸膜腔积液;双肺未见结节肿块。纵隔未见肿大淋巴结。右侧胸膜腔未见积液。2.肝脏、胰腺、脾脏实质内未见异常密度影。双肾上腺不大。双肾未见积水征象。3.2023-10-12新发腹盆腔积液,现片较前增多,盆腔积液分层。4.胃-脾-隔之间腹膜增厚,其内可见粟粒状结;5.子宫切除术后,阴道残端右后上方于2023-10-12新发结节,结节内可见液平,囊壁可见壁结节,囊液呈T1T2双高信号,该囊左前方可见数个微小弥散受限小结节。意见:上述表现提示肿瘤复发可能。
诊断
初步诊断:复发性卵巢癌
诊断依据:根据病史、体征、影像、肿标及病理可确诊。
治疗
于2023年12月15日、2024年1月5日、2024年1月26日予以连续三周期化疗,具体方案:紫杉醇脂质体270mg+卡铂650mg+贝伐珠单抗600mg,胸部增强CT[2024-2-16]:与2023-07-05比较:1.新增左侧胸腔积液;2.右肺上叶尖段肺大疱;两侧胸膜稍增厚;同前。第4次化疗前评估肿瘤标志物较前稍增高,新增左侧胸腔积液,故增加贝伐珠单抗至最大量,于2024年2月21日行紫杉醇脂质体270mg+卡铂650mg+贝伐珠单抗997.50mg全身静脉化疗。前3周期化疗后24h给予硫培非格司亭6mg,ih,后因个人原因第4周期化疗后未予以长效升白。目前患者正在严密随访中,动态监测肿瘤标志物以行下一周期化疗。
治疗结果、随访及转归
化疗后肿瘤标志物变化如表2。
表2. 复发后TC方案+贝伐珠单抗化疗期间肿瘤标志物

前3周期化疗后24h给予硫培非格司亭6mg,ih,分别记录血常规血细胞计数,提示白细胞计数及中性粒细胞计数均正常,因个人原因第4周期化疗后未予以长效升白,白细胞计数及中性粒细胞计数均明显减低(图3),4周期均未发生骨痛等不良反应症状。
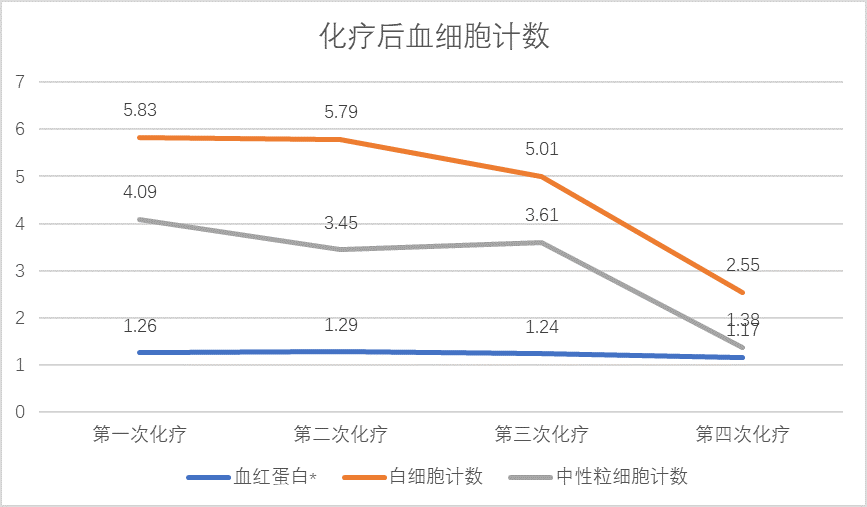
*为方便示数比较,将(血红蛋白计数/100)示于图中
血红蛋白计数单位:g/L;白细胞计数单位:× 109/L;中性粒细胞计数单位:× 109/L
讨论
卵巢癌是妇科常见的恶性肿瘤,病死率居妇科恶性肿瘤首位,严重威胁女性生命[3]。卵巢癌因早期无特异性临床症状,且筛查具有一定局限性,导致诊断极其困难,70%~75%的卵巢癌患者就诊时已为晚期,超过50%的患者在治疗后复发。术后患者接受辅助化疗过程中发生骨髓抑制中性粒细胞减少症的风险极高。对于复发性卵巢癌患者,最新的一项荟萃分析结果提示,与其他非铂单药相比,针对铂耐药ROC患者的化疗,反应率最高的药物还是铂类药物,提出了铂耐药ROC患者可能可以重新从铂类药物治疗中获得显著益处[4]。最新的 NCCN 指南针对铂耐药ROC化疗“可能有效方案”中亦新增推荐含铂化疗方案,这对铂耐药ROC患者的化疗方案提供了更多选择[5]。由此,对于那些具有复杂病因的疾病,如癌症,个体化治疗可以针对特定的分子标志物,提供更精确的治疗方案。对于铂敏感或铂耐药的ROC患者均可考虑化疗作为首选方案。而以铂为基础的联合化疗方案后会出现骨髓抑制,其中中性粒细胞减少症是骨髓抑制性化疗药物引起的最主要不良事件。中性粒细胞在先天免疫中起关键作用,也影响适应性免疫反应,先天性或诱发性中性粒细胞较少症患者会出现严重的,甚至是致命的感染。在这些患者中,感染风险与中性粒细胞减少程度成正比,且继发感染可能导致患者住院时间延长和病死率增加[6]。
重组人粒细胞集落刺激因子可分为短效rhG-CSF和长效PEG-rhG-CSF(聚乙二醇化重组人粒细胞集落刺激因子),是目前临床上常用且可有效降低中性粒细胞减少症发生风险的药物。集落刺激因子是内源性糖蛋白,可诱导骨髓造血祖细胞增殖并分化为特定的成熟血细胞类型。G‑CSF是一种谱系特异性集落刺激因子,由单核、成纤维和内皮细胞产生,其调节骨髓内中性粒细胞的产生并影响中性粒细胞祖细胞增殖、分化和细胞活化。PEG-rhG-CSF是使用基因重组技术生产的一种细胞因子,可有效预防肿瘤患者在放化疗过程中出现中性粒细胞减少。
大多数指南建议,如果在所有计划的化学治疗周期中FN的风险>20%,应预防性使用PEG-rhG-CSF[7]。PEG-rhG-CSF的作用机理是G-CSF与造血细胞的表面受体结合后,作用于粒系祖细胞,刺激粒细胞系统增殖、分化成熟和粒细胞功能的活化。与重组人粒细胞集落刺激因子(rhG-CSF)相比,PEG-rhG-CSF能够降低血浆清除率,延长半衰期并增加疗效[8]。同时也有研究证实,未经一级预防的患者,一旦发生FN,后续化疗过程中再次发生FN的风险为50~60%,因此,二级预防在这些患者中,显得尤为重要。二级预防使用G-CSF一方面可显著降低患者再次发生FN的风险,同时还可促进前1个周期化疗导致粒细胞下降的恢复过程,保障下个周期化疗的剂量以及按时进行。但目前关于硫培非格司亭预防复发性卵巢癌患者化疗后中性粒细胞减少的有效性和安全性数据较少。本研究报道了1例复发性卵巢癌患者行TC方案+贝伐珠单抗化疗期间应用硫培非格司亭预防中性粒细胞减少症,并表明硫培非格司亭可减少化疗后中性粒细胞减少症发生率,并且安全性良好。
利益冲突声明:所有作者均声明本研究不存在利益冲突。
[1]. Torre LA, Trabert B, DeSantis CE, et al. Ovarian cancer statistics, 2018. CA Cancer J Clin. 2018;68(4):284-296. doi:10.3322/caac.21456
[2]. Datta NR, Stutz E, Liu M, et al. Concurrent chemoradiotherapy vs. radiotherapy alone in locally advanced cervix cancer: A systematic review and meta-analysis[J]. Gynecol Oncol, 2017, 145 (2): 374-385
[3]. 王俐力,丁国范,杨丽杰等.不同剂型紫杉醇联合卡铂治疗晚期卵巢癌患者的临床疗效及对血清人附睾蛋白4、糖类抗原125和T淋巴细胞亚群水平的影响[J].癌症进展,2021,19(08):844-847+855.
[4]. Rumyantsev AA,Tyulyandina AA,Fedyanin MY,et al. Platinum vs non-platinum chemotherapy for platinum-resistant ovarian cancer: a systematic review and meta-analysis [J]. medRxiv,2022,7 ( 12) : 22277568
[5]. 卢淮武,徐冬冬,赵喜博等.《2024 NCCN卵巢癌包括输卵管癌及原发性腹膜癌临床实践指南(第1版)》解读[J].中国实用妇科与产科杂志,2024,40(02):187-197.DOI:10.19538/j.fk2024020113.
[6]. Al-Salama ZT, Keam SJ. Mecapegfilgrastim in Chemotherapy-Induced Neutropenia: A Profile of Its Use in China[J]. Clin Drug Investig, 2019, 39 (10): 1009-1018
[7]. Zardawi SJ, Nordman I, Zdenkowski N. A retrospective analysis of nadir-neutropenia directed pegylated granulocyte-colony stimulating factor on febrile neutropenia rates in (neo)adjuvant breast cancer chemotherapy regimens. Cancer Rep (Hoboken). 2020;3(5):e1266. doi:10.1002/cnr2.1266
[8]. 硫培非格司亭注射液说明书[EB /OL]. 2019-12-23 [2020- 03-12].https: / /redsenol.com/24237.html
排版编辑:肿瘤资讯-王俊澔











 苏公网安备32059002004080号
苏公网安备32059002004080号


