2025年美国临床肿瘤学会(ASCO)年会上,作为局部晚期胰腺癌全球第一个成功的三期临床研究,肿瘤电场治疗(Tumor Treating Fields,TTFields)联合化疗治疗局部晚期胰腺癌的PANOVA-3研究入选为LBA大会口头汇报,且全文同步在Journal of Clinical Oncology(JCO)杂志在线发表,并且由于将改变胰腺癌的治疗格局,被入选为今年的“Best of ASCO”,针对该研究结果,【肿瘤资讯】特邀北京大学肿瘤医院郝纯毅教授,基于临床和研究的双向视角,深度解读PANOVA-3研究的临床意义与启示。
北京大学肿瘤医院国际合作部主任,大外科常务副主任,北京大学肿瘤医院软组织和腹膜后肿瘤中心主任,肝胆胰外二病区主任
英国卡迪夫大学名誉教授
中国临床肿瘤学会“CSCO胰腺癌专家委员会”前任主任委员
中国医促会软组织肿瘤专家委员会主任委员
中国临床肿瘤学会“CSCO胃肠神经内分泌瘤专家委员会”副主任委员
中国肿瘤微创治疗技术创新战略联盟副主任委员
中华医学会外科学分会胰腺学组委员
中国医促会肝癌专家委员会秘书长
中国临床肿瘤学会常务理事
中国国际医学交流与促进会常务理事
享受国务院特殊津贴专家
胰腺癌治疗难度大、预后差,亟需治疗方案新探索
胰腺癌是我国常见的消化系统恶性肿瘤之一,恶性程度高、预后极差,外科手术被认为是潜在治愈胰腺癌的唯一有效方式。然而大多数的患者,确诊即为晚期,80%以上的患者确诊时已失去手术治疗的机会。局部晚期胰腺癌(LAPC)指的是一种局限于胰腺但已侵及周围的一些重要的血管,如肠系膜上动脉(SMA)、腹腔动脉(CA)等大的血管,单靠手术很难达到根治性的切除、不适合切除的局部的晚期肿瘤。这类患者通常预后很差,而且缺乏有效的、低毒的治疗方案。目前不可切除的LAPC药物治疗方面,主要以白蛋白紫杉醇联合吉西他滨(AG方案)等化疗方案为主,临床上也有吉西他滨联合替吉奥以及伊立替康脂质体为基础的方案等。总的来讲,离临床需求还相差很远,中位生存期通常不到1年,临床治疗中亟需更多的有效且安全性高的治疗方法与策略。
PANOVA-3 III研究取得突破性结果
肿瘤电场治疗(Tumor Treating Fields,TTFields)被称为肿瘤治疗的第四种疗法,它是一种无创的物理疗法,主要通过低强度中频交变电场来干扰肿瘤细胞有丝分裂,抑制肿瘤生长增殖并诱导肿瘤细胞凋亡等机制发挥抗肿瘤作用。目前TTFields已被美国食品药品监督管理局(FDA)批准上市用于治疗胶质母细胞瘤、恶性胸膜间皮瘤以及非小细胞肺癌,并于2020年成功在中国获批用于治疗胶质母细胞瘤。在 PANOVA Ⅱ期试验中,TTFields 联合吉西他滨 ± 白蛋白紫杉醇可显著延长局部晚期及转移性胰腺癌的无进展生存期(PFS)和总生存期(OS)。基于该研究的结果,电场疗法联合化疗已被《CSCO胰腺癌诊疗指南》列入局部晚期及转移性胰腺癌的治疗推荐。
为进一步验证TTFields在LAPC治疗中的疗效与安全性,开展了这项全球、开放标签、随机对照的Ⅲ期PANOVA-3研究,以评估TTFields联合吉西他滨和白蛋白紫杉醇一线治疗不可切除的LAPC的疗效和安全性。全球20 个国家的 196 个研究中心加入了该研究,共纳入 571 例新诊断的LAPC成年患者,其中中国大陆入组了64例患者(~11%)。
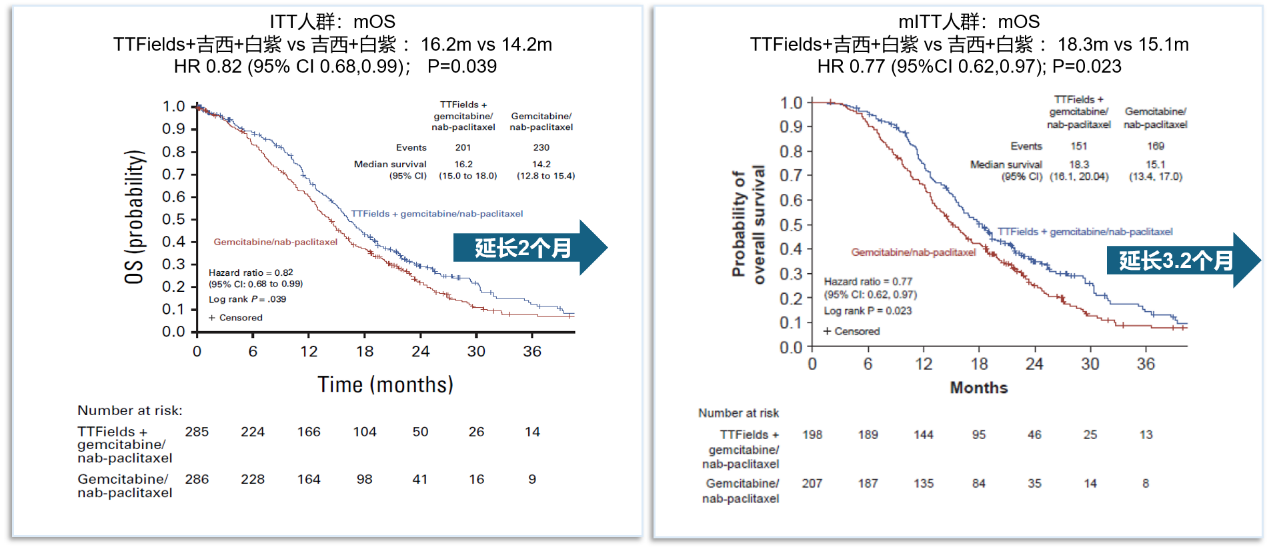
OS获益是胰腺癌治疗的最重要的目的,也是我们常说的在肿瘤治疗当中,OS才是金标准。PANOVA-3研究达到了OS主要终点。结果显示,与单用吉西他滨/白蛋白紫杉醇相比,TTFields 联合化疗组显著延长了 OS(中位 OS 为 16.2 个月 vs 14.2 个月,HR=0.82,P=0.039)。需要注意的是,两组有部分患者在28 天内停药(约30%),而修改后的 ITT(mITT)人群,即至少完成一个治疗周期(28天一个周期)的人群,TTFields 联合化疗组OS获益更为显著(18.3 vs 15.1 个月;HR=0.77)。另外,多项研究表明女性胰腺癌患者生存率优于男性,吉西他滨/白蛋白紫杉醇组的女性比例稍高(56.3%,高于TTFields 联合化疗组的女性比例48.4%),可能使对照组OS偏高。
TTFields联合化疗组在PFS、局部 PFS(从随机分组到局部疾病进展或死亡的时间) 和ORR方面也有获益趋势。两组PFS相近,TTFields联合化疗组中位PFS数值上延长1.3个月(10.6 个月 vs 9.3 个月),局部中位PFS数值上延长2.1个月(12.5个月 vs 10.4个月),客观缓解率(ORR)分别为36.1% vs 30.0%,TTFields 联合化疗组 ORR提高6%。事后分析显示,TTFields 联合化疗组在远处PFS (dPFS,从随机分组到远处疾病进展或死亡的时间) 方面具有显著的改善(13.9 个月 vs 11.5 个月,HR=0.74,P=0.022),说明TTFields联合化疗能够有效控制肿瘤生长并显著降低转移风险。TTFields在作用机制上可以有效干扰肿瘤细胞的运动和迁移,它通过在极性微管蛋白上施加定向力,使其沿电场方向排列,导致微管丰度变化,破坏了细胞的极性和迁移方向性,最终干扰肿瘤细胞的迁移能力。研究也显示,经TTFields干预的肾细胞癌家兔和黑色素瘤小鼠发生肺转移灶的数量明显少于对照组,最终获得生存期的延长,这与本研究中dPFS的改善一致。
同时,TTFields 联合化疗组在无痛生存期方面也显示出临床和统计学显著改善(中位 15.2 个月 vs 9.1 个月,HR=0.74,P=0.027)。无痛生存期定义为从随机分组开始至患者报告的疼痛视觉模拟评分(VAS)较基线增加≥20分或死亡的时间。疼痛是晚期胰腺癌患者常见且严重影响生活质量的症状,同时也是生存的预测因子。因此,TTFields 除了延长OS外,还可能有效控制临床症状的恶化,显著改善患者的生活质量,进一步支持其作为LAPC一线治疗的潜力。
该研究中观察到的生存获益是在每日设备使用率中位为62%(约15小时/天)的情况下实现的,低于研究方案中推荐的75%(≥18小时/天)。既往胶质母细胞瘤临床研究显示,TTFields日均使用时长与生存获益呈正相关,TTFields日均使用时间越长,OS获益越大。提示延长TTFields在LAPC中的持续使用时间,或可进一步提高临床获益。
安全性分析显示,化疗基础上联合TTFields未增加系统性毒性。绝大多数与设备相关的不良事件主要为轻中度的皮肤不良事件。
总体而言,PANOVA-3研究确立了 TTFields 联合吉西他滨/白蛋白紫杉醇的有效性,其能够为LAPC患者带来显著的生存获益,有望成为该类患者的新一线标准治疗选择。期待TTFields联合化疗方案早日在中国落地,惠及更多胰腺癌患者,也给医生带来新的治疗武器。
研究简介
肿瘤电场治疗(TTFields)是一种非侵入性治疗方式,利用低强度电场干扰癌细胞生存和肿瘤进展所需的关键细胞过程。在胰腺癌体内外模型中,TTFields显示出显著活性,并在联合化疗时疗效增强。在Ⅱ期PANOVA试验(ClinicalTrials.gov编号:NCT01971281)中,TTFields联合吉西他滨和白蛋白紫杉醇治疗晚期胰腺腺癌患者被证实是可行、安全且有效的。
在此报告关键性Ⅲ期PANOVA-3试验(ClinicalTrials.gov编号:NCT03377491)的结果,该研究评估了TTFields联合吉西他滨/白蛋白紫杉醇作为不可切除局部晚期胰腺癌一线治疗的疗效和安全性。
PANOVA-3 是一项全球性、随机、开放标签、多中心的 Ⅲ 期临床试验,纳入年龄在18岁及以上、经活检确诊为不可切除的局部晚期胰腺腺癌且未接受过治疗的成人患者,按 1∶1 随机分配接受吉西他滨 1000 mg/m² 和白蛋白紫杉醇 125 mg/m²(每 28 天周期的第 1、8、15 天)联合或不联合 TTFields。主要终点为总生存期(OS),次要终点包括无进展生存期(PFS)、局部无进展生存期(local PFS,从随机分组到局部疾病进展或死亡的时间)、1年生存率、无痛生存期[从随机分组到患者报告的视觉模拟量表(VAS)疼痛评分较基线增加 ≥20分或死亡的时间]和总体缓解率(ORR)、可切除率、安全性等。远处无进展生存期(dPFS,从随机分组到远处疾病进展或死亡的时间)为事后分析。
2018年5月至2023年3月期间,共有571例患者被随机分配至 TTFields 联合吉西他滨/白蛋白紫杉醇组(N=285)或吉西他滨/白蛋白紫杉醇组(N=286)(ITT人群)。两组患者的基线人口统计学和临床特征基本平衡。总体上,52.4% 的患者为女性,其中吉西他滨/白蛋白紫杉醇组的女性比例更高。两组均有~30%的患者在第1个治疗周期内出组,第一周期中患者中断治疗的原因见患者分布和试验流程图。完成一个完整治疗周期并纳入mITT 分析的患者人数分别为TTFields 联合化疗组198例,吉西他滨/白蛋白紫杉醇组207例。
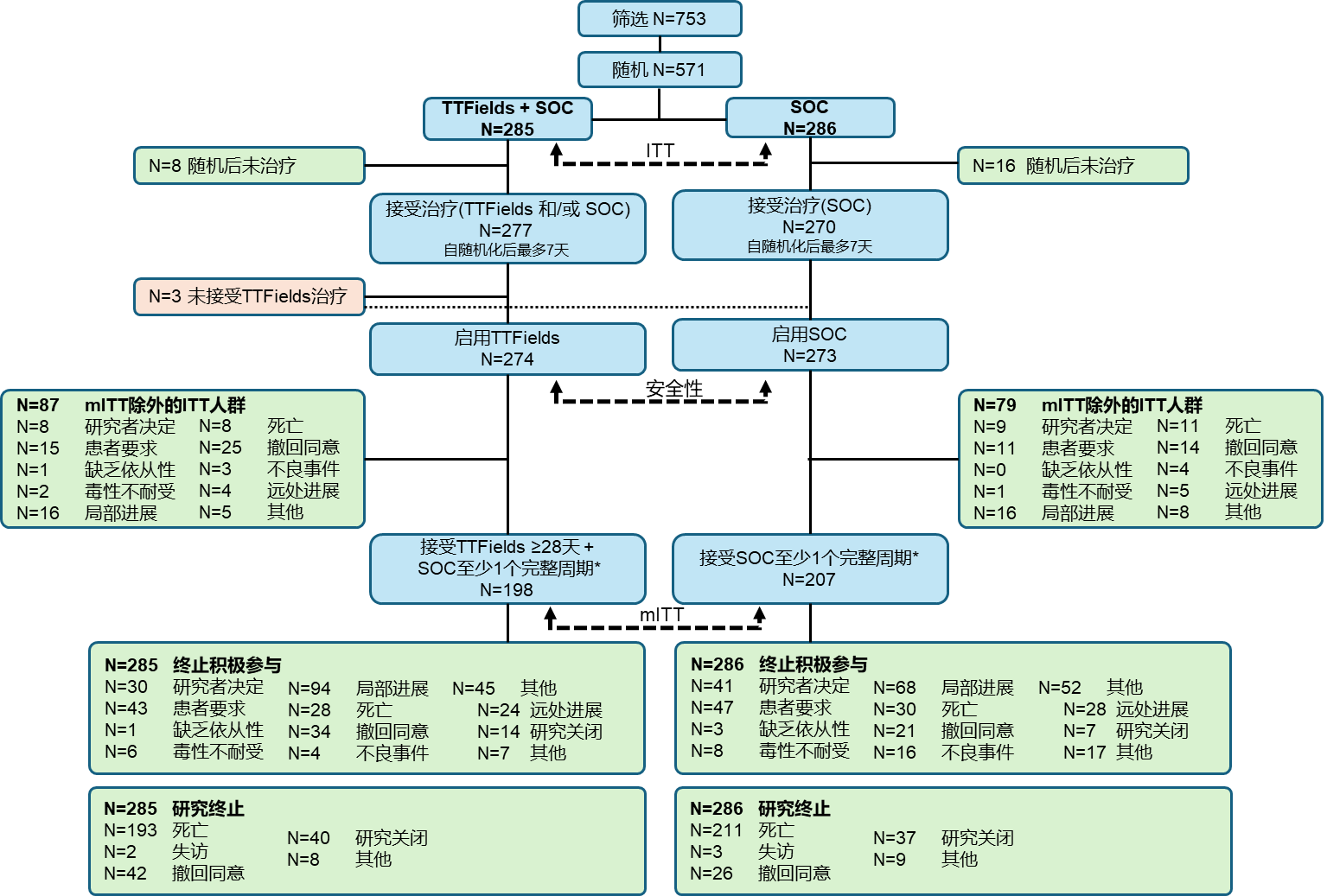
患者分布和试验流程图
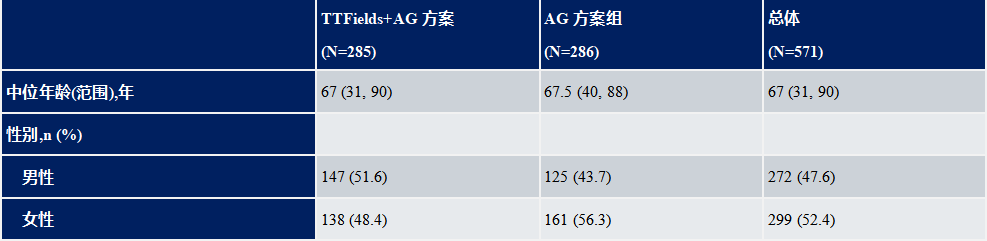
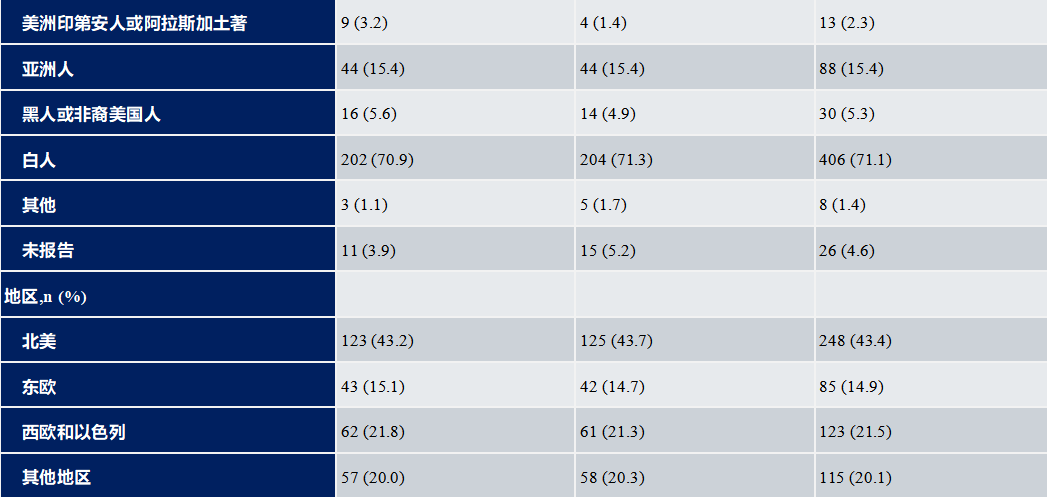
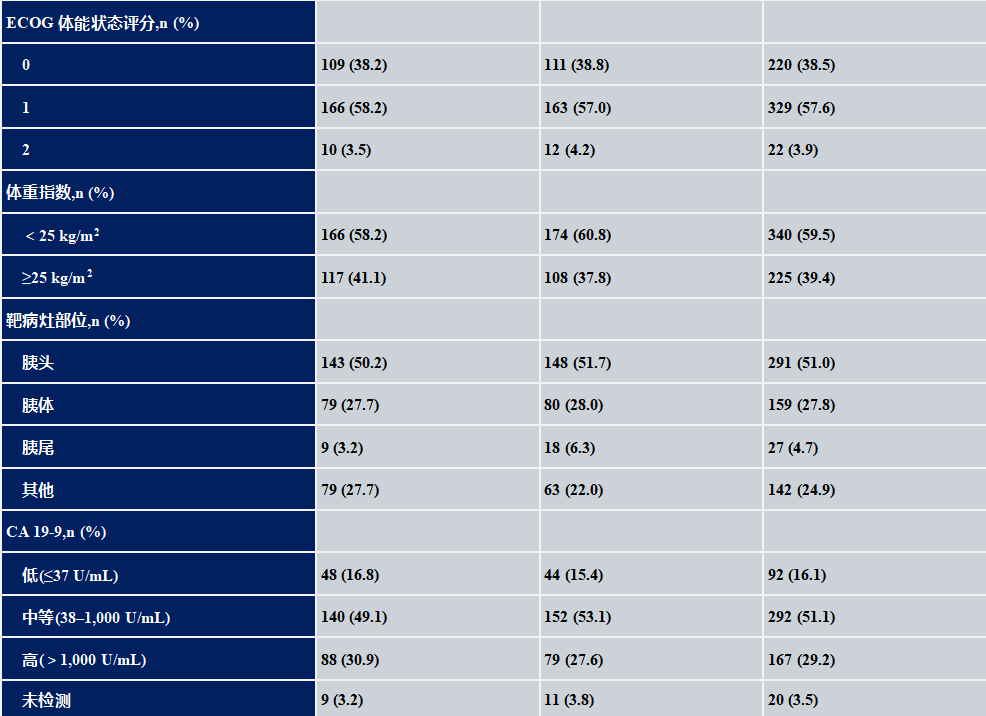
与单用吉西他滨/白蛋白紫杉醇相比,TTFields联合化疗组显著延长了 OS [中位 OS 为 16.2 个月(95% CI:15.0~18.0个月)vs 14.2 个月(95% CI:12.8~15.4个月),HR=0.82(95% CI:0.68~0.99),log-rank 检验 P=0.039]。1年OS率在 TTFields 联合化疗组也显著提高[68.1%(95% CI:62.0%~73.5%)vs 60.2%(95% CI:54.2%~65.7%),P=0.029]。在 mITT 人群中,中位 OS 也显著延长(18.3 个月 vs 15.1 个月;HR=0.77)。
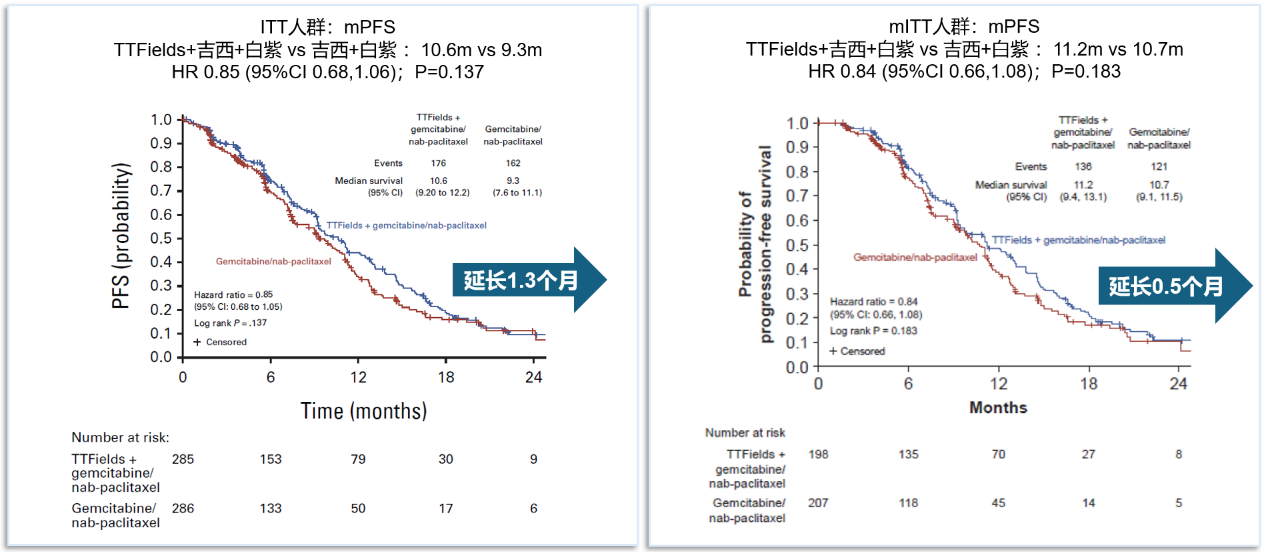
两组PFS相近[TTFields 联合化疗组中位 PFS为10.6 个月(95% CI:9.2~12.2个月),对照组为9.3 个月(95% CI:7.6~11.1个月);HR=0.85(95% CI:0.68~1.05),P=0.137]。但TTFields 联合化疗组的1年 PFS 率显著更高(43.9% vs 34.1%,P=0.026),mITT 人群中结果相似。
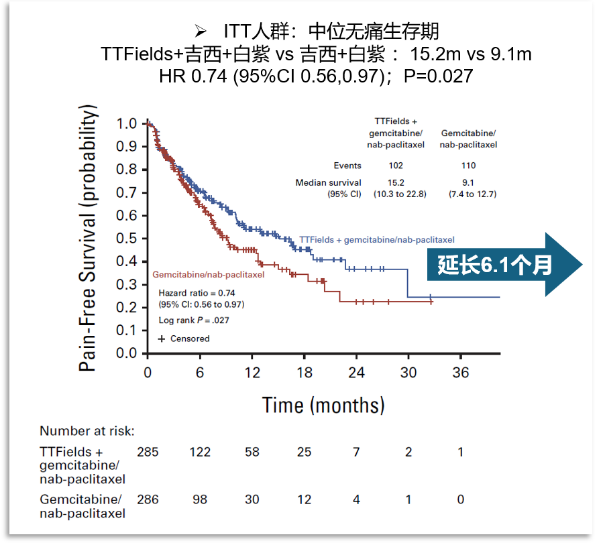
无痛生存期:TTFields 联合化疗组显著延长
无痛生存期在 TTFields 联合化疗组中显著延长[中位15.2个月(95% CI:10.3~22.8个月)vs 9.1 个月(95% CI:7.4~12.7个月);HR=0.74(95% CI:0.56~0.97),P=0.027]。
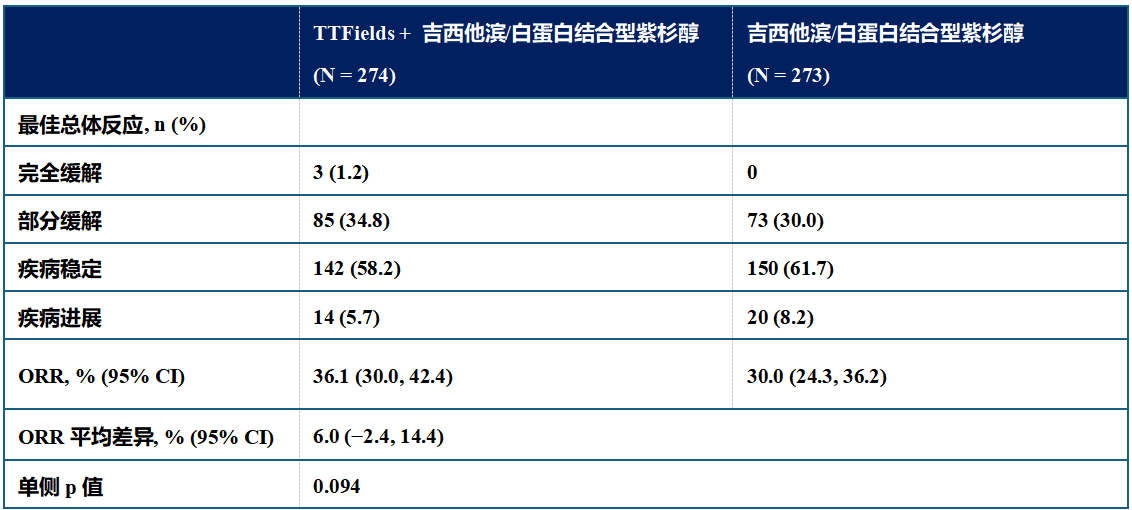
ORR 分别为 36.1%(95% CI:30.0%~42.4%)和 30.0%(95% CI:24.3%~36.2%),差异无统计学意义(P=0.094)
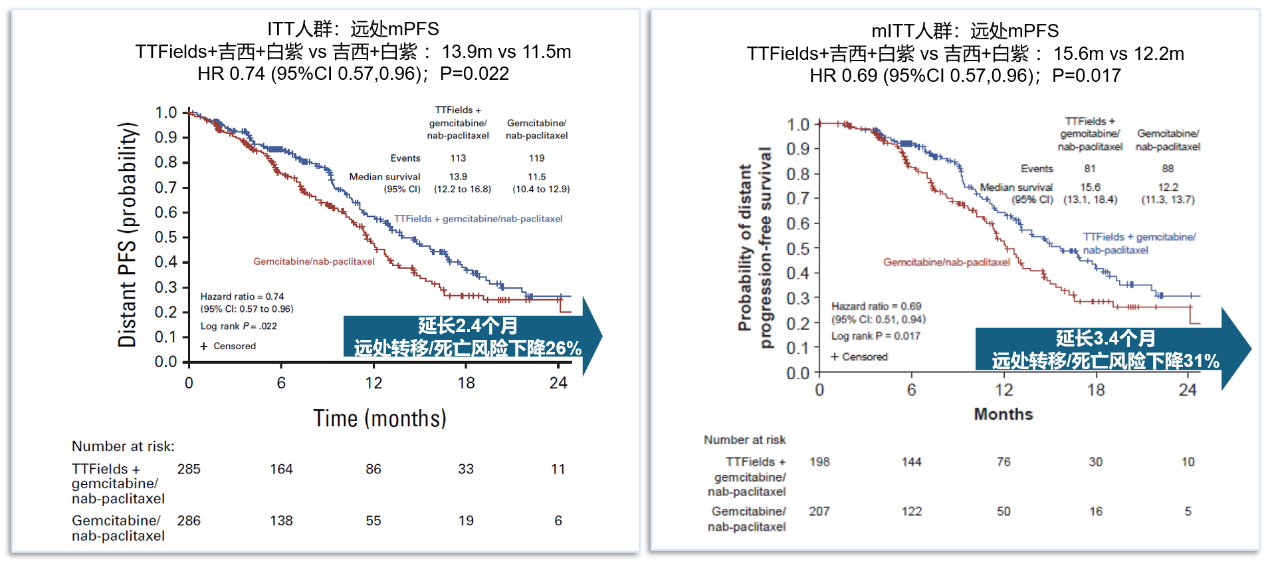
dPFS在 TTFields 联合化疗组中显著延长[中位13.9 个月(95% CI:12.2~16.8个月)vs 11.5 个月(95% CI:10.4~12.9个月);HR=0.74(95% CI:0.57~0.96),P=0.022],mITT 人群中结果相似。
• TTFields联合化疗组与传统化疗组≥3级不良事件(AE)发生率分别为88.7%和84.3%;最常见的≥3级AE是中性粒细胞减少(47.8% vs 47.6%)和贫血(21.9% vs 22.3%)
• 两组严重AE发生率相近且大多数严重AE与化疗或基础疾病相关。
•76.3%接受TTFields的患者出现设备相关皮肤不良事件,绝大多数为轻中度,7.7% 为≥3级。
PANOVA-3 是目前唯一的一项在不可切除局部晚期胰腺癌中显示显著OS获益的Ⅲ期临床试验,确立了TTFields联合吉西他滨/白蛋白紫杉醇的有效性。该疗法在OS、无痛生存期和dPFS方面具有临床意义的改善,且未增加系统性毒性,为局部晚期胰腺癌的管理提供了潜在的突破。PANOVA-3的结果也可能对其他实体瘤治疗具有启示意义,进一步支持TTFields与现有标准治疗联合应用于多种治疗场景的潜力。
相关文章回顾(点击可查看详情):
1.全球Ⅲ期PANOVA-3临床试验中国患者招募全面开启,胰腺癌电场治疗再燃新生机
2.LUNAR研究全文荣登The Lancet Oncology,TTFields联合治疗正成为晚期肺癌治疗新选择
3.【2023 ASCO抢先看】揭密最值得期待的创新肿瘤疗法——肿瘤电场治疗(TTFields)
排版编辑:肿瘤资讯-yu
版权声明
版权归肿瘤资讯所有。欢迎个人转发分享,其他任何媒体、网站如需转载或引用本网版权所有内容,须获得授权,且在醒目位置处注明“转自:良医汇-肿瘤医生APP”。











 苏公网安备32059002004080号
苏公网安备32059002004080号


