食管癌是全球范围内导致癌症相关死亡的第六大原因,尤其在亚洲,食管鳞状细胞癌(ESCC)占所有食管癌病例的约90%。由于疾病通常诊断时已为晚期,且预后较差,其死亡率较高[1]。对于不可切除的局晚期食管鳞癌患者,常规的治疗方案为放化疗,但其生存改善仍然有限。局晚期食管癌患者的3年总生存率通常在26.9%至55.4%之间,许多患者在初次治疗后仍会经历疾病进展[2, 3]。近年来免疫治疗在癌症治疗中取得了革命性的进展,并在晚期和转移性食管癌中显示了突破性的疗效,但免疫治疗在局晚期食管鳞癌的价值仍在探索阶段。目前,一些来自Ⅱ期临床试验的初步数据显示放化疗联合免疫治疗的应用获得了令人鼓舞的结果[3-5]。
患者基本情况及相关检查
患者女性,71岁。
主因无明显诱因出现反酸烧心、胸背部疼痛2个月于2023-08-28就诊。
患者曾于当地查上消化道造影(新乐市医院,2023-08-21):食管中下段占位性病变,建议胃镜进一步检查。
胃镜(新乐市医院,2023-08-18):距门齿28cm可见菜花型肿物生长,表面附带白色溃疡,活检3块。诊断:食管ca?。病理(2023-08-21):食管鳞状细胞癌。
胸部CT检查提示(我院 2023-09-03):食管胸段壁增厚,符合食管癌;纵膈多发淋巴结。
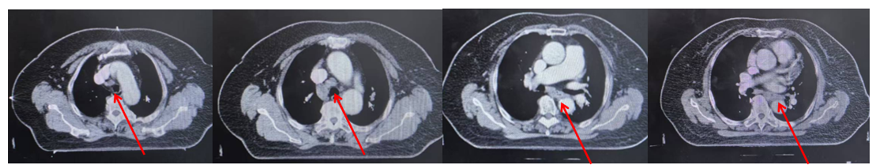
临床分期为:IIIB期(T3N1M0)。
血液ctDNA检测(2023-09-01):阳性。
既往高血压3级(极高危)、2型糖尿病、冠状动脉粥样硬化性心脏病病史。
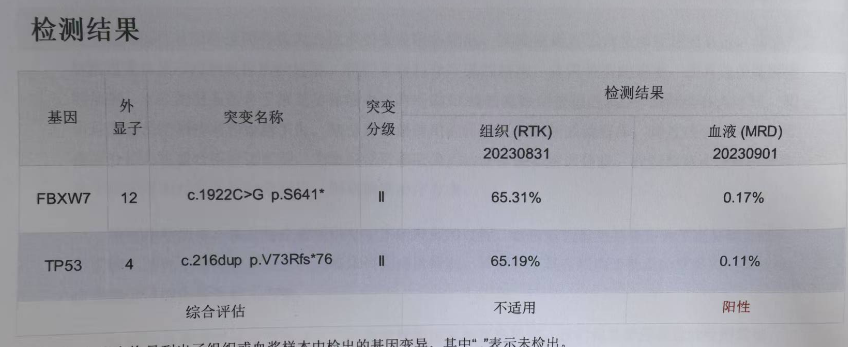
诊疗经过
考虑到患者高龄、一般情况较差及既往高血压、冠心病病史,不适宜手术治疗。排除治疗禁忌,在取得患者知情同意的基础上,自2023-09-01起,患者接受了替吉奥60mg/次,口服,2/日(d1-14)化疗,同时给予替雷利珠单抗200mg(d1)免疫治疗。
自2023-09-10起,患者开始接受食管病变及纵膈肿大淋巴结的放射治疗,放疗总剂量为60Gy/30f,2023-10-31结束放疗。在放疗期间,患者继续接受替吉奥化疗及替雷利珠单抗免疫治疗2个周期。
胸部CT检查提示(2023-10-31):食管胸段壁稍厚,纵膈多发小淋巴结,最大者短径约9mm。
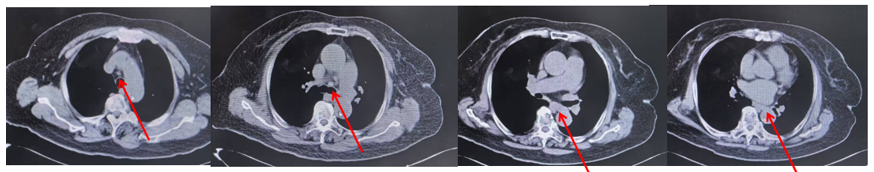
疗效评估为完全缓解(CR),且ctDNA检测(2023-10-31)结果为阴性。
患者于2023-11-04接受1周期替吉奥和替雷利珠单抗联合治疗,后进入替雷利珠单抗维持治疗阶段,免疫维持治疗结束时间为2024-11-10。维持治疗及复查期间,患者影像学检查未见肿瘤进展,ctDNA检测持续阴性。
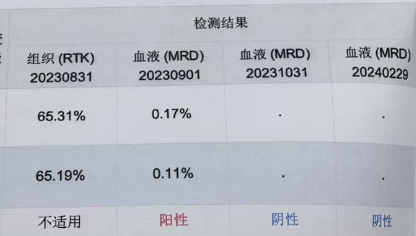
胸部CT检查提示(2024-12-31):
食管癌治疗后,食管胸段壁稍厚,纵膈多发小淋巴结,最大直径8mm。
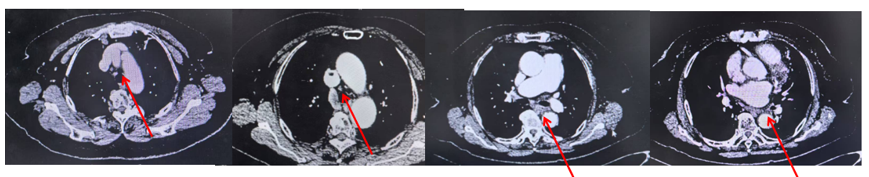
在根治性同步放化疗联合免疫治疗阶段,患者主要不良反应为Ⅱ级白细胞计数降低、Ⅱ级放射性食管炎。维持治疗阶段,患者未诉明显不适,化验指标无明显异常,生活质量良好。
本期特邀专家——沈文斌 教授
放疗三科主任、教授、主任医师、博导
山西长治医学院 客座教授
中国老年学和老年医学学会肿瘤康复分会食管癌委员会主委
中国生物医学工程学会精确放疗分会头颈肿瘤专委会常委
中国人体健康科技促进立体定向放射外科治疗专委会常委
中国老年学和老年医学学会肿瘤康复分会常委
国家癌症中心国家肿瘤质控中心鼻咽癌质控专家委员会委员
中国临床肿瘤学会食管癌专业委员会委员
中国抗癌协会鼻咽癌专业委员会委员
中国抗癌协会放射治疗专业委员会胃癌学组委员
中国抗癌协会放射肿瘤治疗学分会青年委员会委员
中国医师协会放射肿瘤治疗学分会青年委员会委员
中国抗癌协会食管癌专业委员会青年委员会委员
河北省肿瘤防治会肿瘤放射治疗专业委员会副主委
第一作者/通讯作者发表SCI 20余篇、中华系列论文60余篇
“河北省科技进步奖一等奖、二等奖、三等奖” 各1项
专家点评
同步放化疗是不可切除局晚期食管癌的标准治疗方案,但其疗效仍不理想,大多数患者在3年内会出现局部复发或远处转移。近年来,免疫检查点抑制剂在晚期食管癌中的应用取得了显著进展,如KEYNOTE-590和CheckMate 648等研究证实了免疫联合化疗的生存获益。那么,能否在局晚期食管癌患者的传统放化疗基础上加入免疫治疗,从而为其生存带来新突破?
本病例为一名71岁老年女性,合并高血压、糖尿病及冠心病等基础疾病,临床分期为T3N1M0(Ⅲ期)。通过多模态检查(胃镜、CT、ctDNA)明确诊断及分期,且应用ctDNA动态监测为疗效评估及复发预警提供了分子生物学依据。根据ECMRD-001研究设计,患者接受了根治性同步放化疗(食管局部根治性放疗+替吉奥化疗)联合替雷利珠单抗免疫治疗,并在后续辅以1年的替雷利珠单抗维持治疗。在传统根治性放化疗的基础上,联合免疫治疗可能通过激活全身抗肿瘤免疫,协同增效,进一步降低复发风险。同时,采用低毒的口服化疗药替吉奥替代传统的铂类为基础的双联化疗方案,以减轻治疗毒性,提高患者生活质量。治疗后,患者的临床影像学检查结果为CR,且ctDNA持续阴性,提示分子层面微小残留病灶已被清除。在治疗过程中,患者仅出现Ⅱ级白细胞减少和放射性食管炎,经过对症处理后症状得到缓解。
该病例提示,对于高龄且一般情况较差的患者,采用低毒的口服化疗药替代传统的铂类双联化疗药物,并联合替雷利珠单抗免疫治疗与食管局部放疗,可以在保证疗效的同时减轻毒性,确保患者的良好生活质量。
综上所述,本病例展示了根治性同步放化疗联合免疫治疗在局晚期食管鳞癌患者中的应用潜力。初步结果表明,联合治疗方案不仅确保了良好的疗效,还使患者具备较好的耐受性和生活质量。这为食管癌免疫治疗向早期阶段推进提供了新的可能性。
1. Thrift AP. Global burden and epidemiology of Barrett oesophagus and oesophageal cancer. Nat Rev Gastroenterol Hepatol. 2021;18(6):432-43.doi:10.1038/s41575-021-00419-3
2. Pennathur A, Gibson MK, Jobe BA, Luketich JD. Oesophageal carcinoma. Lancet. 2013;381(9864):400-12.doi:10.1016/s0140-6736(12)60643-6
3. Zhu Y, Wen J, Li Q, Chen B, Zhao L, Liu S, et al. Toripalimab combined with definitive chemoradiotherapy in locally advanced oesophageal squamous cell carcinoma (EC-CRT-001): a single-arm, phase 2 trial. Lancet Oncol. 2023;24(4):371-82.doi:10.1016/s1470-2045(23)00060-8
4. Wu L, Li B, Wan G, Wang Y, Zhu J, Liang L, et al. Toripalimab plus chemotherapy and radiotherapy for treatment-naive advanced esophageal squamous cell carcinoma: a single-arm phase 2 trial. Nat Commun. 2024;15(1):7116.doi:10.1038/s41467-024-51105-2
5.Zhang W, Yan C, Gao X, Li X, Cao F, Zhao G, et al. Safety and Feasibility of Radiotherapy Plus Camrelizumab for Locally Advanced Esophageal Squamous Cell Carcinoma. Oncologist. 2021;26(7):e1110-e24.doi:10.1002/onco.13797
排版编辑:肿瘤资讯-邓文普
下期预告
一例肿瘤负荷大的局晚不可切除的食管鳞癌患者经过化免诱导及同期放化疗模式治疗后肿瘤缩小,获得较长的生存
往期回顾:
【食管癌】有一种爱,是我陪你一起抗癌:一例晚期食管鳞癌患者多线免疫治疗病例分享
【食管癌】局部晚期不可手术切除食管鳞癌经放化疗联合替雷利珠单抗治疗后成功转化手术并获得长期生存病例
【食管癌】替雷利珠单抗联合同步放化疗为不可手术的局部晚期食管鳞癌老年患者带来新希望
【食管癌】局部晚期不可切除食管鳞癌患者接受替雷利珠单抗联合治疗,生存获益超过20个月
【食管癌】基于PRO评估后局部晚期食管鳞癌患者术前免疫联合短程放化疗新辅助治疗,OS超过21个月
【食管癌】一例颈段食管癌患者化免诱导后接受dCRT序贯免疫维持治疗,持续cCR长达17个月
【食管癌】局晚不可切除食管鳞癌患者经化疗联合免疫治疗获得手术机会并达到pCR
【食管癌】一例局晚可切除食管鳞癌患者经放化疗后联合免疫治疗达到cCR后保留食管并随访无复发











 苏公网安备32059002004080号
苏公网安备32059002004080号


