表皮生长因子受体(EGFR)突变阳性的晚期非小细胞肺癌(NSCLC)患者,EGFR酪氨酸激酶抑制剂(EGFR-TKI)靶向治疗是标准一线方案。然而临床实践表明,超过90%的患者在治疗12-24个月后会出现获得性耐药,导致疾病进展,这使得如何优化EGFR-TKI耐药的治疗选择成为临床亟待突破的关键问题。为进一步探索EGFR突变阳性晚期NSCLC患者的治疗策略,现分享一例EGFR-TKI耐药晚期肺腺癌患者接受艾托组合抗体治疗的成功案例。
本案例由山东第一医科大学第三附属医院肿瘤内科姜超教授分享,并邀请山东第一医科大学附属省立医院肿瘤中心化疗科王彩霞教授进行点评。现将病例及点评内容整理如下,供大家交流分享。
患者基本信息
一般资料:中年女性,既往体健,无烟酒嗜好
病史概述:
1. 2021年8月,体检发现"右肺占位"至当地医院就诊,基因检测显示EGFR 19Del,历经一代、三代EGFR-TKI治疗;
2. 2024年10月,入我院,右肺占位性病变;右肺胸膜多发实性结节,考虑转移;纵隔、右肺门及右心膈角区多发淋巴结;右侧胸腔积液,并右肺膨胀不全;双肺慢性炎性改变;肝左右叶交界区强化灶;
3. 右肺肿物穿刺活检病理:肺腺癌。
初步诊断:右肺腺癌(Ⅳ期)
分期:rcT4N3M1c,ⅣB期(第8版UICC/AJCC TNM分期)
诊疗历程
该患者整体诊疗历程时间轴如下图所示:
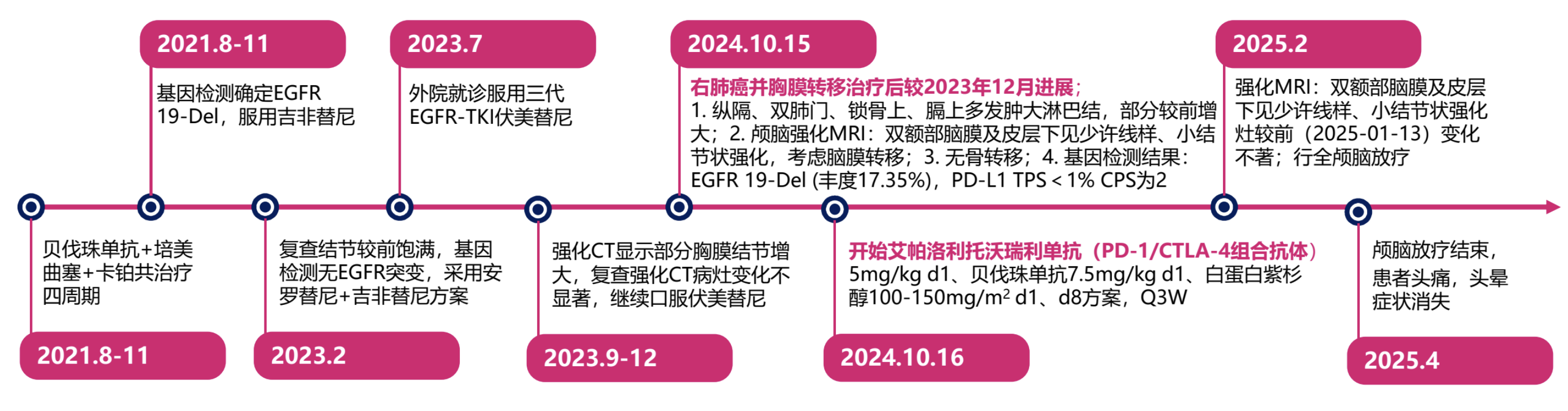
既往EGFR-TKI治疗:2021年8月-2023年12月
患者主诉因治疗意愿强烈,于2021年8-11月期间接受贝伐+化疗方案4个周期。后基因检测确认EGFR 19-Del突变,口服一代EGFR-TKI吉非替尼。影像学复查右肺胸膜结节增大伴胸腔积液增多,且血液检测未现EGFR突变,提示耐药。2023年7月于外院调整治疗方案,换用三代EGFR-TKI伏美替尼靶向治疗,复查提示胸膜结节潜在进展,12月影像示病灶稳定,遂维持治疗并随访。
艾托组合抗体联合方案治疗:2024年10月至今
患者于2024年10月采用艾帕洛利托沃瑞利单抗联合贝伐珠单抗、白蛋白结合型紫杉醇三药方案。2周期治疗后(2024年12月)复查显示治疗初显应答;4周期治疗后(2025年01月)强化CT显示病灶继续好转,患者体能状态显著改善,逐步恢复基本社会活动能力,生活质量明显提升;6周期治疗后(2025年4月)影像学评估显示疗效持续。
疗效评估
1. 2024年12月,2周期治疗后:强化CT显示病灶较前好转,淋巴结转移部分缩小,心包积液减少;颅脑强化MRI显示双额部脑膜及皮层下见少许线样、小结节状强化,右顶骨异常信号,较前变化不显著;
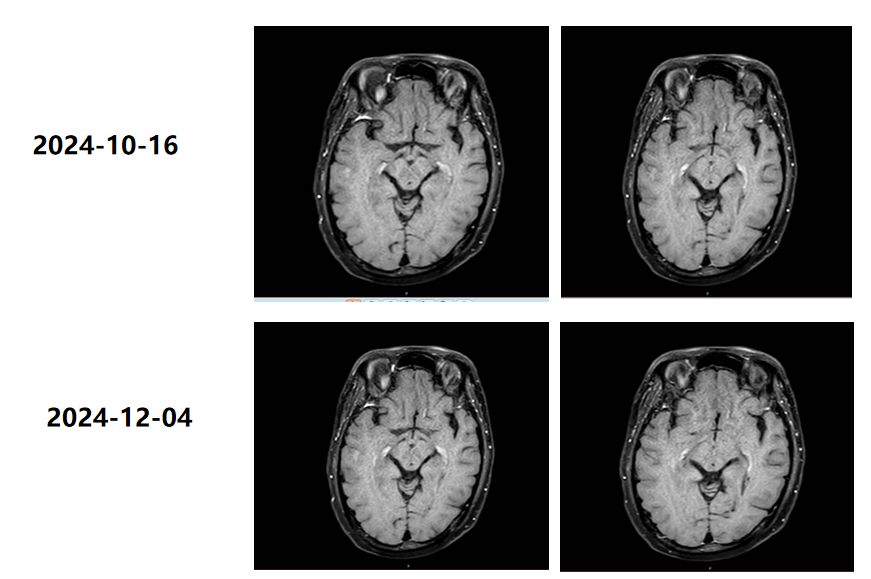
2. 2025年1月,4周期治疗后:强化CT显示病灶继续好转,纵隔、双肺门、锁骨上、膈上多发淋巴结转移部分较前(2024-12-03)略缩小。患者的体质较前明显好转,逐步恢复至正常生活状态;
3. 2025年4月,6周期治疗后,最新复查显示右肺癌并胸膜转移较前(2025-01-13)略好转,纵隔、双肺门、锁骨上、膈上多发淋巴结转移,部分较前略缩小。
专家点评
姜超教授点评
肿瘤学博士 副主任医师
2011年获山东省科技进步奖三等奖
2013年获山东省医学奖三等奖
中国临床肿瘤学会(CSCO)热疗专家委员会委员
世界中医药学会联合会肿瘤精准医学专委会理事
山东省老年学学会肿瘤多学科诊疗委员会常委
山东省药学会抗肿瘤药物专委会委员
山东省抗癌协会肿瘤心脏病分会委员
山东省疼痛研究会癌痛与姑息治疗委员会委员
艾托组合抗体联合方案:精准选择,强效突破
Q1:为何选择艾托组合抗体联合治疗方案?
本例患者为EGFR 19外显子缺失突变的晚期肺腺癌,经历了一代和三代EGFR-TKI治疗后出现耐药。考虑到该患者既往已使用过抗血管生成药物,包括贝伐珠单抗和安罗替尼,最近的基因检测显示“PD-L1 TPS<1% CPS 2”。在已有的研究数据中,PD-L1阴性患者选择PD-1单抗联合方案治疗,有效率和生存均未取得好的结果。
如果选择依沃西单抗(PD-1/VEGF双抗)方案,预估效果可能一般。通过对比EGFR-TKI耐药NSCLC各临床试验数据,我们发现艾托组合抗体+化疗+贝伐珠单抗方案在客观缓解率(ORR)、无进展生存期(PFS)、总生存期(OS)以及治疗相关不良反应(TRAE)方面均显示出亮眼数据。DUBHE-L-201研究队列5中,该方案在EGFR-TKI耐药人群中的中位PFS达8.5个月,中位OS达26.5个月,高于已获批上市的其他免疫治疗方案,实现了EGFR突变晚期NSCLC这类“冷肿瘤”疗效向驱动基因阴性晚期NSCLC免疫一线治疗水平的跨越。另外,贝伐珠单抗对脑转移瘤有一定疗效,考虑到患者体质差,且存在脑膜转移,联合贝伐珠单抗可能具有协同效应,为患者带来更多获益,同患者及家属协商后,最终选择了艾托组合抗体+化疗+贝伐珠单抗方案。
治疗结果证实了我们的选择是正确的。患者接受艾托组合抗体联合贝伐珠单抗和白蛋白紫杉醇治疗后,肿瘤病灶明显缩小,淋巴结转移灶部分缩小,胸腔积液减少,临床获益显著。
新型免疫联合策略:耐药困境革新方案,安全有效双重保障
Q2:艾托组合抗体治疗的临床疗效与安全性体会
在本例患者的治疗过程中,艾托组合抗体联合化疗和贝伐珠单抗对EGFR-TKI耐药PD-L1阴性的NSCLC患者显示出良好的疗效,患者在接受治疗后迅速获得临床缓解,影像学评估显示病灶明显缩小,这与DUBHE-L-201研究EGFR-TKI耐药队列中54.8%的客观缓解率相符。此外,艾托组合抗体与化疗和贝伐珠单抗联合使用时不良反应总体可控。在DUBHE-L-201研究EGFR-TKI耐药队列中,≥3级治疗相关不良反应发生率为35.5%,低于其他同类研究。我们的患者在治疗过程中也未出现严重的免疫相关不良反应。值得一提的是,本病例的实践经验显示,灵活应用全颅脑放疗可有效控制脑膜转移症状。
总之,本例患者的治疗过程充分体现了个体化治疗的重要性。在EGFR-TKI耐药后,艾托组合抗体联合化疗和抗血管生成治疗为患者带来了显著获益,而针对脑膜转移的放疗进一步改善了患者的生活质量。这一成功案例为EGFR-TKI耐药PD-L1阴性的NSCLC的治疗提供了宝贵的临床经验。
王彩霞教授点评
山东省医师协会肿瘤精准医疗医师分会主委
中国医师协会中国肿瘤MDT联盟山东省分盟牵头专家
中国抗癌协会CACA整合“药学+临床”全程管理专项特聘专家
中华医学会肿瘤学分会肿瘤支持康复治疗学组委员
国家卫生健康委 “肺癌规范化诊疗”项目专家顾问
山东省医院协会肿瘤多学科整合诊疗专委会主委
山东省老年学与老年医学学会生物靶向治疗专委会主委
中国老年学和老年医学学会第六、七届理事会理事
中国肿瘤中青年医师人才培养计划-肺癌工作委员会副主委
山东省药品不良反应监测中心、药物滥用监测中心外聘专家
山东省医学会咽喉肿瘤多学科联合委员会副主委
山东省医师协会肿瘤多学科综合治疗专委会副主委
山东省医师协会神经内分泌肿瘤专委会副主委
山东省医疗事故鉴定专家
山东省劳动能力鉴定专家
免疫协同,精准施治:探索EGFR-TKI耐药NSCLC治疗新策略
Q1:EGFR-TKI耐药NSCLC的免疫治疗策略在肺癌精准治疗领域中处于什么样的地位?未来有哪些发展趋势?
随着靶向治疗的广泛应用,EGFR-TKI耐药已成为临床面临的主要挑战。传统化疗方案在这类患者中的疗效有限,中位PFS仅为2.6-4.6个月。而免疫治疗,特别是免疫联合治疗策略是重要选择,如艾托组合抗体+化疗+贝伐珠单抗方案,已在多项研究中显示出更优的疗效,中位PFS可达8.5个月,为这类患者提供了新的治疗选择。EGFR-TKI耐药后的免疫治疗策略正逐渐成为肺癌精准治疗领域中不可或缺的重要组成部分,填补了EGFR-TKI耐药后NSCLC治疗的关键空白。
从治疗模式上看,现在的趋势是采用免疫联合治疗策略,包括双免疫检查点抑制剂(如PD-1/CTLA-4组合抗体)、免疫治疗联合抗血管生成药物、化疗药物或ADC药物等多种组合。这些联合策略通过协同作用,有效改善了治疗效果,也反映了肺癌治疗向精准化、个体化方向发展的趋势。未来,更精准的生物标志物研究,以及液体活检、多组学分析等技术,将帮助我们更准确地预测免疫治疗效果。新型免疫治疗药物的开发、免疫治疗的创新联合策略等将进一步提升治疗获益,而免疫治疗在新辅助或辅助治疗中的应用也将提高根治性治疗的效果。
值得注意的是,随着对EGFR-TKI耐药机制认识的深入,我们可能会发展出更有针对性的治疗策略。例如,对于不同耐药机制(如EGFR在靶耐药、旁路激活、表型转化等)的患者,可能需要不同的免疫治疗组合方案。这种基于耐药机制的精准治疗策略,将是未来研究的重要方向。
总之,EGFR-TKI耐药NSCLC的免疫治疗策略正在从边缘走向中心,成为肺癌精准治疗的重要支柱。未来,随着研究的深入和技术的进步,我们有望开发出更精准、更有效的免疫治疗策略,进一步延长EGFR突变阳性晚期NSCLC患者的生存期,提高生存质量。
聚焦全程管理:构建EGFR突变肺癌标准化诊疗体系
Q2 : 针对EGFR突变阳性肺癌患者的全程管理,如何构建更加完善的治疗路径,特别是考虑到可能出现的各种耐药机制和并发症?
构建EGFR突变阳性肺癌患者的全程管理治疗路径,需要系统性思考,从诊断、治疗到随访的各个环节进行优化。在诊断阶段,除了常规的EGFR突变检测外,应当在初诊时进行更全面的基因组学分析,包括NGS测序以检测可能的共突变(如本例中的BRAF V600E突变)、融合基因等,这些因素可能影响治疗效果和耐药机制。同时,应评估患者的基线状态,包括脑转移筛查、心肺功能评估等,为后续治疗决策提供依据。
对于一线治疗策略,目前三代EGFR-TKI如奥希替尼,已成为EGFR突变阳性肺癌的标准选择,但对于特定亚组患者,如伴有脑转移、共突变或特殊突变类型的患者,可能需要考虑个体化的治疗策略,包括TKI联合化疗、TKI联合抗血管生成药物等。在耐药问题上,应建立规范的随访监测体系,包括定期的影像学评估、液体活检监测等。对于出现寡进展的患者,可考虑继续原TKI治疗加局部治疗;对于广泛进展的患者,应及时进行再次活检或液体活检,明确耐药机制,针对不同的耐药机制,采取相应的治疗策略。
EGFR突变阳性肺癌患者在治疗过程中可能面临多种不良反应,包括TKI相关的皮疹、腹泻、间质性肺炎,免疫治疗相关的免疫相关不良反应,以及疾病进展相关的并发症如脑转移、骨转移等。应建立多学科协作的并发症管理团队,制定预防和处理策略,并进行患者教育,提高患者对并发症的认识和自我管理能力。同时整合疼痛控制、营养支持、心理支持等支持治疗措施。对于晚期患者,姑息治疗的早期介入可以提高生活质量,甚至延长生存期。
此外,EGFR突变阳性肺癌患者的全程管理需要肿瘤内科、胸外科、放疗科、影像科、病理科等多学科团队的紧密合作。应建立规范的多学科诊疗(MDT)机制,针对复杂病例进行集体讨论和决策,制定最佳的个体化治疗方案。
总之,EGFR突变阳性肺癌患者的全程管理是一个动态、复杂的过程,需要根据患者的具体情况、疾病进展和治疗反应不断调整治疗策略。通过构建完善的治疗路径,整合多学科资源,关注耐药机制和并发症管理,可以最大限度地延长患者生存期,提高生活质量,逐步实现将EGFR突变阳性肺癌转变为一种可长期控制的"慢性病"的目标。
排版编辑:肿瘤资讯-jyy











 苏公网安备32059002004080号
苏公网安备32059002004080号


