以下内容仅供中国大陆地区执业的医学药学专业人士阅读参考,如您非前述专业人士,请离开本页面
胃癌因其高度异质性,迫切需要精准的分子分型以指导有效的精准治疗。FGFR2b作为备受期待的一个新靶点,其过表达不仅与胃癌的不良预后紧密相关,也是指导个体化治疗的关键生物标志物。今年的欧洲肿瘤内科学会(ESMO)年会上公布了日本单中心的胃癌/胃食管交界处癌(GC/GEJC)患者中FGFR2b过表达的真实世界数据,及其和其他生物标志物的共表达情况。【肿瘤资讯】特邀复旦大学附属肿瘤医院盛伟琪教授,从病理学视角深入解读这些数据并探讨FGFR2b靶点的检测和应用前景。
复旦大学附属肿瘤医院病理科,主任医师,博士生导师
中华医学会病理学分会消化疾病学组副组长
中国抗癌协会肿瘤病理专业委员会胃肠肿瘤协作组(学组)组长
中国抗癌协会肿瘤病理专业委员会肝脏疾病协作组(学组)委员
中国抗癌协会胰腺癌专业委员会神经内分泌肿瘤学组委员
中国抗癌协会肿瘤药物临床研究专业委员会委员
中国临床肿瘤学会(CSCO)胃癌专家委员会常务委员
中国研究型医院学会病理学专业委员会委员
中国医师协会外科医师分会MDT专委会委员兼副秘书长
国家卫健委MDT专家委员会委员
上海市抗癌协会肿瘤病理专业委员会副主任委员兼秘书长
上海市医师协会病理科医师分会委员会秘书长
上海市抗癌协会大肠癌专业委员会委员
上海市抗癌协会淋巴瘤专业委员会委员等
研究背景
在胃癌中,已发现靶向治疗药物联合化疗可延长生存,包括针对人表皮生长因子受体2(HER2)、程序性细胞死亡蛋白(PD-1)以及紧密连接蛋白18亚型2(CLDN18.2)的药物[1-4]。尽管取得了这些进展,晚期胃或胃食管结合部(GC/GEJC)的预后仍然较差,需要进一步的治疗策略来改善结局。
FGFR在组织形成、血管生成和细胞增殖中至关重要,在一小部分胃癌中表现出基因扩增[5-8] 。此外,在GC/GEJC肿瘤组织中报告了FGFR2蛋白过表达,特别是成纤维细胞生长因子受体2亚型IIIb(FGFR2b)剪接变体,在随机Ⅱ期FIGHT研究中,报道其过表达发生率为20%~30%[9]。贝玛妥珠单抗(Bemarituzumab)是一种靶向FGFR2b的重组人源化IgG1单克隆抗体,在FIGHT研究中显示出前景:与安慰剂+化疗相比,贝玛妥珠单抗+化疗组的PFS(中位9.5个月 vs. 7.4个月; HR 0.72,95%CI,0.49~1.08)和OS(中位19.2个月 vs. 13.5个月;HR 0.77,0.52~1.14)显示出有临床意义的改善[9,10]。基于这些结果,正在进行的Ⅲ期试验(NCT05052801、NCT05111626)旨在进一步评估化疗联合贝玛妥珠单抗治疗晚期GC/GEJC的疗效[11,12]。
本研究试图提供晚期GC/GEJC中FGFR2b表达的临床和分子表征,及其与其他关注的生物标志物如HER2、PD-L1、MMR和CLDN18.2的共表达情况。
研究设计
从日本一家癌症中心的电子病历中收集了患者、治疗和肿瘤特征。纳入标准包括:
不可切除的局部晚期、转移性或复发性GC/GEJC;
组织学证实的腺癌;
在肿瘤组织采集之前未对晚期疾病进行全身化疗;
在研究开始前不超过5.5年开始对晚期疾病进行全身化疗;
具有可用于组织分析的存档组织标本;
签署二次研究的书面知情同意书。
通过IHC检测1L治疗前采集的FFPE样本中的FGFR2b(克隆FPR2-D)和PD-L1(克隆28-8)。FGFR2b过表达定义为任何百分比肿瘤细胞表现出中度(2+)至强(3+)膜染色(FGFR2b任何2+/3+)。基于FIGHT最终分析[10],还评估了FGFR2b过表达的预设替代定义,即有≥10%的肿瘤细胞表现出中度至强的膜染色(≥10% 2+/3+)。PD-L1分层[联合阳性评分(CPS)≥5分或CPS<5分]与贝玛妥珠单抗治疗晚期GC/GEJC患者注册研究中的分层一致,这有助于理解潜在的目标人群。HER2、MMR和CLDN18.2(克隆43-14A)按照既往报告进行评估[13,14],CLDN18.2阳性定义为≥75%的肿瘤细胞表达2+或3+染色强度。研究方案获得日本国家癌症中心研究伦理委员会的批准。
研究结果
根据FGFR2b状态分层的患者和肿瘤标本特征
鉴定并检测了547份肿瘤标本的FGFR2b和PD-L1,其中500份样本可评估FGFR2b。子队列包括128例在研究开始前不超过1.5年收集肿瘤标本的GC/GEJC患者。FGFR2b任何2+/3+的估计发生率为28.9%(37/128;95% CI:21.2%~37.6%),FGFR2b ≥10% 2+/3+的估计发生率为10.9%(14/128;95% CI:6.1%~17.7%)。FGFR2b任何2+/3+与FGFR2b 0/1+染色强度组之间的患者或肿瘤特征无差异,包括Borrmann 4型肿瘤的发生率分别为27.0% vs. 26.4%,或组织学弥漫型发生率为51.4% vs. 49.5%。
表1. 基于FGFR2b状态*分层的患者和肿瘤标本特征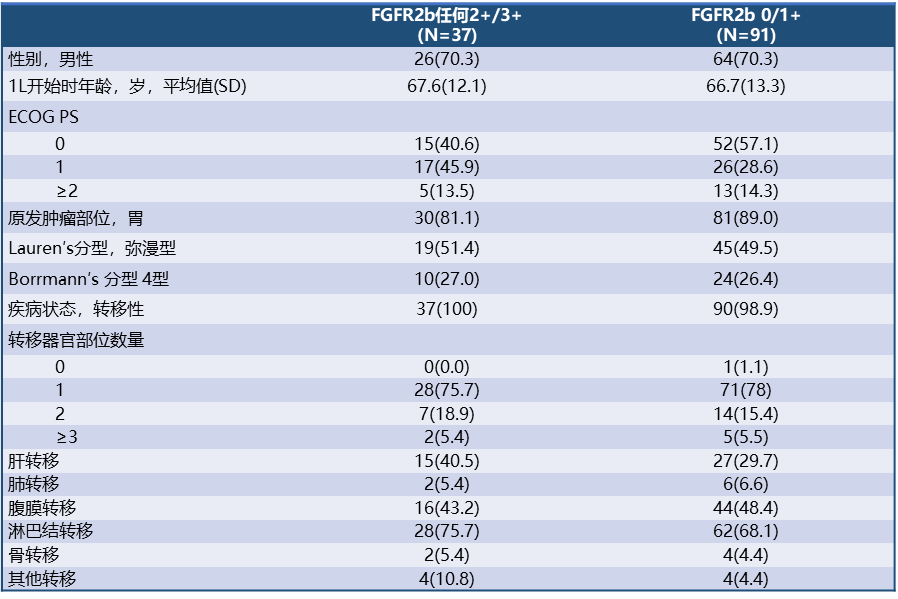
根据FGFR2b状态分层的关注生物标志物的分布和共表达情况
在关注的生物标志物中,FGFR2b任何2+/3+的估计发生率在HER2阳性患者中为16.6%(4/24),在dMMR患者中为0%(0/3),在PD-L1 CPS≥5的患者中为11.4%(5/44),在CLDN18.2阳性患者中为31.0%(13/42)。在FGFR2b任何2+/3+肿瘤样本中,13.5%(5/37)显示PD-L1 CPS≥5,35.1%(13/37)为CLDN18.2阳性。在具有任何FGFR2b 2+/3+表达的37例样本中,16例(44.4%)的关注的生物标志物呈阴性。
表2.根据FGFR2b状态分层的关注生物标志物的分布和共表达情况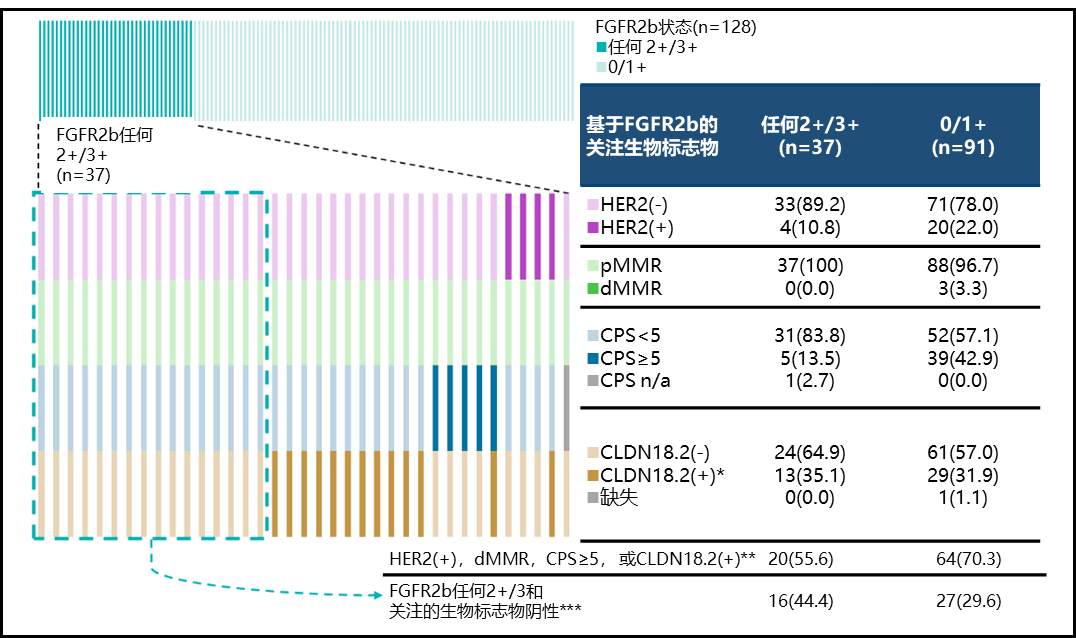
研究结论
FGFR2b是通过IHC检测的一种新型蛋白生物标志物,能够识别可能从当前正在进行的临床试验中接受FGFR2b靶向治疗(如贝玛妥珠单抗)获益的GC/GEJC患者人群。在128例患者的单中心分析中,约30%患者的肿瘤FGFR2b表达为任何2+/3+,其中约40%的患者不适合接受目前获批的靶向治疗。上述结果可能有助于解释正在进行的靶向FGFR2b治疗GC/GEJC的Ⅲ期试验,以及考虑未来针对FGFR2b的治疗策略。
专家点评
在晚期胃癌的治疗领域,精准医学的不断进步正在推动其治疗模式从传统的病理分型和临床分期,向基于分子分型和生物标志物的个体化治疗转变。目前针对HER2、MSI/MMR、PD-L1和CLDN18.2等分子标志物的治疗方案已经展现出良好的临床疗效[15]。此外,随着对胃癌分子生物学的深入理解,FGFR2b这一新兴靶点逐渐引人瞩目,有望为胃癌的精准治疗带来新的希望。
我们知道FGFR家族由四种受体组成,即FGFR1、FGFR2、FGFR3和FGFR4,它们在调节细胞生长、分化和迁移等关键生物学过程中发挥着至关重要的作用。FGFR2b,作为FGFR家族成员FGFR2基因的一个关键亚型,主要表达在上皮细胞中,在与FGF7、FGF10或FGF22配体结合时,会激活其细胞内的酪氨酸激酶结构域,触发一系列的下游信号通路。研究表明,FGFR2b的过表达与胃癌的侵袭性和预后不良密切相关。特别是在弥漫型、低分化和高T/N分期的胃癌中,FGFR2b的过表达更为常见,与患者的总生存期降低显著相关[5]。值得注意的是,FGFR2b蛋白的过表达并不总是与FGFR2基因的扩增同步发生,其他的生物学过程(如调控蛋白质合成与降解的信号通路紊乱)也能够造成FGFR2b蛋白的过表达。因此,不同于通过检测DNA层面的变异来确定基因扩增,采用IHC技术检测FGFR2b蛋白层面的过表达将是其标准检测方法。
在最近的ESMO大会上,研究者报道了日本GC/GEJC患者中通过IHC方法检测FGFR2b过表达的发生率为28.9%,而具有FGFR2b ≥10% 2+/3+的发生率为10.9%,与全球FIGHT研究中的比例(分别为29%和18%)相一致。这些数据不仅为胃癌的分子分型提供了新的视角,也为临床治疗策略的制定提供了重要的指导意义。
贝玛妥珠单抗,作为一种特异性靶向FGFR2b的人源化单克隆抗体,通过阻断FGFR2b与其配体的结合,并介导抗体依赖性细胞介导的细胞毒作用,有效抑制肿瘤细胞的信号传导,从而抑制肿瘤生长[16]。在FIGHT研究中,贝玛曲妥珠单抗联合化疗组相比安慰剂联合化疗组,显著改善了一线GC/GEJC患者的PFS和OS,特别是在 FGFR2b过表达的患者中,疗效更为显著[10]。目前美国FDA和中国CDE均授予其突破性疗法认定,也期待正在进行的两项全球多中心Ⅲ期试验(贝玛曲妥珠单抗联合化疗,贝玛曲妥珠单抗联合免疫和化疗)对于药物疗效的进一步证实[11,12]。
FGFR2b的过表达与其他生物标志物如HER2、PD-L1和CLDN18.2的共表达现象,为临床治疗方案的选择提供了新的思路,或许联合治疗是新的可能。因此,为了及时评估胃癌患者的预后并实现精准治疗,我们迫切期望在国内常规开展FGFR2b的检测,并深入探究其与其他生物标志物的共表达模式。这不仅有助于理解肿瘤的分子特性,还能为胃癌的个体化治疗提供策略指导,从而提升治疗效果。然而,精准筛选出FGFR2b高表达的患者,仍是FGFR2b靶向治疗在临床应用中面临的挑战。我们期待早日建立标准化的FGFR2b IHC检测流程和统一的判读标准,为精准治疗提供坚实的基础。
总体而言,FGFR2b的过表达不仅是胃癌不良预后的一个重要因素,也是指导个体化治疗的关键生物标志物。随着临床研究的不断深入,针对胃癌FGFR2b靶向治疗的应用前景将更加明确,有望为胃癌患者带来更为精准和有效的治疗选择。
1. Janjigian YY, et al. Lancet. 2021;398(10294):27-40.
2. Rha SY, et al. Lancet Oncol. 2023;24(11):1181-1195.
3. Shitara K, et al. Lancet. 2023;401(10389):1655-1668.
4. Shah MA, et al. Nat Med. 2023;29(8):2133-2141.
5. Ahn S, et al. Mod Pathol. 2016;29(9):1095-1103.
6. Han N, et al. Pathobiology. 2015;82(6):269-279.
7. Turner N, Grose R. Nat Rev Cancer. 2010;10(2):116-129.
8. Nagatsuma AK, et al. Gastric Cancer. 2015;18(2):227-238.
9. Wainberg ZA, et al. Lancet Oncol. 2022;23(11):1430-1440.
10. Wainberg ZA, et al. Gastric Cancer. 2024;27(3):558-570.
11. Smyth EC, et al. J Clin Oncol. 2022;40(16 suppl):TPS4164.
12. Wainberg ZA, et al. J Clin Oncol. 2022;40(16 suppl): TPS4165.
13. Kubota Y, et al. ESMO Open. 2023;8(1):100762.
14. Okazaki U, et al. ESMO Gastrointest Oncol. 2024;5(C):100086.
15. Guan WL, He Y, Xu RH. J Hematol Oncol. 2023 May 27;16(1):57.
Xiang H, et al. MAbs. 2021 Jan-Dec;13(1):1981202.
*仅供医疗卫生专业人士学术参考之用
*本文提及的药品和相关适应症尚未获得国家药品监督管理局的批准
排版编辑:肿瘤资讯-CYX











 苏公网安备32059002004080号
苏公网安备32059002004080号


