作为肿瘤治疗领域的国际盛会,2024年世界肺癌大会(WCLC)和2024年欧洲肿瘤内科学会(ESMO)已分别于美国圣地亚哥和西班牙巴塞罗那盛大召开。在今年WCLC和ESMO大会上,众多前沿研究的发布和更新,为广大肺癌患者的长期生存提供了新的希望。基于此,【肿瘤资讯】特邀四川大学华西医院王永生教授深入解读肺癌领域前沿进展,分享对肺癌治疗未来发展的见解。
华西医院肿瘤中心副主任兼临床研究部副部长
四川省卫生健康首席专家、卫健委学术带头人
中国抗癌协会中西医整合肿瘤专业委员会副主任委员
中国医药生物技术协会临床研究专委会副主任委员
中国药理学会药物临床试验专业委员会委员
中关村玖泰药物临床试验技术创新联盟细胞生物制剂临床试验专委会副主任委员
中国临床肿瘤学会(CSCO)免疫治疗专家委员会委员
四川省医师协会药物临床试验研究者分会会长
四川省抗癌协会老年肿瘤治疗专委会主任委员
四川省医促会肿瘤学MDT专委会主任委员
EGFR突变晚期NSCLC一线治疗:新药有望拓宽一线治疗新格局
本次WCLC大会上公布的多项研究为EGFR突变晚期NSCLC一线治疗的临床诊疗带来了突破性进展。Amivantamab是一种具有免疫细胞导向活性的EGFR/MET双特异性抗体,本次WCLC大会上的多项研究验证了Amivantamab联合Lazertinib或化疗在EGFR阳性晚期NSCLC患者中作为一线标准治疗的优越疗效。
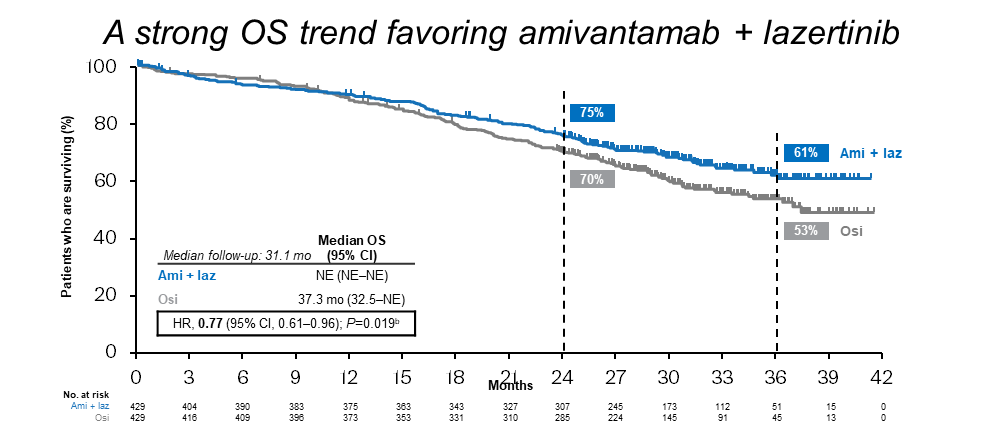
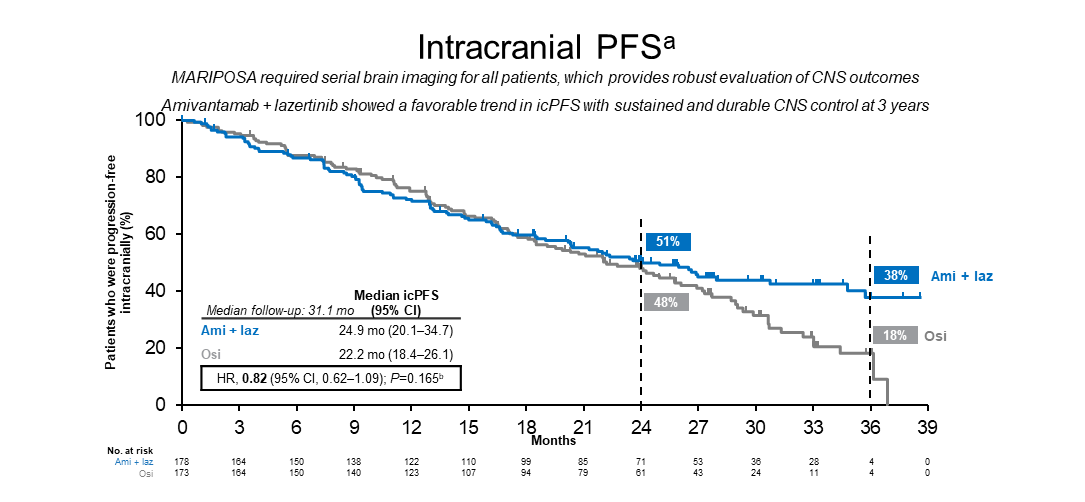
MARIPOSA是一项在EGFR突变型NSCLC患者中比较Amivantamab+Lazertinib(Ami+Laz)与奥希替尼单药(Osi)治疗一线治疗的III期研究。在2023 年ESMO年会就报道了它的早期研究结果[1],[Ami+Laz组与Osi组相比,中位无进展生存期(PFS)分别为23.7个月(95% CI, 19.1-27.7)vs 16.6个月(95% CI, 14.8-18.5),2年OS率分别为74% vs 69% (HR, 0.8; 95% CI,19.1-27.7)。 本次WCLC大会报道了该研究的进一步长期随访数据[2],结果显示Ami+Laz治疗与Osi治疗相比,观察到总生存期(OS)的进一步获益趋势(图1),中位OS NE vs 37.3个月 (HR, 0.77; 95% CI, 0.61-0.96; nominal P=0.019)。OS曲线早期分离并随着时间持续扩大,3年OS率提升近10% (61% vs 53%)。此外,Ami+Laz的联合治疗方案相较于Osi单药治疗,在控制中枢神经系统(CNS)的疾病进展方面展现了更持久的疗效(图2):3年颅内无进展生存期(PFS)率在Osi组中是18%,而Ami+Laz组为38%。基于良好的疗效,美国食品药品监督管理局(FDA)已批准Amivantamab+Lazertinib用于具有EGFR外显子19缺失或外显子21 L858R替代突变的局部晚期或转移性NSCLC患者的一线治疗[3]。目前,该方案已被《CSCO非小细胞肺癌诊疗指南2024》增加在“Ⅳ期EGFR敏感突变NSCLC一线治疗”的文字说明中[4]。近期公布的《NCCN非小细胞肺癌临床实践指南(2024 v9)》[5]也已将其列为针对此类患者推荐的一线治疗方案。
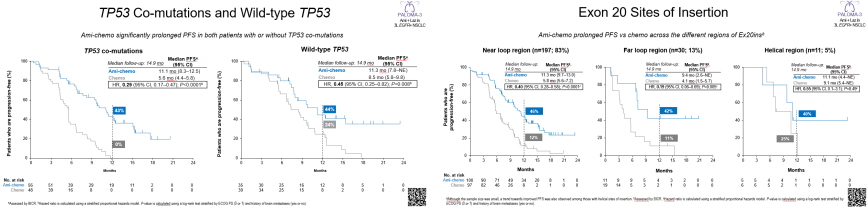
对于EGFREx20ins突变型NSCLC患者一线治疗,值得关注的研究是PAPILLON[6],今年WCLC大会上也有数据的更新。主要结果显示(图3),Amivantamab+卡铂+培美曲塞(ACP)方案较化疗在所有伴高危因素的患者中均体现了疗效优势:基线ctDNA阳性 (HR, 0.38; P<0.0001),治疗6周后ctDNA阳性 (HR, 0.55; P=0.098),TP53共突变 (HR, 0.29; P<0.001)。同时我们观察到:ACP方案在携带Ex20ins不同插入位置的患者中PFS获益一致。此研究也为ACP方案一线治疗Ex20ins晚期NSCLC奠定了基础。今年3月1日,FDA批准ACP方案用于EGFR ex20ins突变阳性局部晚期或转移性NSCLC患者的一线治疗,成为该领域首个获批的一线靶向疗法[7]。基于PAPILLON研究的数据《NCCN非小细胞肺癌临床实践指南(2024 v9)》将其列为针对此类患者优选推荐的一线治疗方案[8]。《CSCO 非小细胞肺癌诊疗指南2024》中仍将其列为Ⅲ级推荐方案[4]。
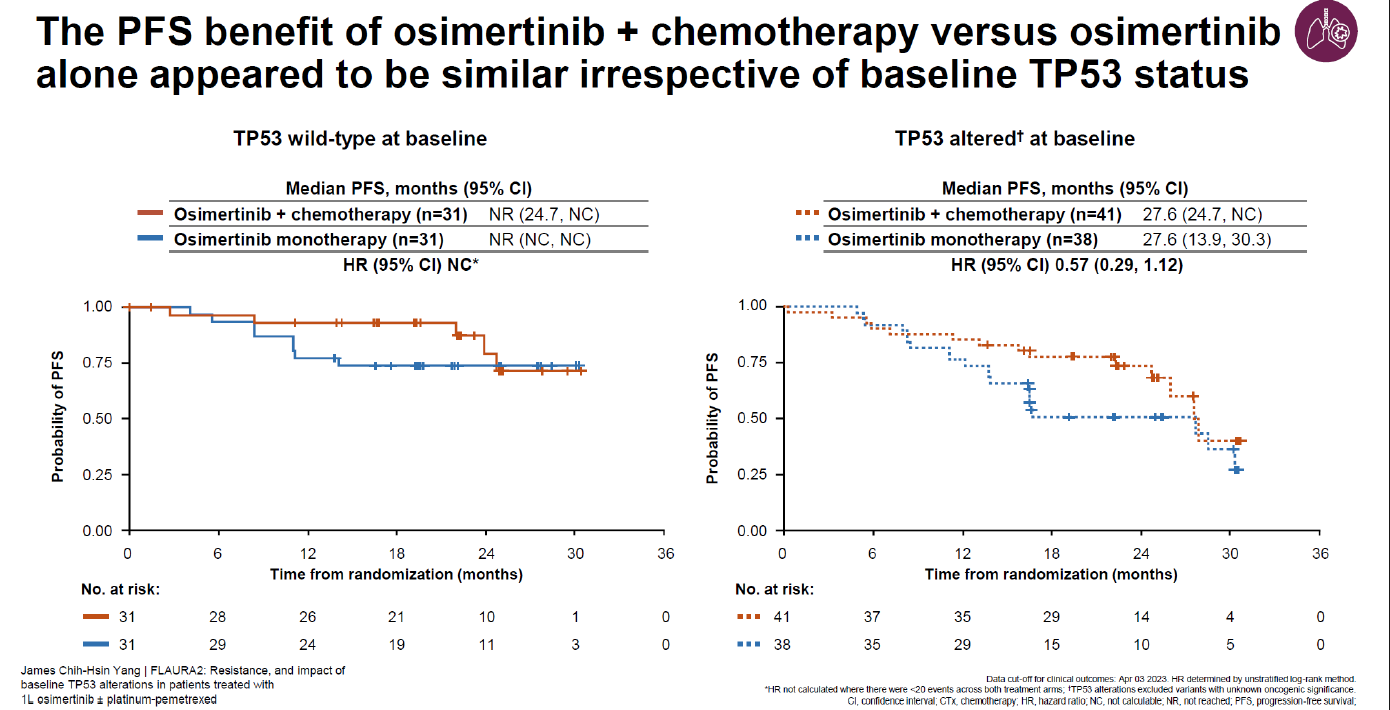
今年WCLC还更新了FLAURA2研究[9]耐药分析及基线TP53状态对结果影响的相关的数据,结果显示,无论基线 TP53 是否改变,奥希替尼联合化疗与奥希替尼单药治疗的 PFS 获益似乎相似,在TP53发生突变的人群中,采用化疗联合奥希替尼与奥希替尼单药组取得了数值上相同的mPFS 27.6个月(图4)。联合化疗或者不联合化疗,耐药机制总体类似,未发现新的耐药机制。
攻坚EGFR突变晚期NSCLC后线治疗耐药性难题:新药探索为患者带来希望
EGFR-TKIs耐药后的EGFR突变晚期非NSCLC患者的后续治疗已成为目前的热点和难点。耐药机制其实可以简单分为两大类,第一个是对驱动基因本身的一个耐药,另一方面是旁路激活的耐药,当然还有一些病理类型转化方面的一些耐药,但是更多的是刚刚提到的这两个方向的耐药机制。在此次2024 WCLC年会和ESMO年会报道的数据中,也有多项研究具有令人鼓舞的结果,这也将为处在耐药困境中的患者提供新的希望。
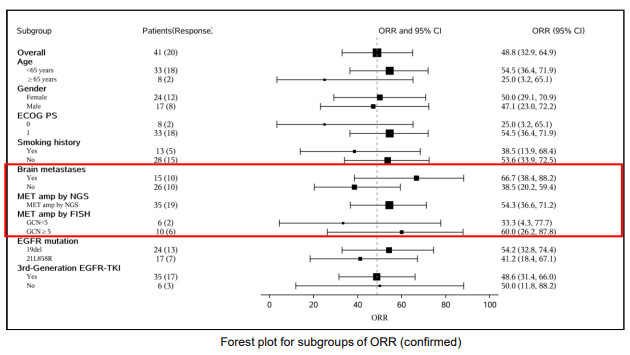
对于旁路激活耐药这一机制,一般会根据具体的耐药机制来选择相应的治疗策略,比如说MET扩增,我们会采用MET抑制剂,比如Her2扩增,或者是BRAF突变,也会根据相应的机制做联合治疗。今年WCLC更新的NCT06343064[10]是MET抑制剂伯瑞替尼联合尚未在国内市场上市的第三代EGFR-TKI PLB1004进行的临床研究结果。该研究同样显示(图5),在既往接受第三代EGFR-TKI治疗的患者中,如果患者存在MET基因扩增,采用MET抑制剂联合第三代EGFR-TKI的治疗方案,整体患者的ORR为48.8%,亚组分析显示,在脑转移患者中ORR为66.7%,经NGS检测伴MET扩增患者的ORR为54.3%。这些研究结果,再次强调了在EGFR突变的NSCLC患者中,EGFR突变和MET基因扩增都是重要的治疗靶点,双重抑制策略可能实现非常理想的抗肿瘤治疗效果。
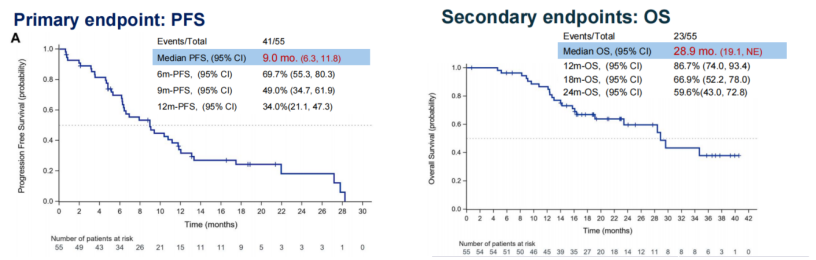
免疫检查点抑制剂(ICIs)治疗对于EGFR-TKIs耐药后的EGFR突变晚期非NSCLC患者来说是一个重要的选择,然而众多研究却显示疗效不够理想。ChiCTR1900026273[11]是探索EGFR-TKI治疗失败后的患者接受PD-L1单克隆抗体贝莫苏单抗联合安罗替尼的治疗。研究结果显示(图6),客观缓解率只有25.5%(95% CI 14.7, 39.0),但疾病控制率达87.3%(95% CI 75.5, 94.7),mPFS为9.0个月(95% CI 6.3, 11.8),mOS为28.9个月(95% CI 19.1, NE),24个月总生存率为59.6%。从这个研究当中我们也看到了免疫治疗在EGFR突变这部分患者的EGFR-TKI耐药之后的应用的潜力,当然这个研究相信未来还有优化的空间,研究结果也将支持免疫治疗在该领域的进一步发展。
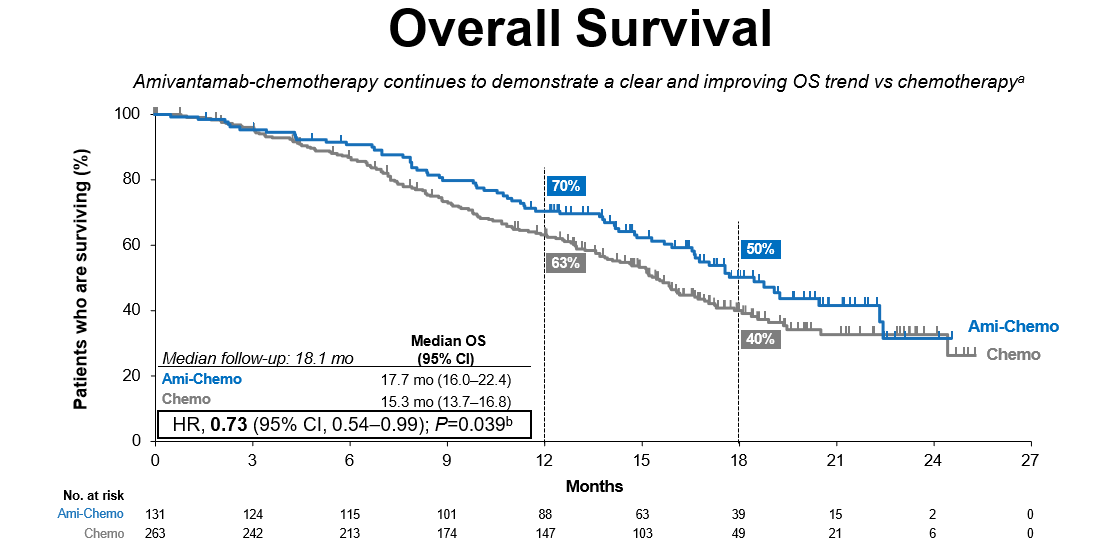
MARIPOSA-2(NCT04988295)是一项随机、开放标签的III期临床试验,评估了Amivantamab联合化疗(卡铂和培美曲塞)用于奥希替尼治疗后疾病进展的局部晚期或转移性NSCLC患者中的有效性和安全性。该项研究已有多项成果公布[12],结果显示,与化疗组相比,Ami+化疗具有显著更长的PFS结果, 中位PFS分别为6.3个月和4.2个月(HR 0.48; P<0.001); Ami +化疗的ORR明显高于化疗组,分别为63% 和 36%;。此次ESMO年会研究者公布了此项研究的进一步延长随访的OS结果[13],中位随访18.1月时,OS获益趋势进一步扩大,中位OS分别为17.7月(16.0–22.4)和15.3月(13.7–16.8),HR, 0.73 (95% CI, 0.54–0.99); P=0.039,18月OS率分别为50%和40%,随访还在继续,期待最终OS结果的发布,这将进一步完善MARIPOSA-2的临床数据,为临床诊疗提供更多的可能性。
总结
国际癌症研究领域的两大学术会议WCLC大会和ESMO年会,以其高质量的科研成果和深入系统的学术探讨,赢得了癌症研究领域专家们的广泛赞誉。今年这两大会议也继续延续了这一传统,特别是在NSCLC这一领域,会议报告涵盖了从早期诊断、个性化治疗策略到创新药物等多个方面的突破性进展。相信这些成果的公布,将不仅为临床医生提供了更多的治疗选择,也将为患者带来了更多的生存希望。
1. Byoung Chul Cho, Amivantamab plus lazertinib vs osimertinib as first-line treatment in patients with EGFR-mutated, advanced non-small cell lung cancer (NSCLC): Primary results from MARIPOSA, a phase III, global, randomized, controlled trial. 2023 ESMO, LBA14.
2. Shirish Gadgeel,Amivantamab Plus Lazertinib vs Osimertinib in First-line EGFR-mutant Advanced NSCLC: Longer Follow-up of the MARIPOSA Study.2024 WCLC,OA02.03.
3. FDA approves lazertinib with amivantamab-vmjw for non-small lung cancer. FDA. August 19, 2024, Accessed August 20, 2024. https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-lazertinib-amivantamab-vmjw-non-small-lung-cancer
4. IⅤ期驱动基因阳性非小细胞肺癌的治疗,中国临床肿瘤学会(CSCO)非小细胞肺癌诊疗指南2024, Accessed April, 2024.
5. Updates in Version 6.2024 of the NCCN Guidelines for Non-Small Cell Lung Cancer from Version 5.2024, NCCN Guidelines Version 9.2024- Non-Small Cell Lung Cancer.
6.Jonathan Goldman,PAPILLON:TP53 Co-mutations, Sites of Insertion, and ctDNA Clearance Among Patients with EGFR Ex20ins-Mutated Advanced NSCLC.2024 WCLC,MA12.06.
7. FDA approves amivantamab-vmjw for EGFR exon 20 insertion-mutated non-small cell lung cancer indications. March 1, 2024, Accessed March 1, 2024. https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-amivantamab-vmjw-egfr-exon-20-insertion-mutated-non-small-cell-lung-cancer-indications.
8.Updates in Version 1.2024 of the NCCN Guidelines for Non-Small Cell Lung Cancer from Version 5.2023,NCCN Guidelines Version 9.2024- Non-Small Cell Lung Cancer.
9.James CH Yang,FLAURA2: Resistance, and Impact of Baseline TP53 Alterations in Patients Treated With 1L Osimertinib ± Platinum-Pemetrexed.2024 WCLC,MA12.03.
10.周彩存、周斐、李玮,Vebreltinib Plus PLB1004 In EGFR-Mutated, NSCLC with MET Amplification or MET Overexpression Following EGFR-TKI.2024 WCLC,MA12.11.
11.史美祺,Benmelstobart, a PD-L1 Mab, Plus Anlotinib in EGFR+ Advanced NSCLC Patients Failed to Prior EGFR TKI Therapies:Phase II Results Update.2024 WCLC, MA11.11.
12.Passaro A, Wang J, Wang Y, Lee SH, Melosky B, Shih JY, Wang J, Azuma K, Juan-Vidal O, Cobo M, Felip E, Girard N, Cortot AB, Califano R, Cappuzzo F, Owen S, Popat S, Tan JL, Salinas J, Tomasini P, Gentzler RD, William WN Jr, Reckamp KL, Takahashi T, Ganguly S, Kowalski DM, Bearz A, MacKean M, Barala P, Bourla AB, Girvin A, Greger J, Millington D, Withelder M, Xie J, Sun T, Shah S, Diorio B, Knoblauch RE, Bauml JM, Campelo RG, Cho BC; MARIPOSA-2 Investigators. Amivantamab plus chemotherapy with and without lazertinib in EGFR-mutant advanced NSCLC after disease progression on osimertinib: primary results from the phase III MARIPOSA-2 study. Ann Oncol. 2024 Jan;35(1):77-90. doi: 10.1016/j.annonc.2023.10.117. Epub 2023 Oct 23. PMID: 37879444.
13. Sanjay Popat, Amivantamab Plus Chemotherapy vs Chemotherapy in EGFR-mutated, Advanced Non-small Cell Lung Cancer After Disease Progression on Osimertinib: 2nd Interim Overall Survival From MARIPOSA-2. 2024 ESMO, LBA54.
CRC Code: EM-166028
Approved Date: 2024/9/18
排版编辑:肿瘤资讯-Zika
✅ “本资料仅用于医学、科学交流,可能涉及尚未在中国获批的产品和适应症。强生创新制药不支持、不鼓励任何未被批准的药品/适应症使用。”
✅ “本资料中涉及的AE/SS/PQC已按照公司的要求上报。”(适用于含AE/SS/PQC的资料)











 苏公网安备32059002004080号
苏公网安备32059002004080号


