靶向CD3和CD20的双特异性抗体(BsAb)是治疗B细胞非霍奇金淋巴瘤(B-NHL)的新突破,目前全球范围内主要的CD3×CD20 BsAb有格罗菲妥单抗(Glofitamab)、mosunetzumab、epcoritamab和Odronextamab等。尽管BsAb显示出显著疗效,但也可能引发严重毒性,特别是细胞因子释放综合征(CRS),这对其安全使用提出了挑战。目前,临床试验中对BsAb相关毒性的评价多参考CAR-T细胞治疗,但两者之间差异化显著。为此,淋巴瘤研究基金会(LRF)组织国际专家小组,制定了评估和管理CD3xCD20 BsAb相关不良事件的共识建议。该共识于2024年4月份发表于Blood,通讯作者为纪念斯隆·凯特琳癌症中心的Lorenzo Falchi教授。【肿瘤资讯】将相关内容进行了整理,以飨读者。

CD3×CD20 BsAb毒性总结
CRS是CD3×CD20 BsAb后最常见的相关不良事件(AE),是一种急性系统性炎症综合征,以发热为特征,可伴有低血压、缺氧、器官功能障碍或高炎症综合征[6]。在BsAb的临床试验中,采取预防策略(如治疗开始期间递增剂量)以降低CRS发生风险。CRS的发生率、时间和严重程度因疾病亚型、BsAb产品、给药途径(静脉vs皮下)和给药计划而异(表1)。临床试验中的CRS 分级是根据2019年美国移植和细胞治疗学会 (ASTCT) 标准,大多数CRS为1级(20%~50%)至2级(5%~29%),但也存在更高级别CRS(1%~7%)。
在BsAb的临床试验中也观察到了神经毒性,根据不良事件通用术语标准 (CTCAE) 和 ASTCT 标准进行记录,两者都是为了描述免疫效应细胞相关的神经综合征 (ICANS)。目前尚无证据表明在接受BsAb治疗期间,患者脑脊液中存在BsAb药物分子、激活T细胞或促炎细胞因子。此外,已知颅内壁细胞不表达CD20(CD3×CD20 BsAb的靶点)[7],因此BsAb治疗相关神经毒性较少见,且通常比CAR-T细胞诱导的ICANS程度低。最常见的神经副作用是头痛和眩晕,类似ICANS的毒性发生率较低(1%~8%)。
除了上述的CRS和神经毒性外,本文对一些其他毒性也进行了讨论,包括燃瘤反应、血细胞减少症和感染性并发症等。
表1. 治疗B-NHL中CD3×CD20 BsAb的结构、给药、CRS和神经毒性的比较
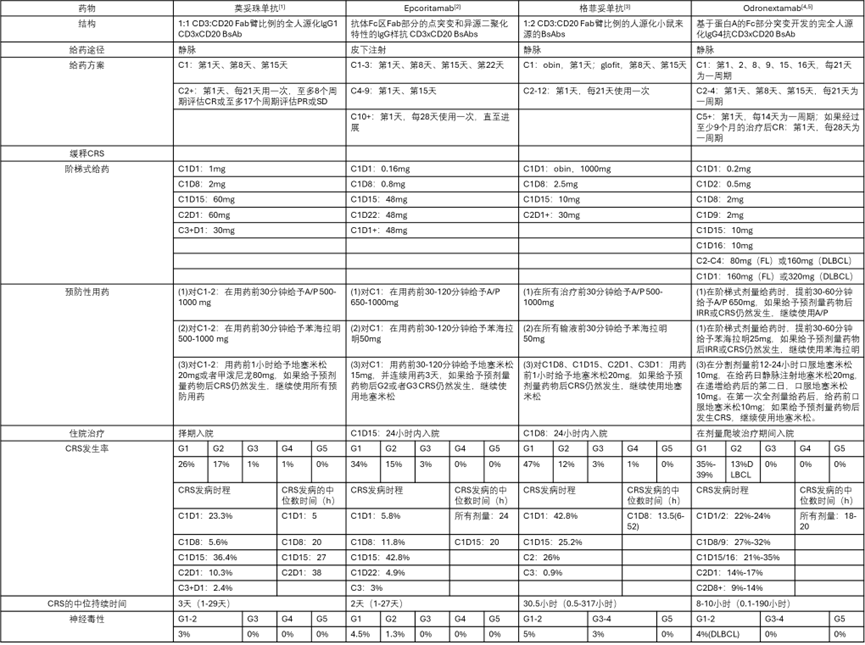
A/P,对乙酰氨基酚(扑热息痛);C,周期;CR,完全缓解;CRS,细胞因子释放综合征;DLBCL,弥漫性大B细胞淋巴瘤;FL,滤泡性淋巴瘤;G,等级;glofit,格菲妥单抗;IgG,免疫球蛋白G;IRR,输液相关反应;obin,奥妥珠单抗;PR,部分缓解;SC,皮下;SD,疾病稳定。
CRS的管理建议
治疗前评估
专家组建议:在CD3×CD20 BsAb治疗前,对患者进行全面体格检查和常规实验室检查,包括全血细胞计数、综合代谢组和乳酸脱氢酶检测。细胞因子水平等炎症标记物的基线检测在预测CRS方面价值尚不明确,可选做。基线心脏超声或MUGA根据临床需要进行,可有助于了解患者心脏储备和应对CRS相关血流动力学变化的能力。对于伴有心脏合并症的患者,若出现1级CRS,需更积极治疗以避免更高级别CRS导致的不稳定。了解潜在心脏疾病有助于决定治疗场所,特别是在门诊进行液体复苏困难时。另外,高龄、有合并症或疾病负荷重的患者面临更高BsAb毒性风险,因此应对这些患者进行更密切监测。
对于CRS评价、识别和管理的建议
a. 治疗前阶段
在CD3×CD20 BsAb治疗前,应讨论CRS的早期诊断和处理计划(表2)。
表2. 在启动CD3×CD20 BsAbs治疗前的保障措施

b. 患者的教育和监测
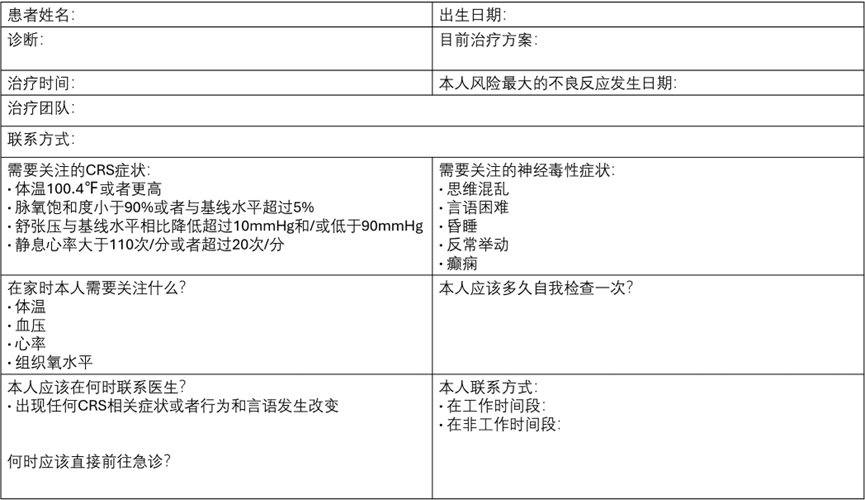
应向患者及看护人提供毒性观察和处理的教育资源,包括CRS和神经毒性的症状、医疗团队联系信息及生命体征自我监测说明等(表2、表3)。
表3.患者教育手册样本
c. 治疗场所
考虑到不同地区的资源差异,在CRS风险最高时期,监测可在门诊或住院部进行。监测地点应依据处方标签,并根据各中心能力调整(表2)。
d. 预防性用药
如表1所述,应根据 BsAb 的说明书使用预防性药物,包括预防性皮质类固醇。通常首选地塞米松,因为CRS的发生率低于其他皮质类固醇。如果在治疗第二周期后未发生CRS,可以在给药前后停用皮质类固醇。
e. 对CRS的管理
在静脉注射BsAb 时出现的发热可能难以与输液反应区分。在这些情况下,考虑到可能发生更严重的CRS,专家组建议在该治疗日暂停输注。
下表4列出CRS的分级定义。专家组一致认为:
对于1级CRS患者,可在门诊处理,并根据情况转诊到诊所或急诊科。
对于2级CRS患者,应尽快在医疗设施进行,继续服用解热药和地塞米松,并使用静脉补液纠正低血压。建议患者在住院部持续管理。对于使用地塞米松无效的2级CRS患者,建议尽早增加抗细胞因子疗法,如托珠单抗。
对于3级CRS患者,需立即转移至重症监护病房,并开始或继续使用退热药和皮质类固醇,并考虑其他抗细胞因子疗法。对于非典型CRS表现,建议进行诊断性检查排除其他诊断。
对于4级CRS患者,需采取积极管理措施,继续3级CRS的支持性措施,增加皮质类固醇的剂量,并结合抗细胞因子疗法。
表4. 根据严重程度提出的针对CD3×CD20 BsAbs相关CRS的管理方案
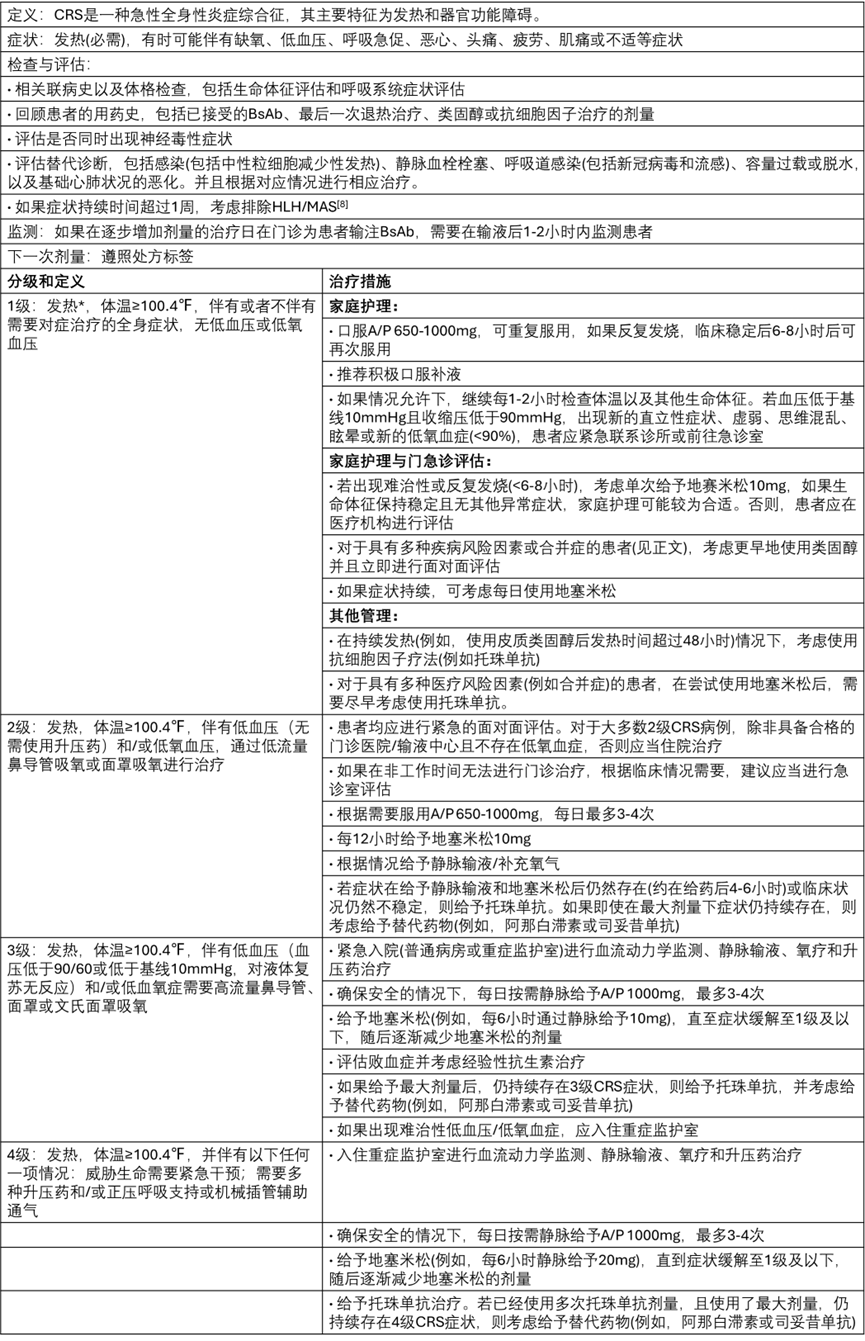
A/P,对乙酰氨基酚(扑热息痛);BP,血压;ICU,重症监护室;MAS,巨噬细胞活化综合征。在极少数情况下,使用退热药或皮质类固醇治疗的患者可能不会将发热作为CRS的首发症状。托珠单抗剂量:8 mg/kg体重静脉注射。对于CRS事件,每次事件不应使用托珠单抗超过两次(至少间隔8小时)或在6周内不超过3次。
f. 剂量调整和再治疗
专家组建议,临床医生需要参考每种BsAb的说明书,来进行剂量调整、中断或延迟、重新给药,以及CRS发作后的预防措施。同样,严重毒性反应(如CRS)后,应根据说明书决定是否重新使用BsAb。
g. 社区肿瘤学观点
淋巴瘤治疗的进展将推动实践变革和新疗法的应用。例如,CD3×CD20 BsAb等现成产品可能使社区中的淋巴瘤患者受益。社区肿瘤学实践应考虑咨询附近的社区或学术中心,特别是在剂量递增期间(CRS风险最高时),以确保紧急评价和管理的资源可用。这些疗法的使用可能促进社区和学术中心之间的合作,使患者能够在居住地附近获得新型治疗。
神经毒性的识别、评估和管理
在BsAb临床试验中,神经系统毒性不常见。对于无神经症状且检查正常的患者,无需常规神经检查,也无需限制驾驶。患者和看护人应了解神经毒性的潜在表现,监测任何神经状态变化。如出现与BsAb相关的神经毒性症状,建议遵循CAR T细胞疗法后ICANS的管理指南。BsAb神经毒性的管理应由多学科团队,包括神经内科和重症监护专家参与。发生神经毒性时,可以考虑额外使用皮质类固醇、住院和密切监测。考虑其他可能导致神经检查异常的原因,并进行评估和治疗(表5)。
表5. CD3×CD20 BsAb的神经毒性分级及推荐治疗
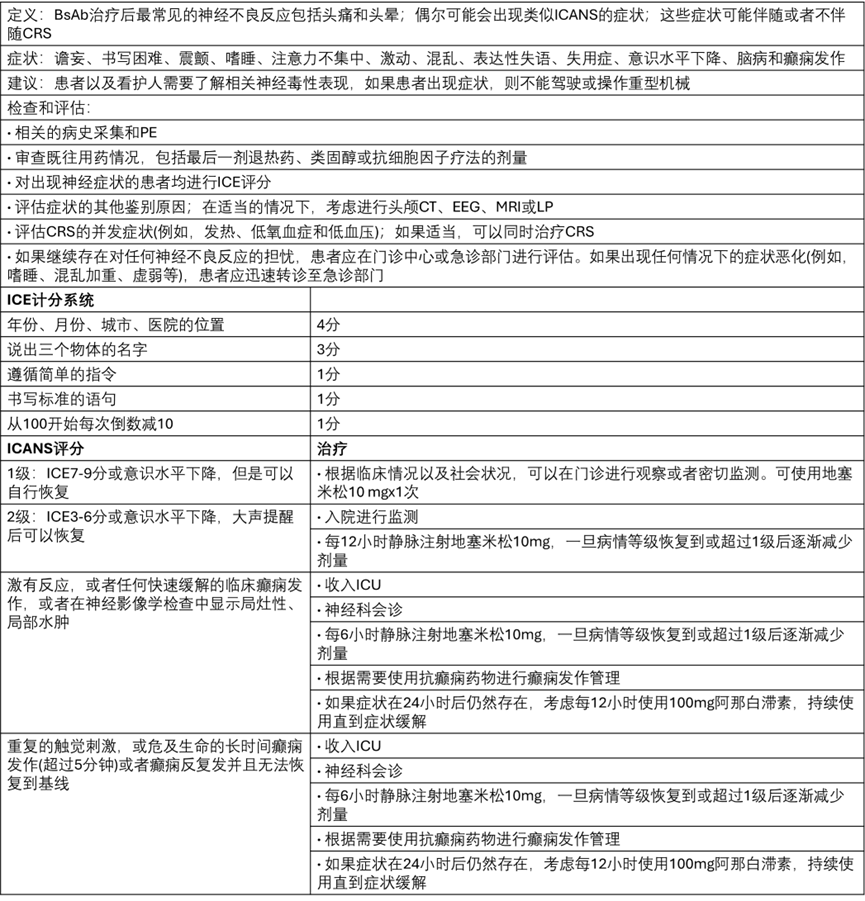
CT,计算机断层扫描;EEG,脑电图;ICE,免疫效应细胞脑病;ICU,重症监护室;LP,腰椎穿刺;MRI,磁共振成像;PE,体格检查
其他毒性的优化管理建议
a. 燃瘤反应
燃瘤反应在BsAb治疗中罕有发生,表现为淋巴瘤病灶体积短暂增加、皮肤发红、疼痛和发热,可能导致局部压迫或器官功能障碍。燃瘤反应通常在第一剂或第一次达到目标剂量时出现,可能与其他CRS症状同时发生。对重要结构附近有大病灶的患者,需采取缓解措施,如放射治疗,并在经验丰富的医疗中心进行监测和治疗。燃瘤反应对皮质类固醇治疗敏感。
b. 血细胞减少
治疗过程中出现中性粒细胞减少症的患者,可以使用生长因子支持,并根据说明书暂停BsAb治疗,平衡疾病控制与中性粒细胞减少症的风险。血小板减少症和发热同时发生时,应注意潜在的出血风险,遵循输血经验治疗贫血或血小板减少症。
c. 感染
活动性感染患者应暂停治疗,以减少免疫毒性的风险。新冠感染患者需根据当地指南管理。B细胞耗竭可能导致长期新冠阳性,应个体化咨询传染病专家。BsAb治疗可能导致低免疫球蛋白血症,应定期监测并考虑静脉免疫球蛋白替代治疗。建议预防肺孢子菌肺炎和水痘-带状疱疹病毒感染,尤其是接受类固醇预防治疗的患者,预防性治疗可能持续到BsAb治疗停止后6个月。乙型肝炎病史患者需进行抗病毒治疗。尽管BsAb患者疫苗反应可能受损,但专家组建议接种标准疫苗,包括流感和新冠疫苗。
d. 肿瘤溶解综合症
目前没有迹象表明BsAb治疗后肿瘤溶解综合征的风险高于其他疗法。专家组建议遵循淋巴瘤患者的标准治疗,对风险增加的患者进行监测和预防。
讨论
CD3×CD20 BsAb用于治疗惰性或侵袭性B-NHL,已获得监管机构批准,未来将逐渐会被临床广泛使用。临床对于这些药物的临床应用充满期待,尽管如此,仍需警惕其独特毒性,尤其是可能导致危及生命的CRS。专家组强调CAR-T细胞疗法和BsAb疗法中神经毒性的差异,指出CD3×CD20 BsAb的ICANS样毒性发生率较低。因此,对于无神经毒性症状的患者,并不普遍推荐进行常规的神经评估、神经系统疾病测试和驾驶限制。此外,这些建议不适用于所有情况,应结合临床判断,特别是高危CRS患者需更积极的监测和管理,必要时考虑替代疗法。
专家组和LRF致力于在获取更多信息或药物时更新建议,并开发和细化风险分层工具以提出更具体的监测和管理建议。BsAb可能会显著改变淋巴瘤治疗模式,需持续研究其毒性和疗效,为临床医生和研究人员提供指导。
1. Budde LE, Sehn LH, Matasar M, et al. Safety and efficacy of mosunetuzumab, a bispecific antibody, in patients with relapsed or refractory follicular lymphoma: a single-arm, multicentre, phase 2 study. Lancet Oncol. 2022;23(8):1055-1065.
2. Thieblemont C, Phillips T, Ghesquieres H, et al. Epcoritamab, a novel, subcutaneous CD3xCD20 bispecific T-cell-engaging antibody, in relapsed or refractory large B-cell lymphoma: dose expansion in a phase I/II trial. J Clin Oncol. 2023;41(12):2238-2247.
3. Falchi L, Carlo-Stella C, Morschhauser F, et al. Dexamethasone is associated with a lower incidence and severity of cytokine release syndrome compared with other corticosteroid regimens when given as premedication for glofitamab monotherapy in patients with relapsed/refractory (R/R) large B-cell lymphoma (LBCL) [abstract]. Blood. 2023;142(suppl 1):3130.
4. Bannerji R, Arnason JE, Advani RH, et al. Odronextamab, a human CD20×CD3 bispecific antibody in patients with CD20 positive B-cell malignancies (ELM-1): results from the Relapsed or Refractory Non Hodgkin Lymphoma Cohort in a single-arm, multicentre, phase 1 trial. Lancet Haematol. 2022;9(5):e327-e339.
5. Kim WS, Kim TM, Cho SG, et al. Odronextamab in patients with relapsed/refractory (R/R) diffuse large B-cell lymphoma (DLBCL): results from a prespecified analysis of the Pivotal Phase II Study ELM-2 [abstract]. Blood. 2022;140(suppl 1):1070-1071.
6. Lee DW, Santomasso BD, Locke FL, et al. ASTCT Consensus grading for cytokine release syndrome and neurologic toxicity associated with immune effector cells. Biol Blood Marrow Transplant. 2019;25(4): 625-638.
7. Parker KR, Migliorini D, Perkey E, et al. Single-cell analyses identify brain mural cells expressing CD19 as potential off-tumor targets for CAR-T immunotherapies. Cell. 2020;183(1):126-142.e17.
8. Hines MR, Knight TE, McNerney KO, et al. Immune effector cell-associated hemophagocytic lymphohistiocytosis-like syndrome. Transplant Cell Ther. 2023;29(7): 438.e1-438.e16.
排版编辑:肿瘤资讯-Kaylee











 苏公网安备32059002004080号
苏公网安备32059002004080号


