
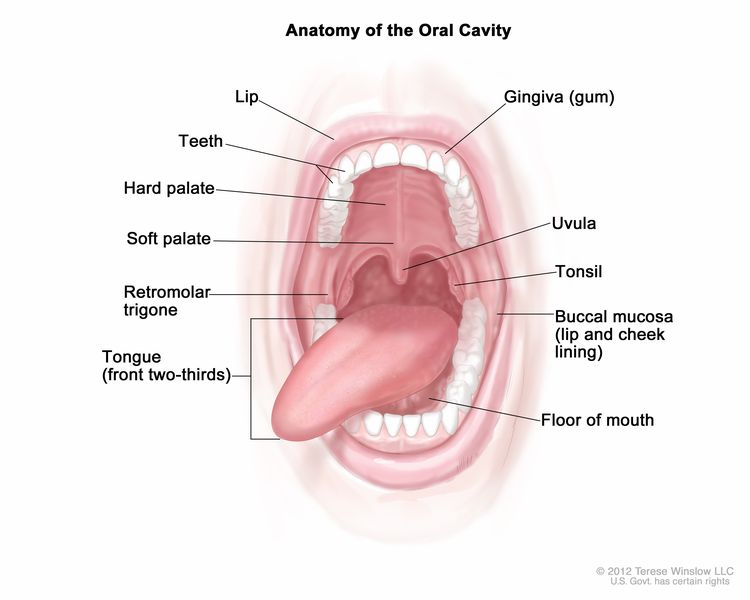
(图片来源:https://www.cancer.gov/types/head-and-neck/patient/adult/lip-mouth-treatment-pdq)
舌癌是一种常见的口腔癌,占口腔鳞状细胞癌的37%~53%[1],常表现为舌部的溃疡或肿块,可能伴有疼痛、口臭、言语及吞咽功能障碍等症状。治疗舌癌的主要方式包括手术切除、放射治疗和化疗。对于早期舌癌,手术和放疗是主要的治疗手段。而对于晚期患者,治疗则侧重于系统性治疗,并需结合多学科团队(MDT)的会诊来制定个性化的治疗方案。
本文分享一例由首都医科大学附属北京潞河医院程瑜蓉医师提供的病例,并邀请首都医科大学附属北京同仁医院张树荣教授进行点评。该患者为舌癌术后短期疾病进展,在当地医院接受信迪利单抗+白蛋白紫杉醇+奈达铂一线治疗1周期后,出现颈部皮肤肿瘤浸润,疾病快速进展。之后我院接受西妥昔单抗+白蛋白紫杉醇+顺铂二线治疗共6周期,其中3周期评效达PR后给予西妥昔单抗联合同步放疗,放疗结束后继续给予原联合方案治疗3周期。然后西妥昔单抗单药维持至今,疗效评估PR。
专家介绍
首都医科大学附属北京潞河医院
北京癌症防治学会肿瘤规范化推广应用专业委员会委员
北京肿瘤防治研究会癌症早筛早诊早治分委会委员
专业研究方向:肿瘤的分子精准治疗及免疫治疗相关毒副反应
主持在研通州区科委课题1项,参与多项国际及国内多中心临床研究
基本信息
患者:男,69岁
主诉:舌癌术后2月余,颈部肿痛1月
个人史:吸烟30年,平均20支/天,未戒,否认嗜酒史及其他特殊嗜好。
既往史:2012年因食管癌行手术治疗,术后病情稳定;3年前外伤后脑出血病史。
家族史:无特殊。
初诊情况:患者2023-2-28因“发现左侧舌侧缘肿物伴疼痛1月”就诊于当地医院,检查见左舌侧缘中后部见直径约2.5cm类圆形肿物,表面溃疡,基底浸润性生长,伸舌功能稍受限,活检病理提示鳞状细胞癌。
初诊辅助检查:
2023-3-1脑颈胸腹部CT:舌左侧软组织肿物影,大小约3.2*2.1cm,增强后可见不均匀强化,考虑恶性可能,颈部可见多枚淋巴结,最大径约1.0cm;
复查胃镜未见明显异常。
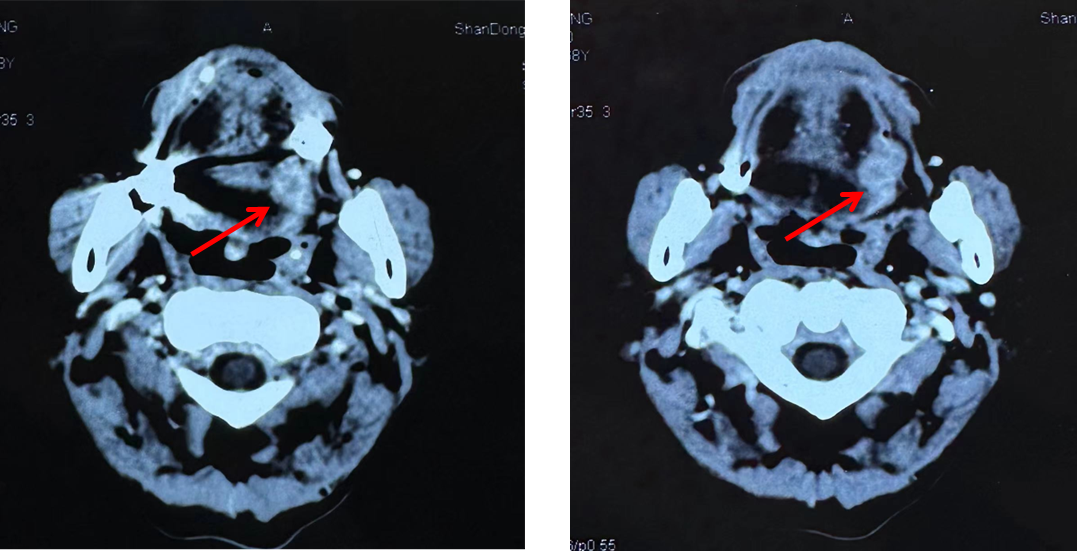
2023-3-1脑颈胸腹部CT
舌癌手术
2023-3-2行“舌恶性肿瘤局部扩大切除术+颈淋巴清扫术“;
术后病理:(左舌)中分化鳞状细胞癌。肿物切面3.8*1.5cm,累及神经。送检切缘均未见肿瘤,浸润深度约8mm。舌缘前部发白区域为上皮过度不全角化。颈部淋巴结10枚,其中4枚查见转移癌(4/10)。分期:pT2N2bM0 IVA期;
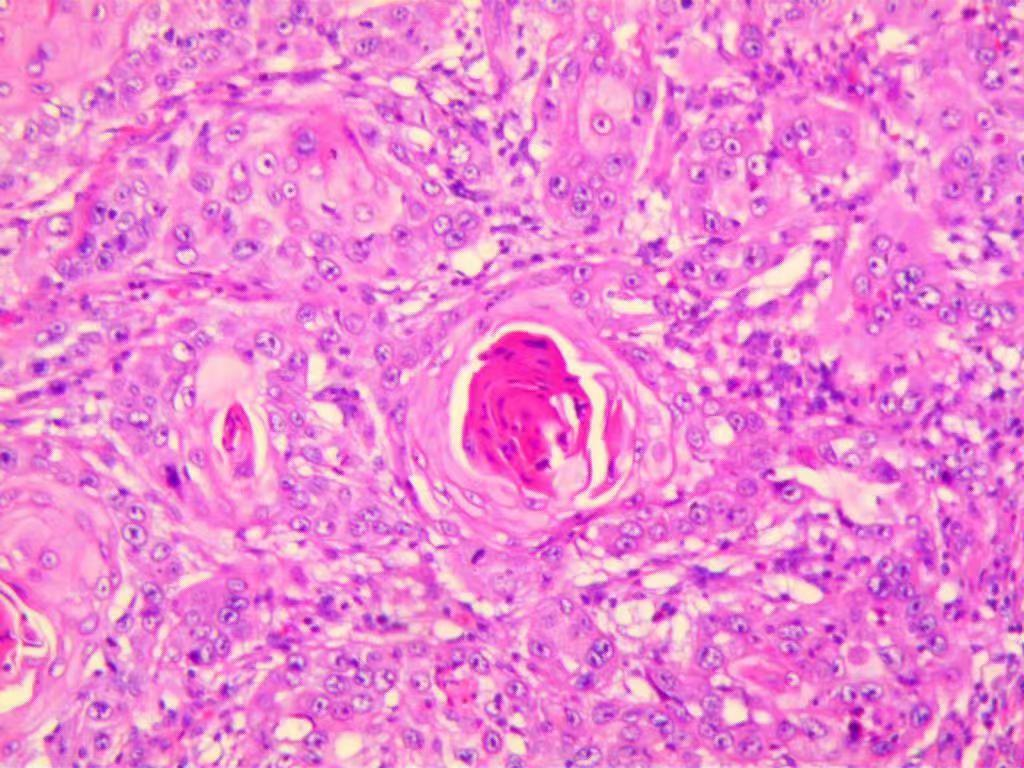
术后病理(左舌)
一、术后第1次疾病进展
2023-3-25开始出现左侧下颌及左颈部肿痛,范围约8.0*3.0cm,伴有针刺痛及红肿,左侧头面部放射痛,伴张口困难,夜间入睡困难,予抗感染治疗,效果欠佳;
2023-4-9颈部CT:舌肿瘤术后,左侧舌根部、左侧颌下及颈部软组织肿胀,首先考虑炎性病变。
2023-4-24鼻咽喉气管镜:会厌、舌根及下咽黏膜肿胀,未见新生物。
2023-4-24 PET-CT:口腔左侧壁及前下壁、左侧颌下、左前侧上颈部软组织增厚,葡萄糖代谢增高(SUVmax 22.3)
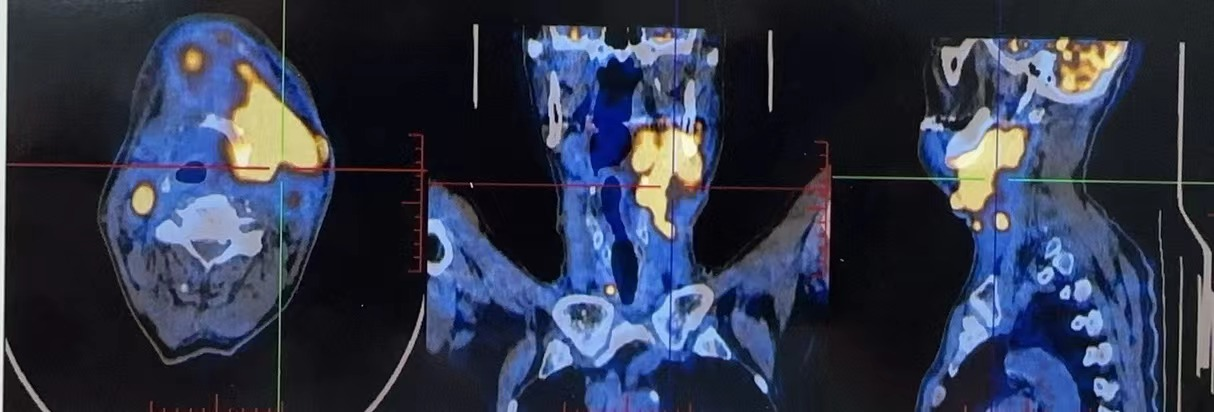
2023-4-24 PET-CT
2023-4-24 PET-CT:双侧颈部、锁骨上区多发代谢淋巴结(SUVmax 12.7),考虑术后疾病进展。
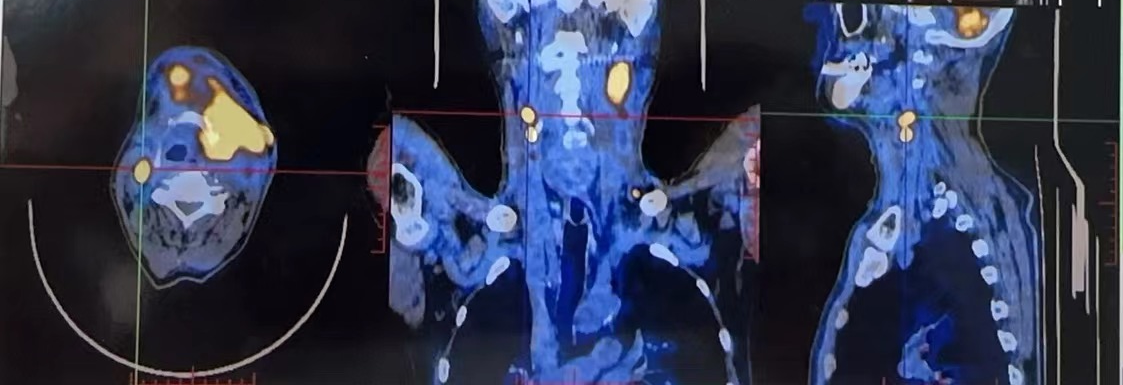
2023-4-24 PET-CT
一线治疗治疗方案:2023-4-28开始信迪利单抗200mg d1+白蛋白紫杉醇300mg(200mg/m2) d1+奈达铂(80mg/m2)120mg d1 q21d治疗1周期。
二、第2次疾病进展
一线治疗疗效:初期左侧颈部肿块继续增大,抗炎治疗后略缩小,最小约7.5*2.5cm,出现左侧颈部结节样病灶伴破溃出血,考虑皮肤浸润。评效PD。
一线方案不良反应:化疗后骨髓抑制,白细胞减少3级,乏力3级。
2023-4-30出现咳嗽、咳大量白痰,结合血常规、痰培养、降钙素原等检查考虑合并大肠埃希菌+白色念珠菌感染,开始头孢哌酮舒巴坦+氟康唑治疗。
2024年5月就诊我院。
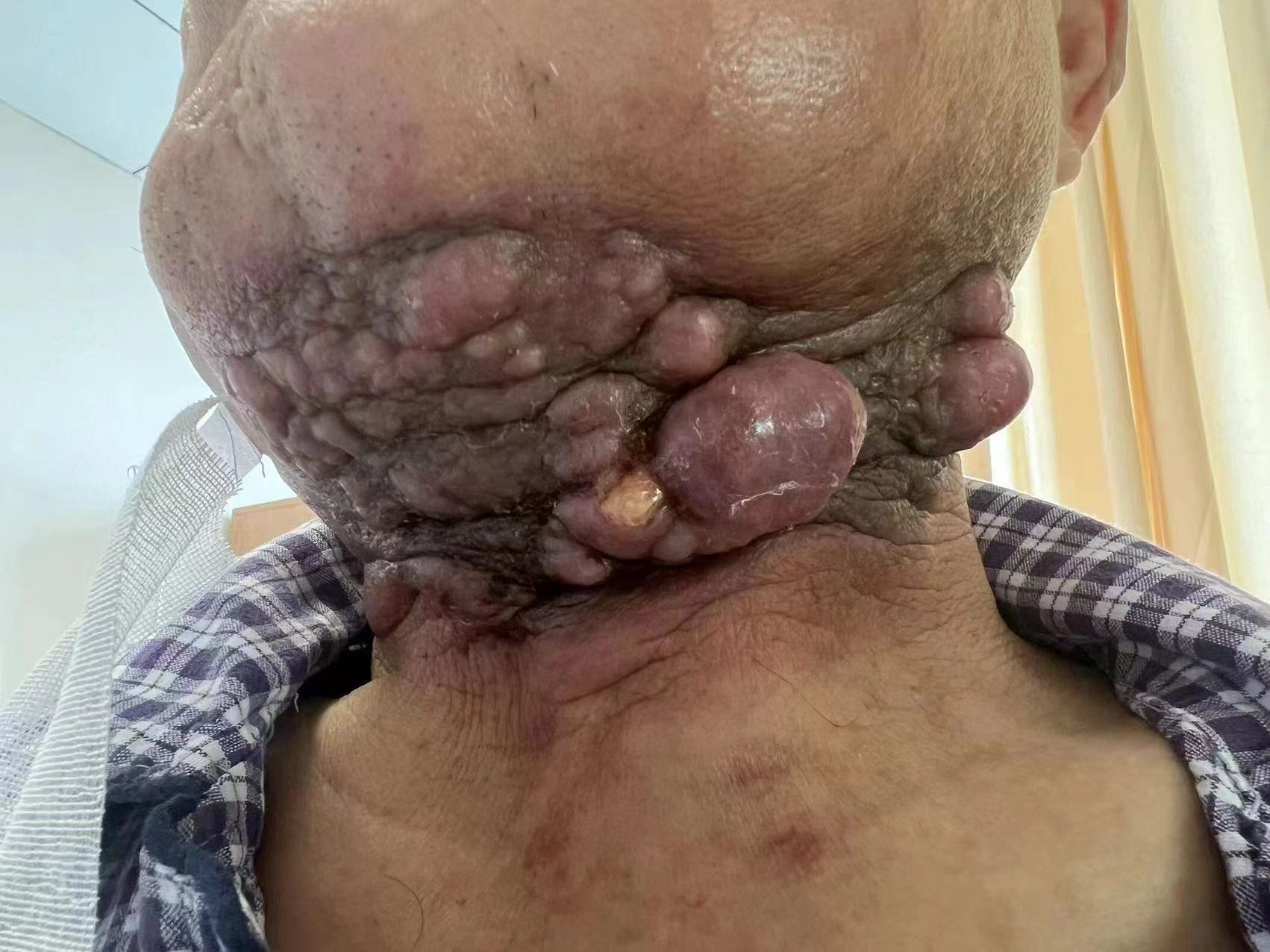
2023.5患者颈部外观
我院病理会诊:(右侧舌缘)(左侧颈部)中分化鳞状细胞癌,侵及肌组织,癌组织侵犯神经,脉管内见瘤栓;淋巴结见转移癌(4/10)。
补充检测:免疫组化:EGFR(++),MLH1(++),MSH2(++),MSH6(++),PMS2(+),HER2(0),p16(-);分子病理:EBER(-)。
NGS:共4个体细胞变异,其中具有明确或者潜在临床意义的变异2个:TERT基因c.-124C>T,TP53基因p.248Q,TMB:1.99个突变/Mb,MSS。PD-L1(22c3):TPS 1%,CPS 1。
MDT团队协作诊断及下一步治疗
初步诊断:
舌癌术后cT4aN3bM0 IVB期
双侧锁骨上淋巴结转移
双侧颈部淋巴结转移
颈部皮肤肿瘤侵犯合并感染
pMMR/EBER-/PD-L1 TPS 1%, CPS 1
MDT参与科室:口腔科、头颈外科、肿瘤内科、放疗科、影像科、病理科、营养科
MDT讨论内容:
1. 疾病特征:舌癌术后2月,分期为cT4aN3bM0 IVB期 双侧颈部、锁骨上淋巴结、皮肤浸润,pMMR EGFR(++)PD-L1低表达 疾病快速进展
2. 患者特征:老年男性,ECOG 1,器官功能好,局部肿瘤负荷大,伴疼痛、营养不良,化疗耐受性差
3. 治疗目标:控制疾病进展,改善生活质量
二线治疗经过
二线治疗方案:2023-5-22、2023-06-14、2023-07-06行3周期治疗:白蛋白紫杉醇(260mg/m2)200mg d1 d8,顺铂(80mg/m2)60mg d1-2 q21d+西妥昔单抗800mg(500mg/m2)q14d。
不良反应:化疗后骨髓抑制、白细胞减少2级、中性粒细胞减少2级、口腔黏膜炎2级。
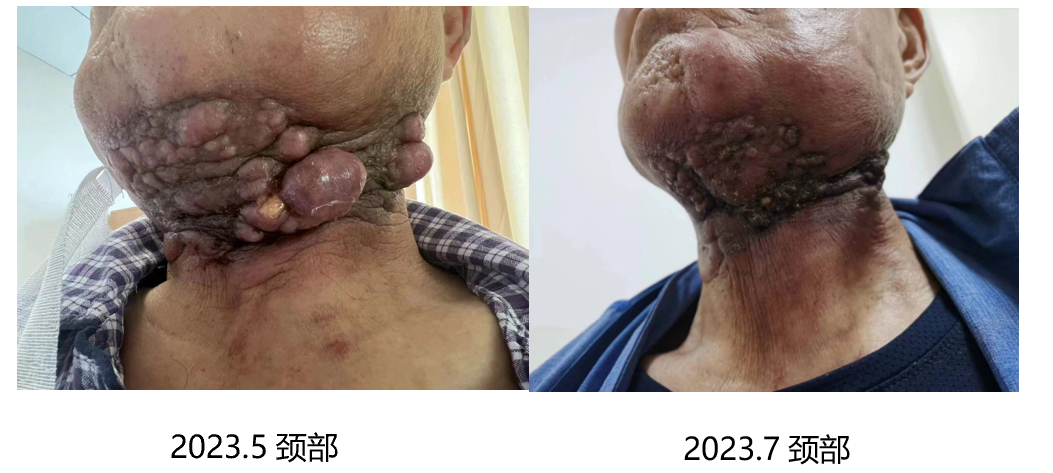
二线方案治疗3周期后疗效评估PR:
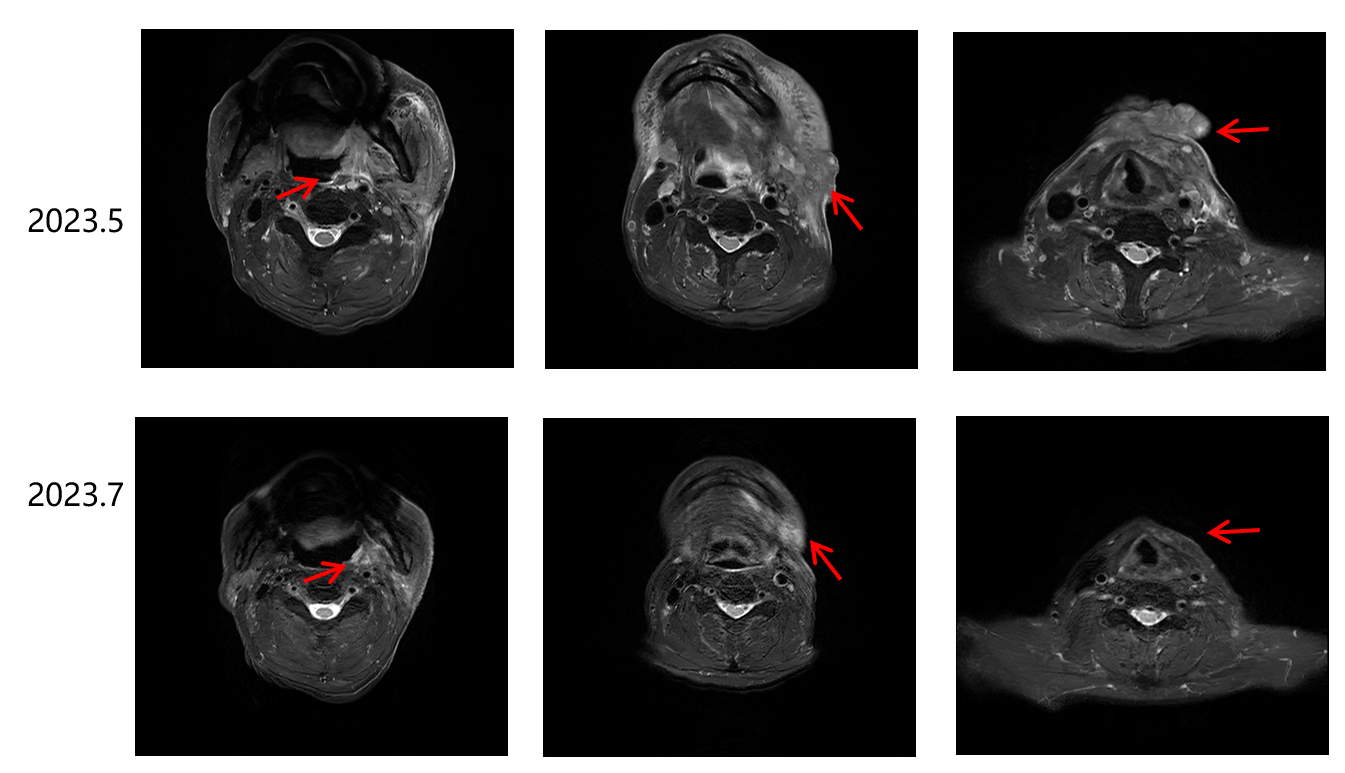
2023年5月和2023年7月颈部核磁
2023-7-17至2023-9-20行28次放疗(VMAT计划),同步每周西妥昔单抗(250mg/m2)治疗。
放疗计划:舌癌术后复发灶69.96Gy/2.12Gy/33F;颈部淋巴引流区60.06Gy/1.82Gy/33F;治疗期间出现颌下皮肤瘘,共执行放疗28次。
实际放疗总剂量:舌癌术后复发灶59.26Gy/2.12Gy/28F;颈部淋巴引流区50.96Gy/1.82Gy/28F。
不良反应及处理:放射性皮炎2级,局部使用外用抗生素联合糖皮质激素后减轻至1级
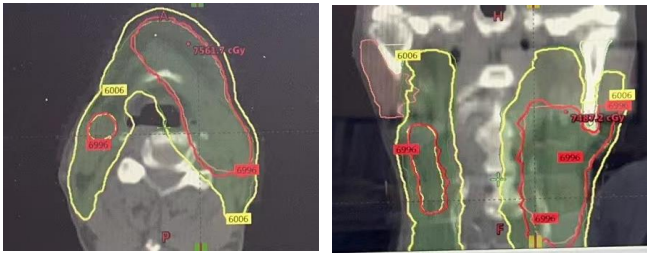
放疗靶区勾画情况
2023-10-14、2023-11-4、2023-11-25继续原方案(白蛋白紫杉醇+顺铂+西妥昔单抗)治疗3周期。放疗前后共完成6周期联合方案治疗。
2023-12-13开始西妥昔单抗800mg(500mg/m2)q14d维持治疗至今。
最佳疗效达PR。
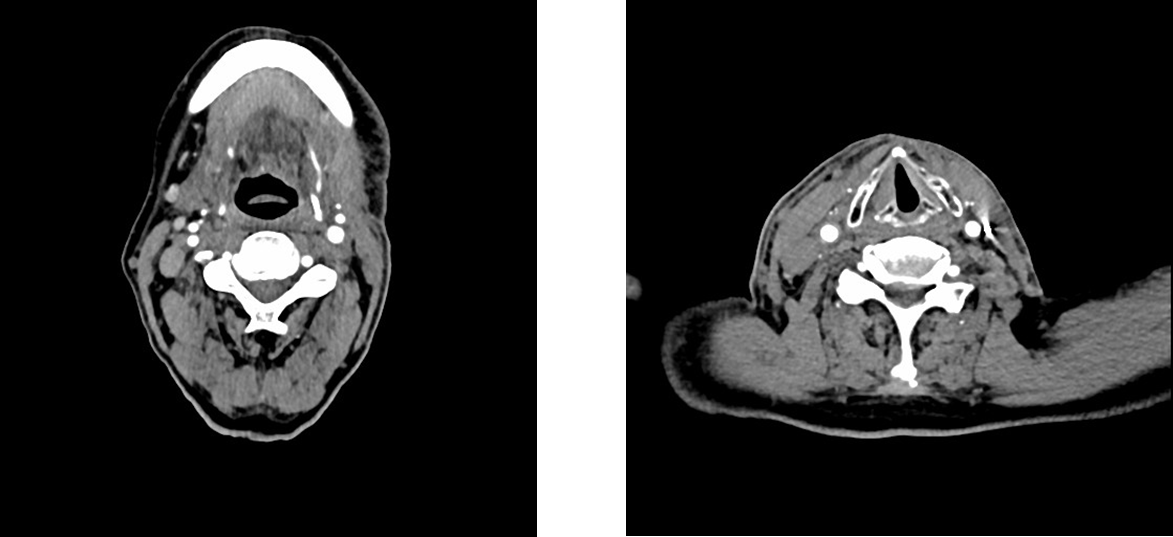
2023.12颈部CT:
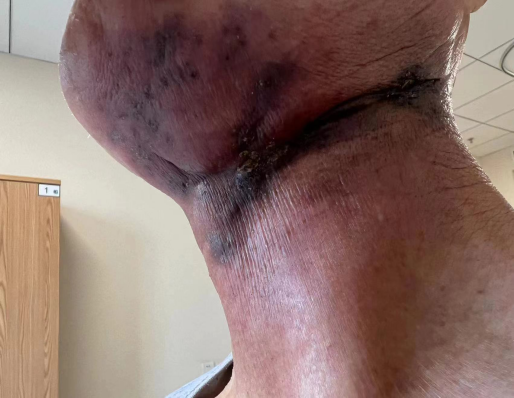
2023.12患者颈部外观
案例启示
R/M SCCHN患者存在很大异质性(复发转移模式、对治疗反应等),治疗模式及全程管理需要进一步细化;
抗EGFR单抗联合免疫治疗在R/M SCCHN中前景可期,治疗方案(包括联合治疗的AE)需要进一步优化;
放疗增敏选择:化疗/靶向/免疫/增敏剂;
西妥昔单抗耐药后的治疗选择。
专家介绍
首都医科大学
附属北京同仁医院 肿瘤中心
首都医科大学肿瘤学系第四届系务委员会委员
首都医科大学肿瘤学系头颈肿瘤学组(临床研究中心)主任
首都医科大学北京同仁医院头颈肿瘤MDT团队成员
中国健康促进基金会头颈肿瘤专委会副主委
中国医药教育协会疑难肿瘤专委会常委
中国抗癌协会肿瘤微创治疗专业会骨与软组织肿瘤
微创治疗分会委员
中国抗癌协会肿瘤热疗专业专业委员会
肿瘤热灌注化疗专家委员会委员
北京癌症防治学会头颈部黑色素瘤专业委员会常委
北京癌症防治学会头颈肿瘤MDT专业委员会常委
北京抗癌协会头颈肿瘤分子诊疗(MTB)专委会常委
北京药学会抗肿瘤药物专业委员会委员
北京医学奖励基金会肿瘤多学科诊疗专家委员会
研究型腺样囊性癌学组委员
该患者是一例较为复杂的舌癌术后复发的病例,整体治疗过程充分体现了局部治疗与系统性治疗的有机结合,各中细节具有典型性值得反复讨论和思考,为日后类似病例的诊治提供参考和帮助。
早期口咽癌常伴有隐匿性的颈淋巴结转移,根据2023版CSCO头颈部肿瘤诊疗指南推荐,除了原发灶切除外还需进行同侧选择性颈部淋巴清扫。该患者检查发现左舌侧缘中后部直径约2.5cm类圆形肿物,后行“舌恶性肿瘤局部扩大切除术+颈淋巴清扫术”,术后病理回报“颈部淋巴结其中4枚查见转移癌(4/10)”,提示患者可能有潜在的高危因素,根据指南推荐需行术后放疗或放化疗作为辅助治疗。但患者处于术后恢复愈合期,尚未接受辅助放疗即出现局部复发(双侧颈部、锁骨上区多发淋巴结转移,未见远处转移描述),需接受全身系统治疗。
对于局部和/或颈部复发,不适宜接受手术及放疗的患者,可参照复发/转移性头颈部鳞癌(R/M SCCHN)的治疗原则,以EXTREME方案为代表的靶向治疗和以“帕博利珠单抗联合化疗”为代表的免疫治疗,均可作为一线治疗的首选方案。KEYNOTE-048研究结果显示,当PD-L1 CPS<1时,EXTREME方案相比“帕博利珠单抗联合化疗”在PFS方面存在获益趋势,OS两组总体相似;当PD-L1 CPS 1-19及≥20时,两组治疗的PFS相似,“帕博利珠单抗联合化疗”的OS更长[2]。但同时也值得注意的是,“帕博利珠单抗联合化疗”的生存获益存在地区(亚洲/非亚洲国家)差异,KEYNOTE-048亚洲人群分析在各CPS水平均未发现“帕博利珠单抗联合化疗”相比于EXTREME方案的PFS和OS获益[3]。
该患者一线选择了“信迪利单抗+奈达铂+白蛋白紫杉醇”的免疫治疗方案,用药1个周期后即出现疾病进展,病理补测结果显示MSS/pMMR、EGFR(++)、CPS=1、TMB 1.99个突变/Mb。分析该患者免疫治疗后快速进展的原因可能是患者术后存在高危因素,同时术后自身免疫水平低,肿瘤部位免疫微环境较差,免疫治疗难以调动免疫细胞杀伤肿瘤,导致肿瘤局部进展迅速产生较大负荷。一般而言,对于肿瘤负荷大,免疫微环境差且伴有显著临床症状的患者,需为其快速缩瘤,应首选抗EGFR单抗联合化疗的靶向治疗;对于肿瘤进展相对缓慢,需要长周期治疗延缓OS拖尾效应的患者,可选择免疫治疗。另外,确定一线治疗方案前还需参考相关免疫组化检测,EGFR表达情况和CPS检测相对比较普遍,当CPS<1同时EGFR检测为阳性时应考虑靶向治疗,当CPS>1时可根据患者具体情况选择合适的治疗方式,一般认为免疫联合化疗的疗效随着PD-L1表达增加而增加;当CPS≥20时且患者年老体弱时,可能会选择免疫单药治疗。其他检测如通过NGS检测TMB等在不增加患者经济负担的情况下可作为辅助参考。在具体药品选择层面,对于一线治疗使用免疫联合化疗的患者,一般参照指南推荐或大型临床研究中使用的药品,如存在个别药物可及性问题时,在实践中也可进行同类替换,但对药品进行替换后可能会对疗效产生影响。总的来说,在选择免疫治疗和靶向治疗时需结合患者的具体情况进行个体化的全面考量。
此外,患者进行免疫治疗后短期内出现进展,需对“超进展”和“假进展”谨慎鉴别。“超进展”是病灶显著进展超过了在没有ICI的情况下的肿瘤生长速率。在ICI治疗期间相比于治疗开始前肿瘤生长动力学比(TGKR)≥2倍;“假进展”是治疗开始后肿瘤病灶有初始增加或出现新病变,但随后肿瘤负荷减轻,一般通过组织活检可证实为坏死或炎性细胞浸润。该患者免疫治疗一个周期后即出现进展,由于用药周期过短难以进行鉴别,不除外免疫治疗起效缓慢的可能。
一线免疫治疗进展后,靶向治疗常被用于挽救治疗。2023年ESMO大会报道的一项研究显示,在铂难治性R/M SCCHN中纳武利尤单抗经治后西妥昔单抗+紫杉醇ORR可达35%,OS可达18.3个月,相比于其他挽救方案均更高[4];另一项研究也显示,铂类药物难治性R/M SCCHN患者接受ICI治疗进展后在紫杉醇的基础上联合西妥昔单抗可获得显著的额外生存获益[5]。2023年ASCO大会上报道了一项“紫杉醇联合西妥昔单抗双周治疗用于既往接受含铂化疗和PD-1抑制剂治疗的R/M SCCHN患者”的II期研究6],结果显示紫杉醇联合西妥昔单抗挽救治疗的ORR达到68.7%, DCR为93.9%,mPFS为5.6个月,二线开始的mOS 为13.4个月,且安全性可控。2022年ESMO大会上的一项回顾性研究分析了使用纳武利尤单抗+铂类的R/M SCCHN患者在治疗失败后的临床治疗数据[7],结果表明免疫进展后使用西妥昔单抗+紫杉醇的患者ORR达到54.9%,DCR为81.7%,均高于其他二线方案且多变量分析显示使用西妥昔单抗+紫杉醇是PFS和OS更有利的独立影响因素。这些研究均展现出靶向治疗可以作为免疫治疗失败患者的有力的挽救选择。
该患者在二线挽救治疗中采用了“白蛋白紫杉醇+顺铂+西妥昔单抗治疗,放疗同步西妥昔单抗治疗,后续含西妥昔单抗的维持治疗”的方案,整体模式与局部晚期的“诱导治疗+放疗+后续靶向维持治疗”根治性策略类似,患者症状得到改善,最佳疗效维持PR,体现了既往临床研究中靶向治疗在免疫治疗失败的挽救治疗中发挥的积极作用和快速缩瘤效果。此外,长期药物治疗尤其是化疗的应用,对骨髓及内脏器官均会产生较大累积负荷导致损伤,总OS可能会收受到影响,利用局部放疗可在保证治疗效果的同时减轻机体总用药负荷,延缓损伤导致的脏器功能衰退,是该阶段合理的选择之一,该患者在西妥昔单抗联合化疗的诱导后,通过放疗同步西妥昔单抗进行局部根治,再次展现了系统治疗与局部治疗的有机结合,同时也表明接受过免疫治疗和靶向治疗的患者对放疗仍具备敏感性。最后,局部晚期头颈部鳞癌放疗结束后仍有一定比例的复发率,放疗后如何进行临床选择,是否需要维持治疗及治疗方案的设计仍需前瞻性临床试验验证。本病例在放疗后使用了辅助治疗及西妥昔单抗的维持治疗,并取得了稳定的疗效,为放疗后的方案选择提供了一种新的思路。
[1]中华人民共和国国家卫生健康委员会.舌癌诊疗指南(2022年版)http://www.nhc.gov.cn/yzygj/s7659/202210/a19e8d0e0c25475fbc8958ed670893c8/files/5dcd7a8ae8bc4225b3dd0042456943de.pdf
[2]Burtness B, et al. Lancet. 2019 Nov 23;394(10212):1915-1928.
[3] Nuttapong Ngamphaiboon, 2019 ESMO ASIA.
[4] 2023 ESMO 940P.
[5] 2023 ESMO 942P.
[6] 2023 ASCO PO6032.
[7] 2022 ESMO 679P.
排版编辑:肿瘤资讯-GY











 苏公网安备32059002004080号
苏公网安备32059002004080号


