
约20%结直肠癌的患者在初诊时已经发生了转移,手术较为困难,mCRC患者在历经多线治疗后,可用药物有限。前线治疗以基于伊立替康、奥沙利铂的化疗联合方案为主,进入三线治疗后可选TAS-102、呋喹替尼与瑞戈非尼。对于无法耐受静脉化疗的患者,可能会优先考虑使用三线口服药物。其中,TAS-102除单药使用外,近年来也在探索联合贝伐珠单抗、呋喹替尼、瑞戈非尼等药物的联合应用,在临床实践中的应用价值逐渐提高。【肿瘤资讯】特邀程先硕教授、肖斌教授、李中福教授、肖英教授、阎婷婷教授与陈利辉教授,分享带来2例晚期结直肠癌病例,患者接受TAS-102联合治疗后获得良好生存获益。
病例一:
TAS-102联合贝伐珠单抗方案在mCRC患者后线治疗中可持续发挥作用
病例汇报:程先硕教授 北京大学肿瘤医院云南医院
病例点评:
肖斌教授 保山市人民医院
李中福教授 重庆市急救医疗中心
博士,主治医师
云南省肿瘤医院/昆明医科大学第三附属医院结直肠外科
云南省干细胞与再生医学协会第一届委员
云南省抗癌协会肿瘤药物临床研究专业委员会第一届委员
云南省医学会肿瘤学分会泛家族遗传性肿瘤防控学组秘书
云南省医学会外科学内分泌外科专业学组组员
擅长结直肠癌微创治疗;复发,转移性结直肠癌的综合诊治。
主持云南省省级项目2项,参与国家重点研发计划1项,国家自然科学基金3项,云南省科技厅重点项目3项,其他省级项目10项
WJGO, Cancer Investigation, Frontier in immunology,Frontier in oncology, PLOS one等杂志审稿人
《南方医科大学学报》特约审稿专家,2023年度优秀审稿专家
获得云南省科技进步奖一等奖1项,西山区科技进步奖二等奖1项
参编专著2部,译著1部,授权发明专利1项,申请发明专利4项,发表论文50余篇,其中,专家论坛1篇,SCI :16篇。
病例介绍
1. 患者基本情况
一般资料:女,64岁。
主诉:反复下腹部疼痛1年余,加重3月余。
家族史:父亲气管癌、母亲直肠癌病史(已故)。
身体情况:BMI 23 Kg/m2;体重 60 kg,身⾼ 147 cm,BSA 1.52 m2; ECOG PS评分:1分;营养⻛险评分(NRS)1分;⽇常⽣活能⼒(ADL)I级。
肿瘤标记物: CEA:2.38 ug/L,CA242:3.95 Ku/L,CA19-9:11.14 Ku/L,CA125:17.65 Ku/L。
影像学检查:
CT(2018-06):1.回盲部肠壁不规则增厚并肿块形成,大小约5.6 cm×5.0 cm×6.2 cm,病变局部累及回肠末端,病变肠壁浆膜⾯局部⽑糙,周围脂肪间隙稍模糊;病变肠周多发(>7枚)肿⼤淋巴结,⼤者约1.2 cm×1.1 cm。2.后子宫肌壁⻅⼀稍低强化肿块,⼤⼩约3.0 cm×2.7 cm,考虑⼦宫肌瘤可能。
乳腺超声(2018-06):两侧乳腺增⽣超声改变。双侧腋窝、双侧腹股沟淋巴结:未⻅肿⼤。
肠镜(2018-06):1.盲肠、回盲瓣⼝旁肿块型癌?待病检。2.所⻅其余结肠⼤致正常。
病检:黏液腺癌。
诊断:1.回盲部黏液腺癌 MSS型 pT4bN2aM0 ⅢC期;2.⼦宫肌瘤。
2. 治疗经过
2018-07 腹腔镜根治性右半结肠切除术。
术后病理报告:(右半结肠及肿瘤)黏液腺癌,癌组织浸润肠壁固有肌层全层达浆膜下脂肪组织。标本两端切缘、阑尾于镜下未见癌组织。肠系膜周围淋巴结(6/16)见癌转移,另见癌结节2枚。
术后重要基因检测:KRAS+。
2018-08 一线治疗:术后辅助化疗mFOLFOX6(9周期),SD。
MRI: 肝S8一类圆形长T1长T2信号结节,约1.2 cm×1.2 cm,增强不均匀环形强化,考虑转移。
2018-09 超声引导下行射频消融术。
2019-07 右乳乳头状癌 cT2N0M0 ⅡA期,患者拒绝手术,行内分泌治疗(阿那曲唑)。
2021-07 肝上结节增大增多,疾病进展。
二线治疗:FOLFIRI+贝伐珠单抗⽅案化疗11周期。患者体弱,中途放弃。
2021-12 复查CT: 1、肝右前叶上段多发结节(2.5*2.1 cm),考虑转移。2、肝门区、门腔间隙多发肿大淋巴结,考虑转移(3.6*2.0 cm);上中腹腹膜后多发小淋巴结显示,部分较前稍缩小,部分同前。
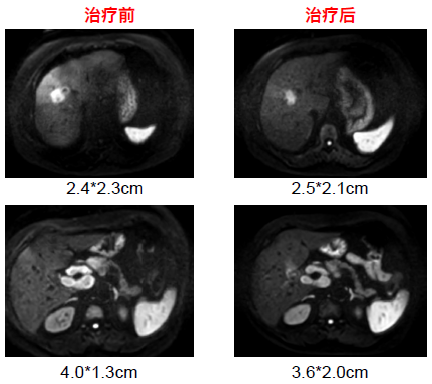
图 1 ⼆线治疗期间影像学⽐较
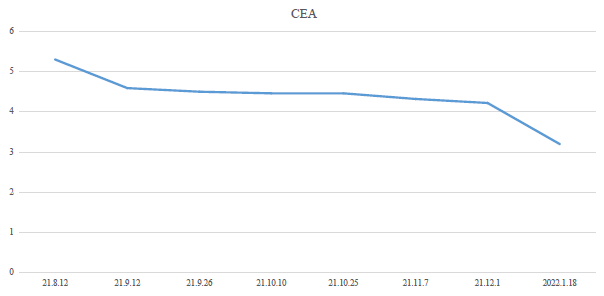
图 2 肿瘤标志物CEA的变化
2022-05 术后4年,肝穿刺活检术:镜检示肝组织增⽣伴脂肪变性,少许炎细胞浸润,局部见游离粘液湖,未见上皮成分。
2022-08 三线治疗:TAS-102+贝伐珠单抗治疗至今,截至目前累计行该方案15周期。
2024-3 复查CT:1、轻度脂肪肝;肝右前叶多发结节(1.7*1.5 cm),较前稍缩小;2、肝门区、门腔间隙多发低密度灶(2.3*2.0cm),考虑淋巴结肿大,较前稍缩小。
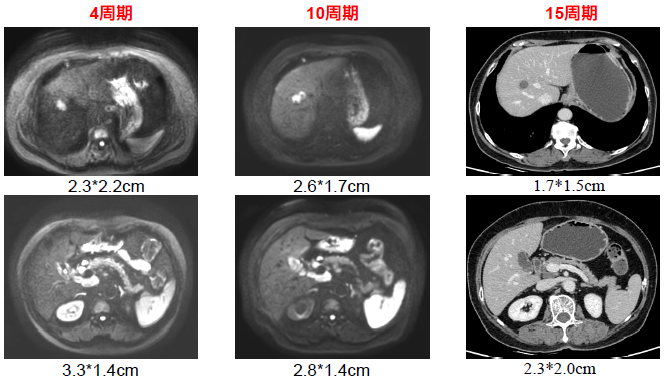
图 3 三线治疗期间影像学⽐较
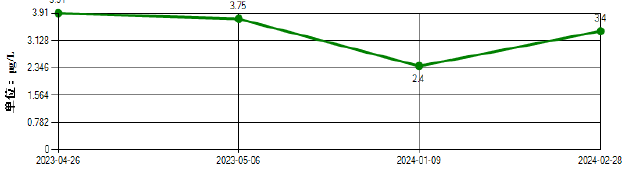
图 4 肿瘤标志物CEA的变化
3. 病例小结
该患者首诊诊断为回盲部黏液腺癌 MSS型。经根治性手术后一线接受mFOLFOX6辅助化疗。复查提示肝转移(S8),行超声引导下射频消融术。期间患者不能坚持化疗,定期复查。2019年07月,术后1年确诊右乳乳头状癌,cT2N0M0 ⅡA期,患者拒绝手术,行内分泌治疗(阿那曲唑)。2021年7月,术后3年,肝右叶,肝门区转移进展,行二线治疗,FOLFIRI+贝伐珠单抗方案化疗11周期,疾病稳定,但由于患者体弱,中途放弃。2022年7月,术后4年,考虑转移再次进展,经MDT会诊后,考虑患者高龄,化疗毒副作用大,患者不能耐受,于 2022年8月开始行TAS-102+贝伐珠单抗治疗至今,疾病达PR,截至目前累计行该方案15周期。
保山市人民医院肿瘤科主任医师
云南省医师协会《肿瘤医师分会》常委、委员会委员
云南省抗癌协会老年肿瘤专业委员会委员
云南省抗癌协会淋巴瘤专业委员会委员
云南省医学会放射肿瘤治疗学分会第三届委员会委员
云南省医师协会肿瘤多学科诊疗专业委员会委员
云南省抗癌协会肿瘤生物治疗专业委员会委员
保山市医学会呼吸病学专科分会委员会委员
保山市医学会肿瘤学分会委员会委员
主任医师、硕士研究生导师、重庆市急救医疗中心主任
中国NOSES联盟重庆分会理事
重庆胃肠外科联盟常务理事
重庆市医学会外科专委会委员
重庆市医院管理协会外科管理专委会常务委员
重庆市中西医结合胃肠肿瘤专委会常务委员
重庆市抗癌协会胃癌专委会副主任委员
重庆市抗癌协会大肠癌专委会常务委员
重庆市抗癌协会微创外科专委会委员胃肠外科学组委员
重庆市抗癌协会胃肠间质瘤委员会常务委员
重庆市医师学会肿瘤MDT委员会委员
《现代医药杂志》编委
发表学术论文20余篇、其中SCI收录6篇
肖斌教授:回盲部是炎症、息肉、肿瘤的好发部分。回盲部肿瘤治疗参照结直肠癌指南。该病例从初诊到三线治疗体现了多学科诊疗的优势,涉及手术、放疗、化疗、病理学、影像学等多学科的规范化治疗。整体诊疗经过较为成功,患者术后发现肝转移后,接受化疗治疗方案,但耐受性较差。较为幸运的是,患者对TAS-102+贝伐珠单抗治疗敏感,病情得到控制,病灶缩小、CEA下降,达PR。此外患者同时患有乳腺癌,通过该病例我们可以发现在双重肿瘤、肿瘤反复复发进展的患者中,规范化诊治至关重要,为患者带来疗效最大化。
李中福教授:结直肠癌根治术后肝转移并不少见,从外科医生角度来看,如果转移病灶有机会行手术后达到R0清除,则更倾向于手术治疗。此外约20%的结直肠癌患者在初诊时已经发生了转移,手术较为困难,如何通过内科等治疗方式在治疗后将肿瘤转化为可切除状态是外科医生更为关注的。该病例后期出现肝多发转移,经过二线、三线治疗后取得较好效果,在治疗过程中如果有机会再次行基因检测,推荐复查基因检测,探索是否可行靶向治疗。
病例二:
TAS-102为不能耐受化疗的mCRC多发转移患者提供治疗希望
病例汇报:肖英教授 重庆医科大学附属第一医院
病例点评:
阎婷婷教授 云南大学附属医院
陈利辉教授 重庆大学附属肿瘤医院
医学博士
重庆医科大学附属第一医院肿瘤科主治医师
重庆市中西医结合学会肿瘤专委会青年委员会委员
重庆市医师协会放射肿瘤治疗医师分会近距离治疗学组委员
重庆市中西医结合学会肿瘤放疗专委会青年委员
重庆市医学会胃肠肿瘤MDT专业委员会工作秘书
主要研究方向:消化道肿瘤、头颈部肿瘤、妇科肿瘤、肺癌
病例介绍
1. 患者基本情况
一般资料:男,50岁。
主诉:结肠癌肝转移术后化疗联合靶向治疗后。
病史:2019-06患者多次出现进食刺激性食物或饮酒后腹部绞痛,以中下腹为主,每次持续数小时,自行服用药物后可缓解。就诊前2周再次出现饮酒后腹部绞痛,症状同前,持续2天后缓解。
既往史:高血压病。
查体:ECOG 评分0分,腹部无明显阳性体征。
肿瘤标志物:CA19-9: 26.2,CEA: 14.3↑。
影像学检查:
肠镜(2019-12):进镜80 cm(横结肠远端?)见肠腔内菜花状新生物侵及一圈,肠腔狭窄,肠镜无法通过,于该处取组织送检,取检后于该新生物周围黏膜下注射纳米炭示踪,染色效果好。80 cm以下结直肠黏膜轻度水肿,未见确切新生物或溃疡。
活检:结肠腺癌。
胸部平扫、全腹部、盆腔增强CT:横结肠肠壁增厚,符合结肠癌表现,病灶累及浆膜面及肠周脂肪间隙,肠周及中结肠系膜区多发转移淋巴结可能性大。右肺小结节,转移不除外,建议短期复查。脂肪肝;肝囊肿。左侧肾上腺髓脂瘤可能。
诊断:结肠脾曲中分化腺癌pT4N0M0,ⅡB期;横结肠息肉;原发性高血压病2级 很高危;肺结节性质待定;脂肪肝;肝囊肿。
2. 治疗经过
2019-12 腹腔镜辅助左半结肠切除术。
术后病理报告:左半结肠中分化腺癌,侵及全层及肠周。未见明显脉管侵犯,见神经侵犯。近切缘、远切缘、放射状切缘、网膜未见癌累及。肠周淋巴结未见癌转移(0/12)。
基因检测:MSH2(+),MSH6 (+),MLH1 (+),PMS2 (+),KRAS G13D(+), NRAS (-),Braf(-),Ki-67 40%(+),S100神经纤维(+),MSS。
一线治疗:外院行Capox方案辅助化疗半年。
2020-12 复查上腹部增强MRI:肝S5转移瘤可能性大。
行全麻下腹腔镜肝部分切除术+胆囊切除术+腹腔粘连松解术。
术后病理报告:肝结合免疫组化及临床病史,符合结肠癌转移。肝切缘未见癌累及。慢性胆囊炎伴胆固醇沉着。
免疫组化:CSX2(+),STAB2(+),VILLIN(+),HC(-),ARG1(-),CK7(-),CK20(+)。
基因检测:BRAF野生型,KRAS p.G13D错义突变,NRAS野生型,MSS,UGT1A1*28野生型,UGT1A1*6杂合突变型。
二线治疗:FOLFIRI方案化疗3周期。
2021-01 肝转移复发,超声引导下行肝脏射频消融治疗。
FOLFOXIRI+贝伐珠单抗治疗第4~6周期。
2021-04 患者出现严重恶心、呕吐,无法耐受,血常规示三系降低。停用奥沙利铂。
FOLFIRI+贝伐珠单抗治疗第7~12周期。
2021-12 停药4月,复查PET-CT考虑肺转移。
TAS-102+⻉伐珠单抗治疗5周期,疗效达PR。出现腹泻、三系降低。
2022-09 自行停药4个月后疾病进展,恢复TAS-102+⻉伐珠单抗治疗。出现乏力、心跳加速、无法行走,三系降低,无法耐受,2023-01暂停用药。
2023-02 复查提示进展,贝伐珠单抗联合TAS-102双周方案(d1-5)治疗,TAS-102减量为标准剂量的75%。
2023-08 CT:左半横结肠吻合口肠壁增厚,与2023-05-15 CT片比较肠壁增厚程度可疑加重,建议结合肠镜检查;肝多发小转移灶,部分消失(S8),部分缩小;双肺多发转移,较前相仿。
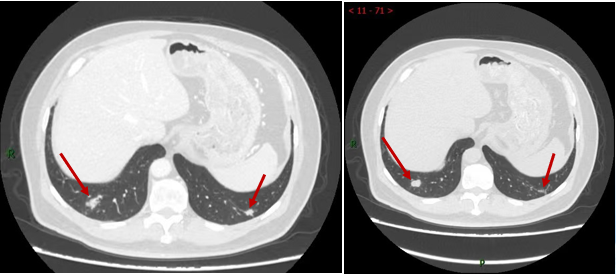
图 5 CT(2023-08-11)
患者肿标持续上涨,但影像学评估治疗有效。患者无法耐受强烈治疗方案,继续原方案治疗。
2023-09 骨扫描提示多发骨转移。
三线治疗:TAS-102联合呋喹替尼。用药1周期,肝功能异常,停药。
2023-11 MR头颅平扫考虑脑转移。
2023-12 肝衰竭死亡。
3. 病例小结
患者50岁男性,确诊结肠脾曲中分化腺癌pT4N0M0,ⅡB期,行腹腔镜辅助左半结肠切除术,术后于外院行Capox方案辅助化疗半年。1年后复查MRI肝转移瘤可能性大,行全麻下腹腔镜肝部分切除术+胆囊切除术+腹腔粘连松解术。术后行二线治疗,给予FOLFIRI方案化疗3周期,肝转移瘤明显缩小。超声引导下行肝脏射频消融治疗后,予FOLFOXIRI+贝伐珠单抗治疗第4~6周期,出现严重恶心、呕吐,无法耐受,血常规示三系降低。停用奥沙利铂,FOLFIRI+贝伐珠单抗治疗第7~12周期。术后2年出现肺转移,TAS-102+⻉伐珠单抗治疗5周期,肿瘤标志物下降,肺转移缩小,疗效达PR。出现轻度腹泻、三系降低。患者因经济原因自行停药4个月后疾病再次进展,恢复TAS-102+⻉伐珠单抗治疗后因不能耐受不良反应暂停用药。调整方案,贝伐珠单抗联合TAS-102双周方案(d1~5)治疗,TAS-102减量为标准剂量的75%,病情平稳。半年后发现骨转移,由于患者无法耐受强烈化疗,继续保留TAS-102作为基础化疗方案,三线行TAS-102+呋喹替尼治疗,用药1周期出现肝功能异常,停药后1月MR头颅平扫考虑脑转移。
云南大学附属医院肿瘤科、主治医师
云南省医学会肿瘤学分会第十届委员
中华结直肠癌MDT联盟云南分盟委员
云南省转化医学学会精准放射治疗分会委员
云南女医师肿瘤支持与康复专业委员会委员
云南省预防医学会健康传播分会委员
副主任医师
重庆大学附属肿瘤医院胃肠肿瘤中心
2010年毕业于四川大学华西临床医学院
硕士研究生
2018年赴美国佛罗里达医院访问学习
重庆市抗癌协会会员
重庆市解剖学会会员
中西医姑息治疗专委会委员
重庆市造口专业委员会委员
阎婷婷教授:该患者术后行化疗辅助治疗,1年后出现肝转移,行全麻下腹腔镜肝部分切除术,后予化疗二线治疗,期间疗效显著,但肿瘤标志物仍高,建议继续维持治疗。目前mCRC可用药物仍不多,且mCRC进入慢病管理阶段,停药可能加重患者复发风险,可以选择低毒、低强度药物维持治疗提高患者生存期和生活质量。患者疾病进展后对贝伐珠单抗联合TAS-102治疗反应较好,但该患医从性差导致最终再次较快进展。
陈利辉教授:该病例在出现肝转移后行手术治疗,为患者带来获益。术后可以考虑化疗联合靶向治疗。患者出现肝转移、肺转移、骨转移、脑转多发转移,但最终死于肝衰竭,说明mCRC的治疗需要综合考虑,平衡治疗和不良反应之间的关系。此外,出现转移时可再次行基因检测,如果有免疫治疗或靶向治疗机会,可给予相应治疗。对于三线以及后线治疗,单药治疗不良反应相对较轻,可能维持更长时间治疗。
总结
TAS-102疗效显著,为晚期结直肠癌患者提供更多选择
结直肠癌(CRC)是我国第二大癌症,2022年2月国家癌症中心发布的最新统计数据显示,每年新发肠癌达40.8万人[1]。约20%结直肠癌的患者在初诊时已经发生了转移,手术较为困难[2]。mCRC患者在历经多线治疗后,可用药物有限,TAS-102是mCRC患者的三线治疗标准方案。在《CSCO结直肠癌诊疗指南(2023年版)》中[3],TAS-102与瑞戈非尼、呋喹替尼一同获得了转移性结直肠癌(mCRC)三线治疗的一级推荐。其中,TAS-102作为口服化疗药物具有独特作用机制,以口服方式给药更为便捷,方便患者长期用药使用。
近年来,基于TAS-102单药三线治疗的优异结果,其联合治疗策略也备受瞩目。SUNLIGHT研究[4]证实,TAS-102联合贝伐珠单抗较TAS-102单药取得了更好的中位OS(10.3个月 vs. 7.5个月,HR=0.61;95%CI,0.49~0.77;P<0.001),降低了39%的死亡风险。对于这些经过大量治疗存在耐药的mCRC患者来说,这是很好的结果。
mCRC后线治疗的目标是提高生活质量、延长生存时间,因此治疗的安全性也尤为关键。SUNLIGHT研究表明联合治疗组较单药组并未显著增加不良事件,安全性可管理。而对于不能耐受TAS-102+贝伐珠单抗标准治疗的患者,日本BiTS研究[5]显示双周方案可在不影响疗效的前提下,明显降低中性粒细胞减少症发生率,安全性更优。
TAS-102+贝伐珠单抗方案因其疗效和安全性兼顾的特点为不适合强烈治疗的mCRC患者及老年患者带来了新的希望。该方案已经在2023版指南中获得mCRC三线治疗的II级推荐,预计随着SUNLIGHT Ⅲ期临床研究正式发表,证据级别有望得到进一步提升。
[1] He J, et al. J Natl Cancer Cent.2022,2(1):1-9.
[2] Ciardiello, F, et al. CA A Cancer J Clin, 72: 372-401.
[3] CSCO 结直肠癌诊疗指南(2023版)
[4] Prager G W, Taieb J, Fakih M, et al. Trifluridine–tipiracil and bevacizumab in refractory metastatic colorectal cancer[J]. New England Journal of Medicine, 2023, 388(18): 1657-1667.
[5] Satake H, et al. Oncologist . 2020 Jul 14
排版编辑:肿瘤资讯-SY











 苏公网安备32059002004080号
苏公网安备32059002004080号


