
2024年3月21日,在HR阳性/HER2阴性(HR+/HER2-)早期乳腺癌辅助治疗领域中,备受瞩目的NATALEE研究全文正式刊登在《新英格兰医学杂志》(NEJM)![1] 这是迄今为止瑞波西利临床研究第5次荣登新英格兰医学杂志,前4次登榜均是在晚期乳腺癌一线治疗中取得重大突破,包括3项临床研究均取得的OS获益的结果。而本次登榜标志着瑞波西利在早期乳腺癌领域探索中再次突围。这些持续亮眼的研究成果也让大家看到瑞波西利真正的实力。
在CDK4/6抑制剂辅助治疗HR+/HER2-早期乳腺癌的研究中,PALLAS和PENELOPE-B研究均以失败告终,而NATALEE和monarchE研究探索成功。monarchE研究聚焦HR+/HER2-早期乳腺癌淋巴结阳性的高危人群,而NATALEE研究则在更广泛复发风险人群中也能取得显著疗效,开启CDK4/6抑制剂辅助治疗新时代。在此,【肿瘤资讯】特邀天津医科大学附属肿瘤医院 张瑾教授,谈一谈NATALEE研究设计和疗效数据有哪些亮点?哪些人群需要接受CDK4/6抑制剂强化辅助治疗?
天津医科大学肿瘤医院院长助理
中国天津乳腺癌防治研究中心常务副主任
天津医科大学肿瘤医院乳腺肿瘤三科科主任
国务院政府特殊津贴专家
第四届“国之名医”荣誉称号获得者
ESMO 乳腺癌专家委员会 委员
中国抗癌协会乳腺癌专业委员会 副主任委员
中国抗癌协会肿瘤多学科诊疗(MDT)专业委员会 副主任委员
中华医学会肿瘤学分会 委员
中华医学会肿瘤学分会恶性肿瘤早诊早治学组 副组长
中华医学会外科学分会乳腺癌学组 委员
中国医师协会外科医师分会乳腺外科专家工作组 副组长
中国医师协会肿瘤多学科诊疗(MDT)专家委员会 常委
天津市医学会肿瘤学分会 主任委员
天津市抗癌协会常务理事
天津市乳腺癌质控专家委员会主任
NATALEE研究独特的魅力:400mg瑞波西利辅助治疗3年,惠及人群更广
1) 临床研究人群:NATALEE研究覆盖更广泛的II-III期患者
NATALEE研究为一项全球多中心、随机对照的Ⅲ期临床试验,共5101例II-Ⅲ期HR+/HER2-早期乳腺癌患者,按照1:1随机分为两组,分别接受瑞波西利(400mg/天,给药3周+停药1周,持续3年)+内分泌治疗(来曲唑2.5 mg/天或阿那曲唑1mg/天,持续≥5年,男性和绝经前女性同时接受戈舍瑞林治疗)或单独内分泌治疗(图1)。
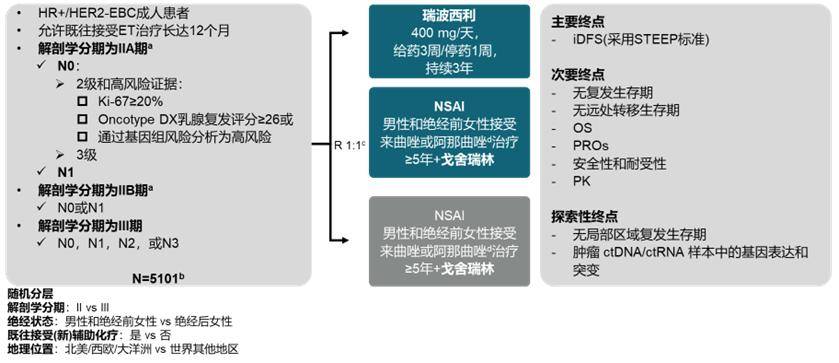
图1 NATALEE研究设计
NATALEE研究人群几乎包含了所有IIA到IIIC期,只有针对T2N0的患者,要求G3或G2(伴有Ki-67≥20%或基因组高风险);研究入组的N0患者占比28%;IIA期和IIB期患者各占比20%。
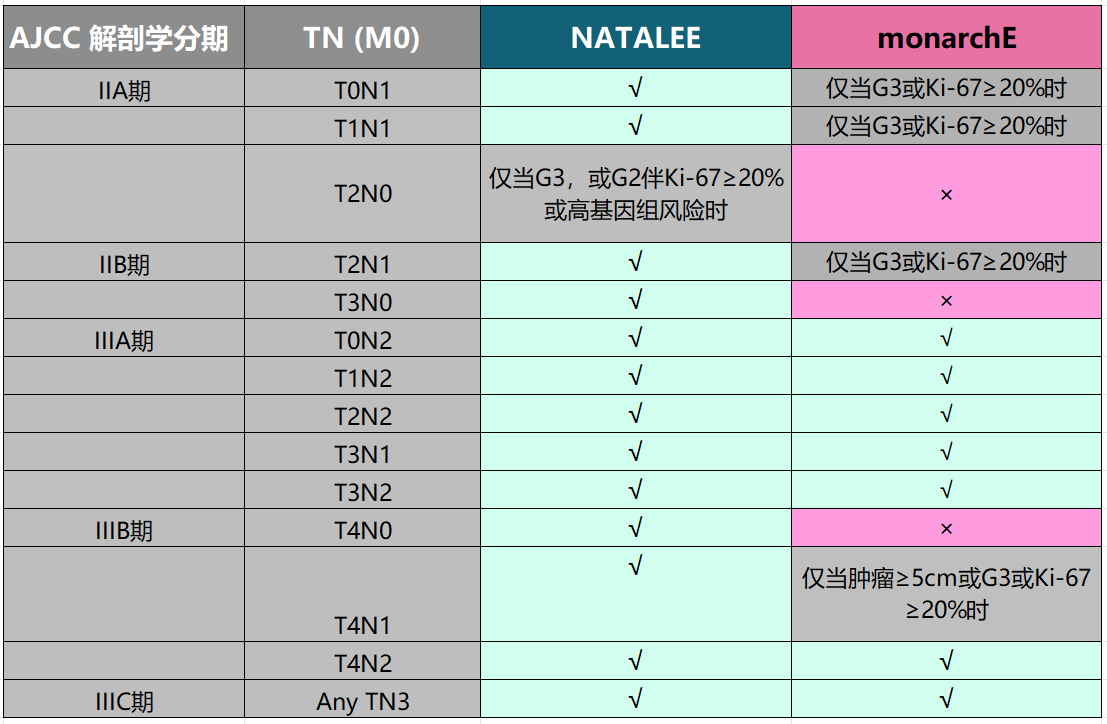
而monarchE研究[2]人群必须有病理腋窝淋巴结(ALN)阳性≥4枚,或腋窝淋巴结阳性1-3枚且至少具有以下一种高风险特征:原发肿瘤≥5cm;G3;Ki-67≥20%。没有纳入N0的患者。IIA期和IIB期患者分别占比约12%、14%,且只有N1人群符合G3或Ki-67≥20%时才允许入组; IIIA和IIIB期患者中,N2/3都能入组以外,N1人群需在肿瘤≥5 cm或G3或Ki-67≥20%时才允许入组(表1)。
因此,NATALEE研究既包含了monarchE研究人群,又纳入monarchE研究以外的人群(包括N0和N1全人群)
表1 NATALEE研究和monarchE研究入组人群比较
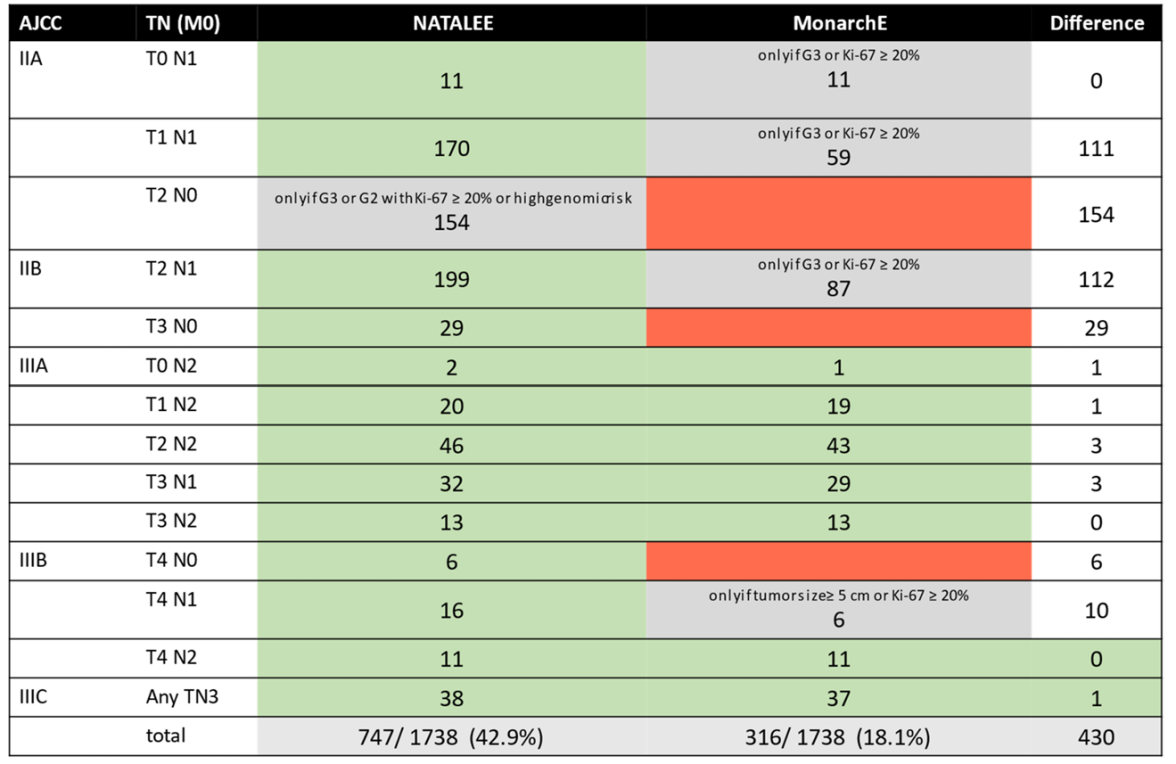
德国回顾性研究显示[3],2018年1月-2020年12月期间, 2家中心接受完整手术切除的1738名HR+/HER2-早期乳腺癌患者,43.0%符合NATALEE研究的纳入标准,18.1%符合monarchE研究的纳入标准;这说明真实临床中广泛的复发风险人群占比高,差异明显集中在T1N1,T2N0和T2N1患者中(表2)。
表2 德国真实世界中符合 NATALEE 和 monarchE研究患者重叠的详细信息
2)研究疗效:瑞波西利辅助疗效稳健获益
在主要终点方面,NATALEE研究的主要分析显示[4],瑞波西利+NSAI组的iDFS显著高于单独NSAI(90.4% vs 87.1%),绝对值差异为3.3%,患者复发风险降低25.2%(HR 0.748;95% CI,0.618~0.906;P=0.0014)(图2)。延长随访5.6个月[5],iDFS事件数从426增加至509,曲线尾部交叉消失,呈现逐渐分开的趋势。最终iDFS分析表明,瑞波西利+NSAI组iDFS持续稳健获益(90.7% vs 87.6%,HR 0.749,95% CI,0.628-0.892)(图2)。而且所有患者亚组(包括淋巴结阴性、II期、Ⅲ期等)均观察到一致的临床获益(图3)。
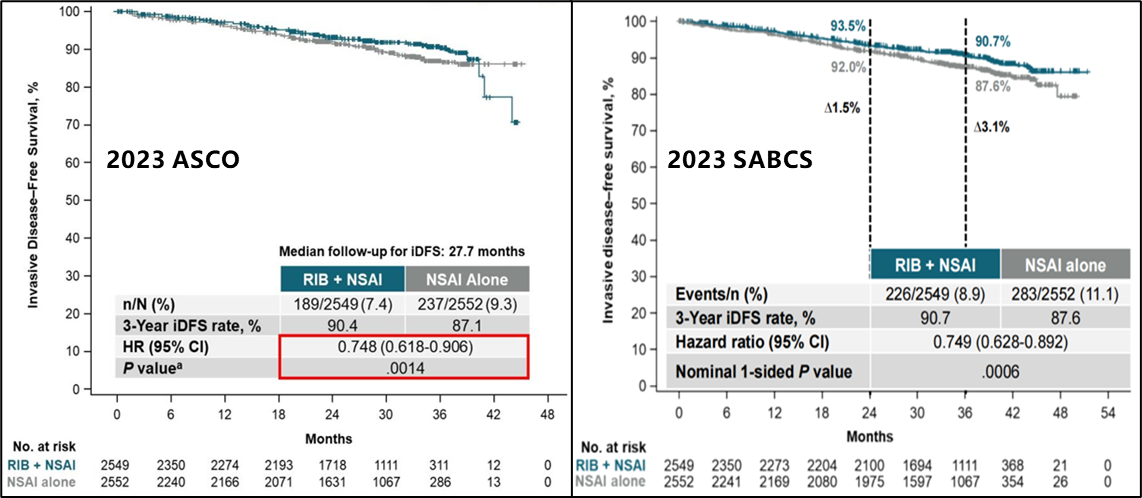
图2 NATALEE研究中ITT人群的3年iDFS数据(2023 ASCO 和2023 SABCS)
再看monarchE研究,在相似随访时间内(中位随访27.1月)[6],阿贝西利联合ET(AI或TAM)对比单纯ET,可将iDFS事件风险降低30%, 2年-iDFS率的绝对值获益2.7%,3年-iDFS率的绝对值获益5.4% (HR 0.70 , 95% CI 0.59-0.82) 。延长随访时间至54月时[7],阿贝西利在高危人群中持续稳健获益。但需要重点关注monarchE研究的2个问题:
1) monarchE研究有近31%患者接受TAM治疗,阿贝西利联合TAM对比疗效偏弱的TAM,拉高了ITT人群获益的疗效[8](2年-iDFS:TAM人群:HR 0.537,AI人群 HR 0.760)回看monarchE研究中阿贝西利联合AI治疗人群的风险比跟NATALEE研究相似(HR 0.748)。
2) monarchE研究的队列2人群[7],观察到阿贝西利具有OS损害趋势(HR1.078 ,0.465-2.501)。 这表明腋窝淋巴结阳性1-3枚患者,如果仅伴有Ki-67≥20%,目前的证据不支持阿贝西利辅助治疗,但NATALEE研究却可以弥补此类患者的临床需求,只要淋巴结阳性,均可从瑞波西利治疗中获益[4](图3)
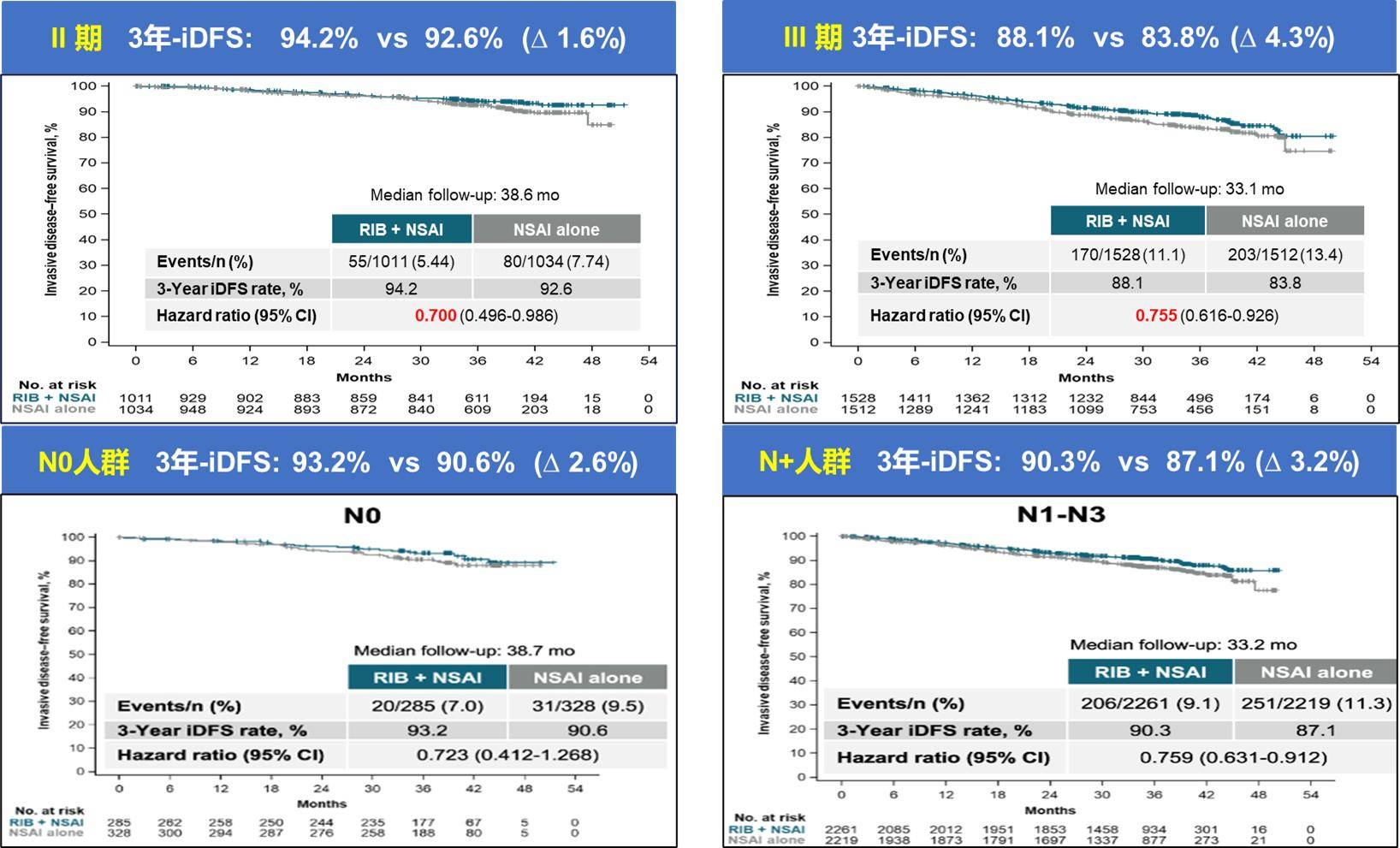
图3 NATALEE研究中TNM分期和淋巴结分层人群iDFS数据(2023 SABCS)
适合CDK4/6抑制剂强化辅助治疗人群在哪里?
一般认为,复发风险越高的患者越有必要接受CDK4/6抑制剂强化辅助治疗。例如高危人群便被认为应接受强化辅助治疗,基于2024年CACA-CBCS指南乳腺癌复发转移风险评估分层分类,目前公认的高危分层标准依然是≥4个阳性淋巴结;1~3个同时伴有高危因素(原发肿瘤≥5cm;G3;Ki-67≥20%)[9]。而在monarchE研究中,入组的早期乳腺癌患者也同样皆为高危人群。但是对于中危人群接受CDK4/6抑制剂强化辅助治疗的必要性,此前则存在着争议。英国一项对88项试验结果的荟萃分析曾强调了对于包括II期N0患者在内的中危患者进行强化辅助治疗的必要性[10]。这项荟萃分析对HR+乳腺癌患者5年辅助内分泌治疗停止后20年的复发风险进行了分析。结果提示,从第0年到第20年,每5年乳腺癌患者远处复发和死亡率与淋巴结状态密切相关(P<0.001),1-3个阳性淋巴结的女性20年远处复发风险为31%,而即便是N0的女性患者,20年的远处复发风险也可达到22%。因此,对于这部分患者,持续的监测和个性化的管理策略显得尤为重要。
而NATALEE研究入组的人群便包括了中危(II期及N0患者)和高危人群,其中N0患者伴高危因素患者的3年复发率近10%(图3)。IV期PreFace研究[11](NCT01908556)中在2009-2011年间纳入的3529例患者数据进行分析符合不同研究入组标准患者在未被CDK4/6抑制剂强化辅助治疗干预前提下的预后差异。915例患者符合NATALEE研究的入组标准: III期患者的预后最差,3年DFS率87%;IIA(T2N0伴G3)患者的3年DFS率只有91%, 差于IIA(N1)患者(93%),跟IIB患者(91%)相似;5年DFS率方面也观察到了类似的结果。这提示其实以N分期作为划分标准或许并不能清晰反映IIA期患者的预后,IIA(T2N0伴G3)患者较IIA(T0-1N1)患者的预后更差。因此,即便该患者为N0,如果临床伴有其他风险因素(如G3),其复发风险仍然不可小觑。这也再次使我们重新思考对于患者复发风险的划分不能静态地以TNM分期作为标准,还需考虑其他风险因素,如组织学分级等。
此前,由于我国人口基数大、地域差异明显以及医疗资源分布不均等特点,尚缺乏足够的针对中危复发风险乳腺癌患者的高质量流行病学数据,尤其是N0、II期患者在标准内分泌治疗后的复发风险。
但NATALEE研究的结果则给予我们新的启示:对于N0伴复发风险的人群和N+人群,行CDK4/6抑制剂的强化辅助治疗,可助力降低该类患者的复发风险,提高治愈率。未来重新定义早期乳腺癌的复发风险人群意义重大,更期待中国有更多这方面研究的开展,奠定更多高级别的循证医学证据,精准找出适合CDK4/6抑制剂强化辅助治疗的人群。
总结
瑞波西利已在HR+/HER2-晚期乳腺癌中稳占一线治疗地位,显著提高患者的总生存。而在早期辅助治疗探索中,瑞波西利探索再获成功,NATALEE研究刊登新英格兰医学期刊,夯实了CDK4/6抑制剂在HR+/HER2-早期乳腺癌辅助治疗价值,为广泛的II-III期乳腺癌患者提供新的防御武器,极大程度引起临床重新审视那些相对中危人群(II期或N0伴高危因素)的治疗需求。期待NATALEE研究更长的随访给我们一个有力且清晰的回答,为早期患者谋得更长的生存时间,实现治愈!
[1] Ribociclib plus Endocrine Therapy in Early Breast Cancer. N Engl J Med. 2024 Mar 21;390(12):1080-1091.
[2] Abemaciclib Combined With Endocrine Therapy for the Adjuvant Treatment of HR+, HER2-, Node-Positive, High-Risk, Early Breast Cancer (monarchE). J Clin Oncol. 2020;38:3987-3998
[3] The Clinical Relevance of the NATALEE Study: Application of the NATALEE Criteria to a Real-World Cohort from Two Large German Breast Cancer Centers. Int J Mol Sci. 2023 Nov 15;24(22):16366.
[4] Ribociclib and endocrine therapy as adjuvant treatment in patients with HR+/HER2− early breast cancer: Primary results from the phase III NATALEE trial. 2023 ASCO. LBA 500..
[5] Ribociclib (RIB) + nonsteroidal aromatase inhibitor (NSAI) as adjuvant treatment inpatients with HR+/HER2− early breast cancer: final invasive disease–free survival (iDFS)analysis from the NATALEE trial. 2023 SABCS. GS03-03.
[6] Adjuvant abemaciclib combined with endocrine therapy for high-risk early breast cancer: updated efficacy and Ki-67 analysis from the monarchE study. Ann Oncol. 2021 Dec;32(12):1571-1581. J Clin Oncol. 2024 Mar 20;42(9):987-993.
[7] Adjuvant Abemaciclib Plus Endocrine Therapy for Hormone Receptor-Positive, Human Epidermal Growth Factor Receptor 2-Negative, High-Risk Early Breast Cancer: Results From a Preplanned monarchE Overall Survival Interim Analysis, Including 5-Year Efficacy Outcomes.
[8] Agency EM. Verzenios EPAR. Assessment report variation. https://www.ema.europa.eu/en/documents/variation-report/verzenios-h-c-004302-ii-0013-epar-assessment-report-variation_en.pdf. 2022.
[9] 中国抗癌协会乳腺癌专业委员会临床应用指南(2024年版).
[10] 20-Year Risks of Breast-Cancer Recurrence after Stopping Endocrine Therapy at 5 Years. N Engl J Med. 2017 Nov 9;377(19):1836-1846.
[11] Prognostic Impact of Selection Criteria of Current Adjuvant Endocrine Therapy Trials Natalee and Monarche in Postmenopausal Hrpos/Her2neg Breast Cancer Patients Treated with Upfront Letrozole[J].
排版编辑:Winnie











 苏公网安备32059002004080号
苏公网安备32059002004080号


