2024年3月9日,国际著名期刊Nature Communications发表了由多位亚洲学者合作完成的PEONY研究的最终分析报告[1]。该研究由复旦大学附属肿瘤医院的邵志敏教授和黄亮教授牵头,联合国内与亚太地区共23家医学中心,首次对亚洲HER2阳性早期或局部晚期乳腺癌患者在接受新辅助和辅助治疗时,全程使用帕妥珠单抗与安慰剂+曲妥珠单抗+化疗方案的有效性和安全性进行了比较。结果显示,帕妥珠单抗组在5年无事件生存期(EFS)和无病生存期(DFS)上表现出显著提高,且安全性良好。研究进一步证实了“曲帕双靶”在HER2阳性乳腺癌治疗中的积极作用。【肿瘤资讯】特对精华予以整理,以飨读者。

HER2双重阻断策略在新辅助和辅助治疗中的应用
HER2靶向治疗显著改善了HER2阳性早期乳腺癌患者的预后,尤其是曲妥珠单抗的使用提高了pCR率和生存率[2,3,4]。然而,仍有多数患者未达到pCR[2,5],且约三分之一在3年内复发[5]。帕妥珠单抗与曲妥珠单抗的联合治疗在APHINITY研究中显示能显著改善DFS[6,7,8],且未增加心脏不良事件[6,9,10]。
NeoSphere研究[11]证实了新辅助治疗方案中加入帕妥珠单抗能提高pCR率,尽管长期生存数据存在较大置信区间[12]。PEONY试验作为III期研究,主要结局先前已有报道[13],是首个验证了在亚洲患者中加入帕妥珠单抗能显著提高总体(乳房+淋巴结)病理完全缓解率(tpCR),与NeoSphere研究结果相似[11,13]。
本次报告PEONY试验的长期疗效(3年和5年)最终分析,评估了包括辅助治疗期、总体治疗期和免治疗随访期的数据,以及EFS、DFS、总生存期(OS)和安全性等预先指定的次要终点。
研究方法
PEONY试验共纳入329名女性患者,2:1随机分配至帕妥珠单抗组(219人)和安慰剂组(110人),均接受新辅助和辅助治疗。治疗方案包括帕妥珠单抗或安慰剂与曲妥珠单抗和多西他赛的联合使用,随后是5-氟尿嘧啶、表柔比星和环磷酰胺的辅助化疗。
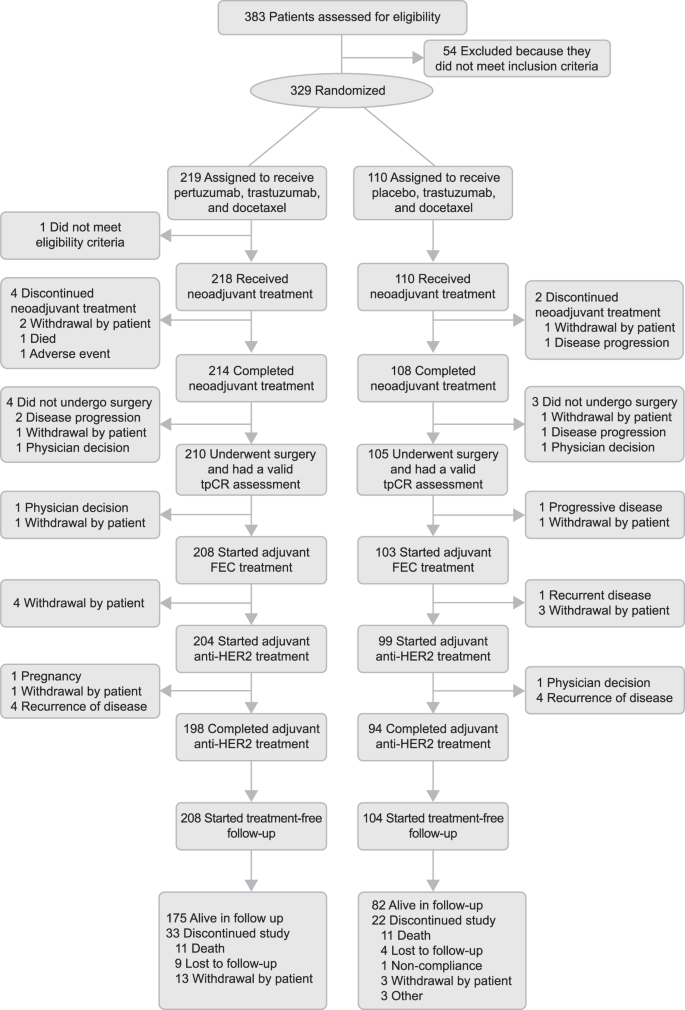
研究结果:帕妥珠单抗显著改5年EFS与DFS
入组患者基线特征
两组患者的基线特征总体平衡,包括年龄、疾病阶段、激素受体状态等。170名(51.7%)患者疾病为激素受体阳性,100名(30.4%)属于局部晚期。保乳手术率在帕妥珠单抗组为57例(26.0%),安慰剂组为35例(31.8%)。

5年EFS
经过中位时间为62.9个月的随访,帕妥珠单抗组的3年EFS率为88.9%,而安慰剂组为79.7%,显示出9.2%的改善(95% CI 0.29-18.1; p = 0.043)。5年EFS率分别为84.8%和73.7%,帕妥珠单抗组有11.1%的改善(95% CI 1.2–21.0; p = 0.027),风险比(HR)为0.53(95% CI 0.32–0.89)。(图1)
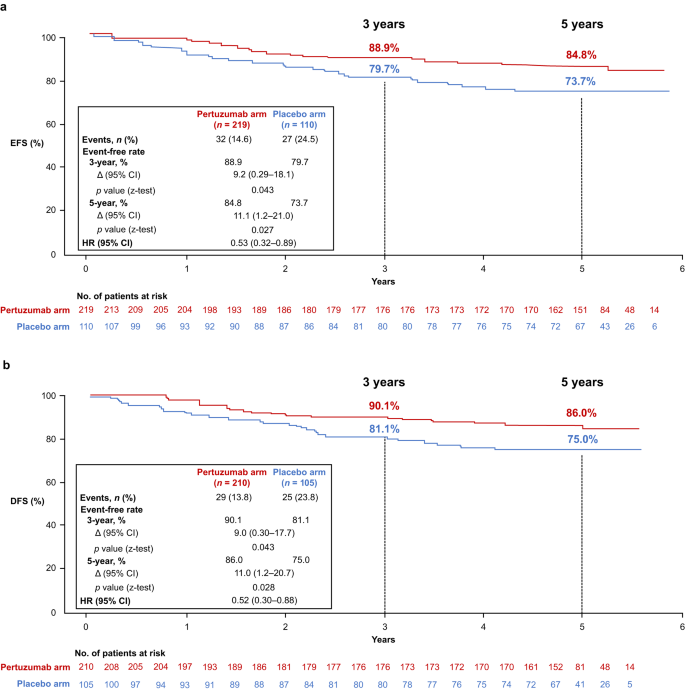
图1 长期疗效终点EFS和DFS的Kaplan-Meier曲线
5年DFS
对于DFS,帕妥珠单抗组的3年DFS率为90.1%,安慰剂组为81.1%,改善了9.0%(95% CI 0.30–17.7; p = 0.043)。5年DFS率分别为86.0%vs 75.0%,提高11.0%,95%置信区间:1.2~20.7,P=0.028;HR 0.52,95%置信区间:0.30~0.88。(图1)
两组的OS事件较少,但帕妥珠单抗组有改善趋势,3年OS率分别为97.0%和91.0%,5年OS率分别为93.9%和90.0%(提高3.9%,95%置信区间:2.9~10.7,P=0.262;HR 0.53,95%置信区间:0.23~1.19)。
亚组分析:未tPCR患者也可从帕妥珠单抗治疗获益
探索性亚组分析揭示了帕妥珠单抗在不同患者群体中相对于安慰剂的疗效优势。这些亚组基于疾病阶段、激素受体(ER和PgR)状态和生物标志物水平进行划分。
分析发现,帕妥珠单抗在提高EFS和DFS方面对所有预设亚组均有益处(图2),尤其在激素受体阴性和淋巴结阳性的高风险患者中效果更为显著。
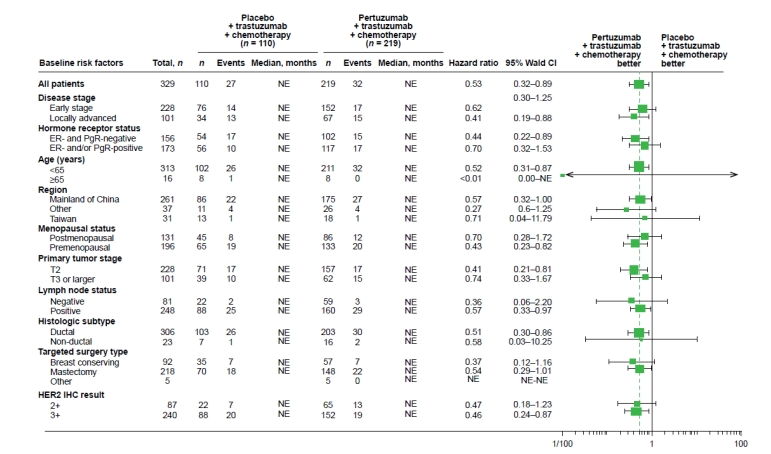
图2 ITT人群EFS亚组分析
此外,无论是否达到tpCR,帕妥珠单抗组的DFS率均优于安慰剂组(图3-4),特别是在未达到tpCR的患者中,帕妥珠单抗组显示出更明显的DFS改善:3年DFS率为88.3%,安慰剂组为76.8%;5年DFS率为82.1%,安慰剂组为68.8%(图3)。
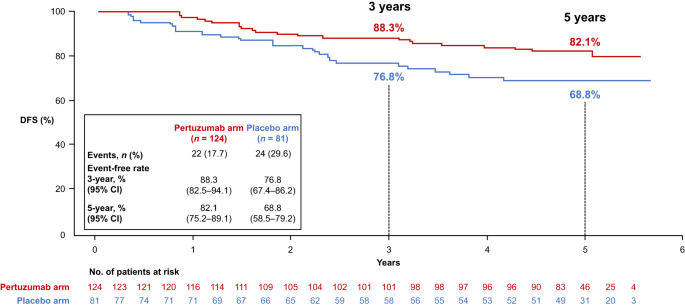
图3 具残留病灶患者DFS亚组分析
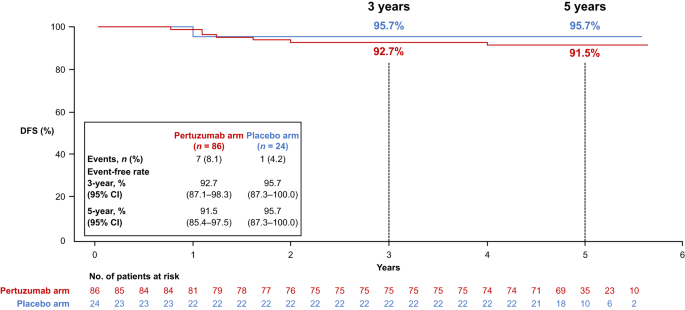
图4 tpCR人群DFS亚组分析
预先指定的生物标志物分析发现,未检测到PIK3CA突变的患者比检测到PIK3CA突变的患者具有更好的EFS和DFS率(图5)。HER2免疫组化(IHC)亚组分析也显示,HER2 IHC 3+亚组相比于HER2 IHC 1+/2+亚组有更长的EFS和DFS。
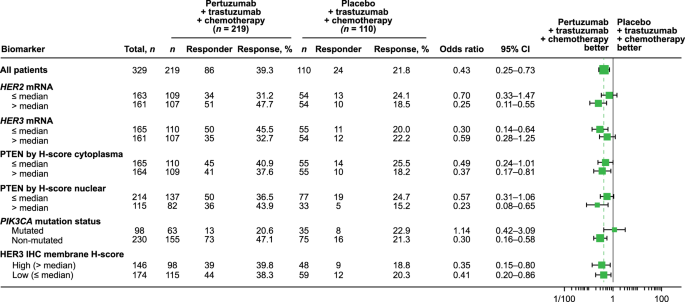
图5 ITT人群中生物标志物亚组tpCR分析结果
安全性数据与帕妥珠单抗已知的安全性概况一致,两组之间的不良事件发生率大致相当,但帕妥珠单抗组腹泻的发生率较高(40.8% vs 17.3%)。
PEONY试验临床意义与局限性
PEONY试验通过长期随访证实了帕妥珠单抗在提高HER2阳性乳腺癌患者5年EFS和DFS方面的显著效果,巩固了其在临床治疗中的地位,并确认了其良好的安全性。探索性亚组分析推动了精准医疗的进展,而试验的国际多中心特性增强了结果的普适性。
尽管如此,试验在OS评估上的非专门设计、未包含T-DM1的局限、缺乏长期心脏安全性监测、统计效能限制以及可能与现行治疗标准有偏差的研究设计,指出了未来研究需深入的方向,尤其是在亚组样本量方面。
1. Huang, L., Pang, D., Yang, H. et al. Neoadjuvant–adjuvant Pertuzumab in HER2-positive early breast cancer: final analysis of the randomized phase III PEONY trial. Nat Commun 15, 2153 (2024). https://doi.org/10.1038/s41467-024-45591-7
2. Gianni, L. et al. Neoadjuvant chemotherapy with trastuzumab followed by adjuvant trastuzumab versus neoadjuvant chemotherapy alone, in patients with HER2-positive locally advanced breast cancer (the NOAH trial): A randomised controlled superiority trial with a parallel HER2-negative cohort. Lancet 375, 377–384 (2010).
3. Cameron, D. et al. 11 years’ follow-up of trastuzumab after adjuvant chemotherapy in HER2-positive early breast cancer: final analysis of the HERceptin Adjuvant (HERA) trial. Lancet 389, 1195–1205 (2017).
4. Slamon, D. et al. Adjuvant trastuzumab in HER2-positive breast cancer. N. Engl. J. Med. 365, 1273–1283 (2011).
5. Untch, M. et al. Pathologic complete response after neoadjuvant chemotherapy plus trastuzumab predicts favorable survival in human epidermal growth factor receptor 2-overexpressing breast cancer: results from the TECHNO trial of the AGO and GBG study groups. J. Clin. Oncol. 29, 3351–3357 (2011).
6. von Minckwitz, G. et al. Adjuvant Pertuzumab and trastuzumab in early HER2-positive breast cancer. N. Engl. J. Med. 377, 122–131 (2017).
7. Piccart, M. et al. Adjuvant Pertuzumab and trastuzumab in early HER2-positive breast cancer in the APHINITY trial: 6 years’ follow up. J. Clin. Oncol. 39, 1448–1457 (2021).
8. Loibl, S. et al. Adjuvant Pertuzumab and trastuzumab in patients with early HER-2 positive breast cancer in APHINITY: 8.4 years’ follow-up. Ann. Oncol. 33, VP6–2022 (2022).
9. Swain, S. M. et al. Cardiac tolerability of Pertuzumab plus trastuzumab plus docetaxel in patients with HER2-positive metastatic breast cancer in CLEOPATRA: a randomized, double-blind, placebo-controlled phase III study. Oncologist 18, 257–264 (2013).
10. Swain, S. M. et al. Pertuzumab, trastuzumab, and docetaxel for HER2-positive metastatic breast cancer (CLEOPATRA): end-of-study results from a double-blind, randomised, placebo-controlled, phase 3 study. Lancet Oncol. 21, 519–530 (2020).
11. Gianni, L. et al. Efficacy and safety of neoadjuvant Pertuzumab and trastuzumab in women with locally advanced, inflammatory, or early HER2-positive breast cancer (NeoSphere): a randomised multicentre, open-label, phase 2 trial. Lancet Oncol. 13, 25–32 (2012).
12. Gianni, L. et al. 5-year analysis of neoadjuvant Pertuzumab and trastuzumab in patients with locally advanced, inflammatory, or early-stage HER2-positive breast cancer (NeoSphere): a multi centre, open-label, phase 2 randomised trial. Lancet Oncol. 17, 791–800 (2016).
13. Shao, Z. et al. Efficacy, safety, and tolerability of Pertuzumab, trastuzumab, and docetaxel for patients with early or locally advanced ERBB2-positive breast cancer in asia: the PEONY phase 3 randomized clinical trial. JAMA Oncol. 6, e193692 (2020).
排版编辑:肿瘤资讯-Kelly











 苏公网安备32059002004080号
苏公网安备32059002004080号


