在诊断为间变性淋巴瘤激酶(ALK)突变阳性的非小细胞肺癌(NSCLC)患者中,阿来替尼的中枢神经系统渗透性显著优于克唑替尼。Thoracic Research and Practice发布的一篇文献,探索了阿来替尼在预后特征不佳的ALK阳性NSCLC患者中的疗效及其在一线治疗中的地位,并报告了真实世界数据[1]。
研究目的
转移性NSCLC患者的生存率非常低。然而,随着ALK基因染色体重排的ALK突变阳性患者靶向治疗的发展,患者的生存期已显著延长。NSCLC患者ALK突变率约3%-7%,约20%-30%的ALK阳性NSCLC患者在诊断时和50%的患者在病程中观察到脑转移。[2] 脑转移的存在也与高发病率和死亡率密切相关。通过靶向治疗,这一经常发生脑转移的患者群体的总生存期(OS)有所延长。
克唑替尼是首个ALK受体抑制剂,由于其优于标准化疗,已被成功使用了很长时间。然而,由于中枢神经系统(CNS)渗透性不佳,在治疗过程中常见脑转移。[3] 因此人们开始寻找新的治疗方法。
阿来替尼是第二代酪氨酸激酶抑制剂(TKI),由于其亲脂性,具有非常好的CNS渗透性。因此,它可以预防脑转移的发生和现有转移瘤的进展,提供比克唑替尼更长的无进展生存期(PFS),毒性更低。[4]由于缺乏维持血脑屏障中血流的p-糖蛋白底物,它可以有效穿透CNS。[5]
本研究旨在评价阿来替尼和克唑替尼在真实世界中作为一线治疗对生存和脑转移的影响。
材料和方法
研究者对2016年6月至2021年4月期间在本院门诊确诊的38例ALK阳性NSCLC患者的数据进行了分析,这些患者均接受了ALK TKI作为一线治疗。对这些患者未接受任何化疗方案的情况进行了回顾性分析。未在本院接受随访和治疗的患者未纳入研究。
研究记录了患者的人口统计学特征、分期、转移状态、治疗方法、PFS和OS。根据患者在一线治疗中使用克唑替尼还是阿来替尼以及在病情进展时是否接受二线治疗进行分类。对未进展且存活至2021年4月30日的患者计算PFS和OS,并记录所有数据。
研究结果
38例接受ALK TKI作为一线治疗的ALK阳性NSCLC患者入选本研究。患者的平均年龄为56.0±11.5岁,其中24例(63.2%)为男性,8例(21.1%)无吸烟史。所有患者均为腺癌类型,且均处于4期。最常见的转移部位分别为胸膜15例(39.5%)、骨11例(28.9%)、对侧肺10例(26.3%)。 入院时7例(18.4%)患者和治疗期间6例(15.8%)患者检测到脑转移。各19例患者分别接受克唑替尼或阿来替尼作为一线治疗。对于克唑替尼治疗后疾病进展的8例患者,阿来替尼作为二线治疗。
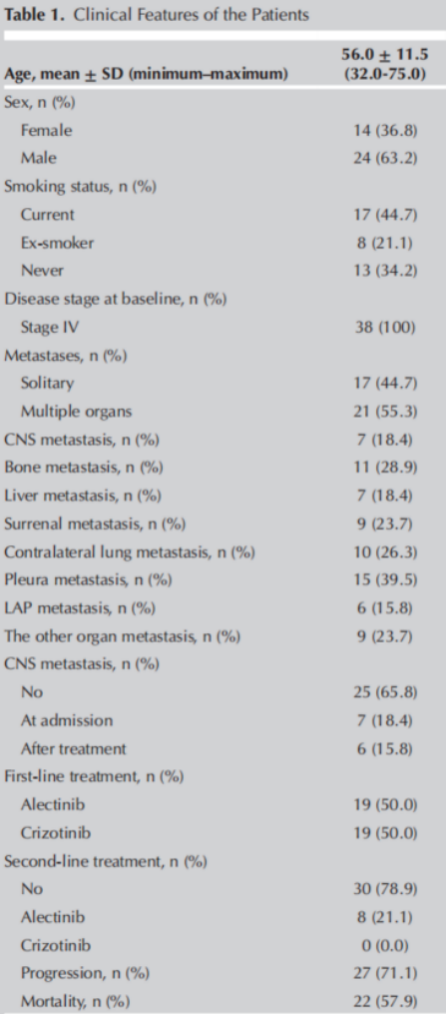 表1.患者的临床特征
表1.患者的临床特征
阿来替尼治疗组有14例多发性转移患者,而克唑替尼治疗组有7例(P=0.022)。在阿来替尼治疗前,有6例患者发生脑转移;在治疗期间未观察到新的脑转移。克唑替尼治疗前仅有1例患者发生脑转移;治疗期间有6例患者发生脑转移(P=0.006)。
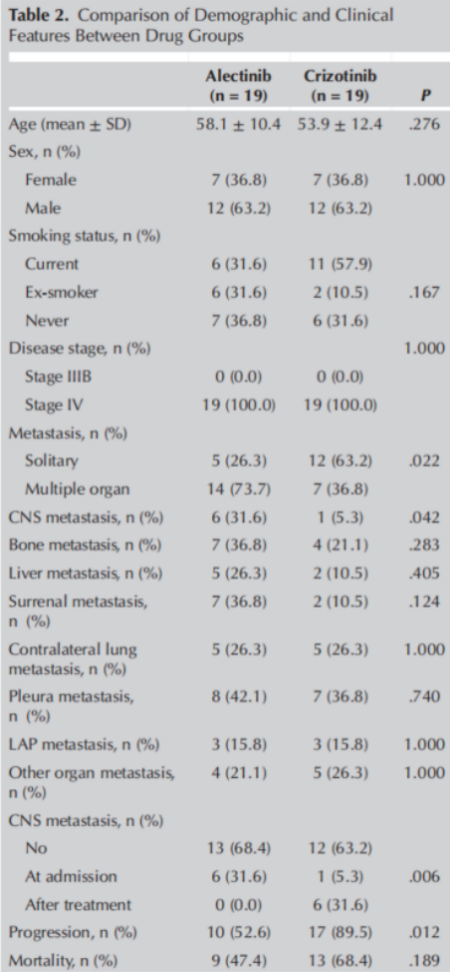 表2.药物组间人口统计学和临床特征的比较
表2.药物组间人口统计学和临床特征的比较
在阿来替尼组10例(52.6%)患者和克唑替尼组17例(89.5%)患者中观察到进展(P=0.012)。
尽管阿来替尼组的PFS为23.5±4.2个月,OS为24.6±4.1个月,克唑替尼组的PFS为17.1±4.8个月,OS为26.5±6.1个月,但PFS和OS均无统计学意义(分别为P=0.187,P=0.383)(表3)。
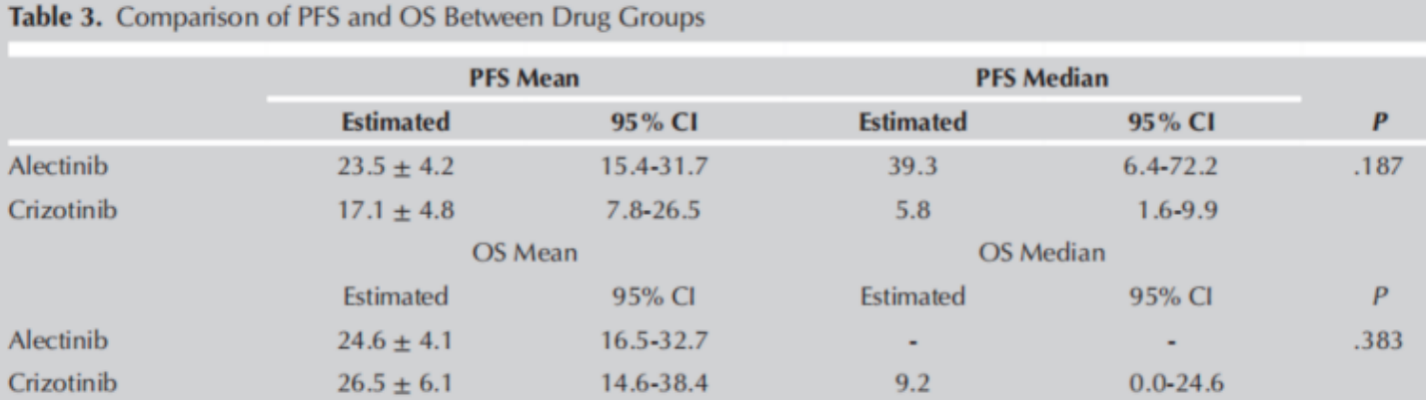 表3. 药物组间PFS和OS的比较
表3. 药物组间PFS和OS的比较
在进展后接受阿来替尼二线治疗的8例患者中,平均OS为18.2±7.0个月,而无法接受阿来替尼治疗的12例患者的平均OS为4.0±2.0个月,显著更短(P=0.004)(表4)。
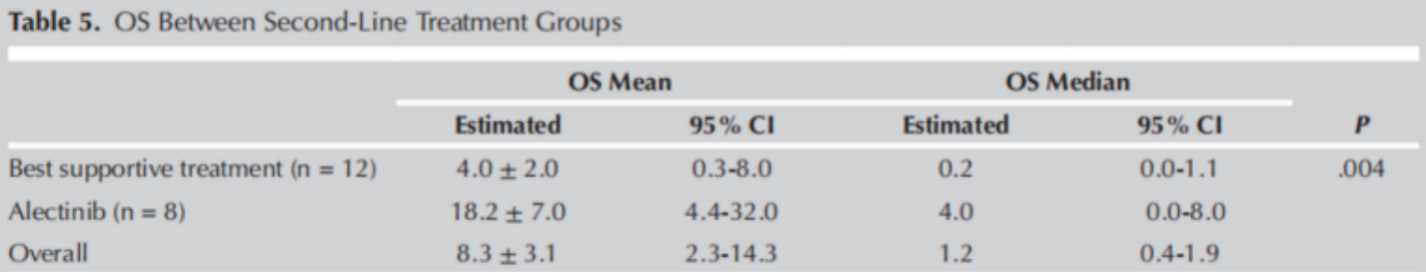 表4. 二线治疗组间的OS
表4. 二线治疗组间的OS
讨论
许多研究表明,用于ALK阳性NSCLC患者的TKIs优于化疗,而阿来替尼在PFS和OS方面均优于克唑替尼。[6] 在我们的患者群体中,我们试图回答迄今为止用于一线治疗的阿来替尼是否优于克唑替尼,以及阿来替尼是否对脑转移有效,更重要的是是否能预防脑转移的发生。
我们回顾性分析了在我院所接受诊断、治疗和随访的38名ALK阳性NSCLC患者的数据。阿来替尼组和克唑替尼组刚好都有19名患者。阿来替尼组患者的平均年龄更大,转移率更高(P=0.022),治疗前出现脑转移的患者更多(P=0.006)。然而,阿来替尼组有10例(52.6%)患者出现病情进展,克唑替尼组有17例(89.5%)患者出现病情进展(P=0.012)。这表明,与克唑替尼相比,老年组(脑转移灶和多发转移灶较多)患者使用阿来替尼能更成功地控制病情。本研究结果与Alex研究结果一致;在阿来替尼和克唑替尼用药时间相似的情况下,阿来替尼组和克唑替尼组病情进展或死亡发生率分别为41%和68%。
克唑替尼组只有1名患者在治疗前出现脑转移,6名患者在治疗期间出现脑转移,而阿来替尼组有6名患者在治疗前出现脑转移;在治疗期间没有发现新的脑转移。)这一差异表明,阿来替尼是一种亲脂性药物,很容易穿过中枢神经系统屏障,从而阻止了中枢神经系统新转移灶的形成。我们的数据显示,阿来替尼在脑转移方面具有优势,与Alex评估中枢神经系统疗效的研究相似[5]。
阿来替尼组的PFS为(23.5±4.2)个月,克唑替尼组的PFS为(17.1±4.8)个月。尽管阿来替尼提供了6个月左右的更长的PFS,但这一时间并不具有统计学意义。不过,我们仍然认为不应低估这段时间,可能会以患者数量的增加为标志。
这也与以下事实有关:尽管第一批患者接受了克唑替尼治疗,但我们还是给最后一批患者提供了阿来替尼,因为阿来替尼获得政府报销的时间太晚,所以克唑替尼的数据才最终确定。然而,阿来替尼的数据需要更多时间才能最终确定。未来几年,我们的阿来替尼真实数据将更加准确。Khan等对涉及3297例患者的12 项研究进行的荟萃分析表明,阿来替尼和其他新一代ALK抑制剂的PFS明显优于克唑替尼。[7]
在本研究中,阿来替尼组的OS为24.6±4.1个月,克唑替尼组为26.5±6.1个月。Mok等[8]更新了ALEX研究的OS数据,阿来替尼的平均OS为48.2个月,而克唑替尼为23.3个月,这使得阿来替尼在有无中枢神经系统转移的患者中意义重大。此外,34.9%的阿来替尼组患者和8.6%的克唑替尼组患者仍在接受治疗。该研究与本研究不同之处在于,使用克唑替尼治疗后病情恶化的患者没有接受阿来替尼治疗。[8] 虽然没有统计学意义,但本研究认为,阿来替尼组患者生存率低的原因是脑转移等预后不良的患者较多。此外,克唑替尼组约有一半患者在病情进展后接受了阿来替尼治疗。
在本研究中,38名患者中有10人(52.6%)在使用阿来替尼治疗期间病情恶化,17人(89.5%)在使用克唑替尼治疗期间病情恶化(P=0.012)。在使用克唑替尼进行二线治疗的17名进展患者中,有8名患者可以接受阿来替尼治疗。其余19名患者没有接受任何治疗。进展后接受阿来替尼治疗的患者的总生存期为(18.2±7.0)个月,而未接受任何治疗的患者的总生存期为(4.0±2.0)个月(P=0.004)。换句话说,阿来替尼在克唑替尼耐药的患者中效果很好。那么,我们可能会想,把阿来替尼留给对克唑替尼产生耐药性的患者进行二线治疗是否更合理呢?然而,我们认为不应忘记那9位因表现受损而未接受任何治疗的患者。Alex临床研究者Peters等的研究发现,阿来替尼的12个月无进展率为68.4%,克唑替尼为48.7%,这支持了本研究结果。[9] 在ALUR研究[10]中,克唑替尼治疗进展的患者在二线治疗中接受阿来替尼或化疗。与化疗组相比,阿来替尼组在颅内转移和颅外转移方面的PFS均明显优于化疗组。
综上,我们发现在ALK阳性NSCLC患者中,阿来替尼在一线治疗预后较差、有或无脑转移的患者中优于克唑替尼。今后,随着患者人数的增加,以及接受阿来替尼治疗的患者的真实数据的出现,这项研究将更有意义。
结论
阿来替尼组的进展率低于克唑替尼组患者,即使阿来替尼组中多发性转移和脑转移的患者更多。
1. Katgı N, Çimen P, Akyol M, Gürsoy P, Agüloğlu N. Comparison of Alectinib/Crizotinib Data in First-Line Therapy in Patients with Anaplastic LymphomakinasePositive Nonsmall Cell Lung Carcinoma with Poor Prognostic Features for Alectinib. Thorac Res Pract. 2023 Jul;24(4):180-185. doi: 10.5152/ThoracResPract.2023.22200.
2. Xia B, Nagasaka M, Zhu VW, Ou SI, Soo RA. How to select the best up front therapy for metastatic disease? Focus on ALKrearranged non-small cell lung cancer (NSCLC). Transl Lung Cancer Res. 2020;9(6):2521-2534.
3. Johung KL, Yeh N, Desai NB, et al. Extended survival and prognostic factors for patients with ALK-rearranged non-small cell lung cancer and brain metastasis. J Clin Oncol. 2016;34(2):123-129.
4. Sivignon M, Monnier R, Tehard B, Roze S. Cost-effectiveness of alectinib compared to crizotinib for the treatment of first-line ALK+advanced non-small cell lung cancer in France. PLOS ONE. 2020;15(1):e0226196.
5. Gadgeel S, Peters S, Mok T, et al. Alectinib versus crizotinib in treatment-naïve anaplastic lymphomakinase-positive (ALK +) non-small cell lung cancer: CNS efficacy results from the ALEX study. Ann Oncol. 2018;29(11):2214-2222.
6. Elliott J, Bai Z, Hsieh SC, et al. ALK inhibitors for non-small cell lung cancer: A systematic review and network meta-analysis. PLOS ONE. 2020;15(2):e0229179.
7. Khan M, Lin J, Liao G, et al. ALK Inhibitors in the treatment of ALK-positive NSCLC. Front Oncol. 2018;8:557.
8. Mok T, Camidge DR, Gadgeel SM, et al. Up dated overall survival and final progression free survival data for patients with treatment-naive advanced ALK–positive non-small cell lung cancer in the ALEX study. Ann Oncol. 202031(8):1056-1064.
9. Peters S, Camidge DR, Shaw AT, et al. Alectinib versus crizotinib in untreated ALK-positive non–small cell lung cancer. N Engl J Med. 2017;377(9):829-838.
10. Novello S, Mazières J, Oh IJ, et al. Alectinib versus chemotherapy in crizotinib pretreated anaplastic lymphomakinase (ALK) –positive non-small cell lung cancer: results from the phase III ALUR study. Ann Oncol. 2018;29(6):1409-1416.
排版编辑:肿瘤资讯-olivia











 苏公网安备32059002004080号
苏公网安备32059002004080号


