抗体偶联药物(ADC)是一类兼具靶向特异性和化疗药物高活性的新型药物,其对复发/转移性乳腺癌展现出优越的治疗效果。三阴性乳腺癌(TNBC)是一种高度异质性和侵袭性的恶性肿瘤,治疗手段相对匮乏,预后较差,临床上亟待寻找可用于精准治疗及提高预后的新靶点[1]。人滋养层细胞表面抗原 2(Trop2)在TNBC中高表达,Trop-2 ADC戈沙妥珠单抗(SG;商品名:拓达维®)凭借着优异的疗效,成为首个获批用于晚期TNBC的ADC药物,开启了我国晚期TNBC的精准治疗新时代。尽管ADC药物疗效卓越、整体安全性良好,但临床医生仍需积极学习药物相关不良反应管理,这样才能充分运用好为这把新兴利器,为患者带来最大化获益。
医学博士,博士生导师
中山大学附属第一医院乳腺外科行政主任
中国医药教育协会乳腺疾病专委会常务委员
中国临床肿瘤协会乳腺癌专委会委员
中国医师协会乳腺外科医师委员会委员
中国医师协会肿瘤分会乳腺专委会委员
广东省健康管理学会乳腺病专业委员会主任委员
广东省抗癌协会乳腺癌专业委员会副主任委员
广东省女医师协会乳腺癌防治专家委员会副主任委员
广东省健康管理学会肿瘤专业委员会委员
曾分别于美国Emory大学和美国MD Anderson癌症中心进修。承担多项国家、省市级科研项目,在« Cancer Res»、« Int J Cancer »、« Cancer Letters»、« Clin Chem Lab Med»、« Proteomics»、«中华医学杂志»、«中华外科杂志»、«中华普通外科杂志»等专业期刊发表论文80余篇,参加多部专著编写。
不同ADC不良事件谱存在差异,不可一概而论
近年来,ADC药物在乳腺癌治疗领域取得了蓬勃进展。HER2是探索最为广泛的靶点,其代表药物德曲妥珠单抗(T-DXd)已获批用于HER2阳性、HER2低表达晚期乳腺癌的二线及以上治疗,恩美曲妥珠单抗(T-DM1)获批用于早期HER2阳性乳腺癌的强化辅助治疗或晚期HER2阳性乳腺癌的二线及其后治疗。诸如SG、Dato-DXd、SKB264等以Trop-2为靶点的ADC药物也取得了不少亮眼成果,其中SG已在国内外获批用于治疗既往接受过至少两次系统治疗(其中至少一次用于转移性疾病治疗)的不可切除的局部晚期或转移性三阴性乳腺癌(mTNBC)成人患者。
鉴于ADC不良反应涉及抗体、细胞毒性制剂、连接子以及偶联过程等多个环节,因此,ADC不良反应安全谱也存在差异[2],不可一概而论——比如,可见于以HER2为靶点的ADC药物T-DM1或T-DXd的心脏毒性则与其结构中共同含有的曲妥珠单抗的靶向、脱瘤效应有关[3]。除此之外,T-DM1还有肝毒性、血液毒性、恶心呕吐等AE,其中≥3级AE主要为血小板减少、肝毒性,FDA曾对其可能导致的肝毒性、心脏毒性和胚胎-胎儿毒性均予以黑框警告。T-DXd常见AE也以恶心呕吐、腹泻、血液毒性为主,≥3级AE以中性粒细胞减少最为常见,FDA也曾对其可能导致的间质性肺病(ILD)和胚胎-胎儿毒性予以黑框警告。而以Trop-2为靶点的ADC,如SG,其常见AE为血液毒性、恶心呕吐、腹泻等,其中≥3级AE以中性粒细胞减少、腹泻为主,FDA也曾对此予以黑框警告。
SG总体安全可控,为晚期TNBC患者保驾护航
SG是全球首款获批用于晚期TNBC的Trop-2 ADC药物,开启了我国TNBC靶向治疗的先河。其安全性数据从I/II期IMMU-132-01篮子试验到近期于2023 ESMO大会公布的真实世界研究可见一斑。
I/II期IMMU-132-01篮子试验初步验证了SG在mTNBC中的疗效与安全性[6],基于此,FDA加速批准SG治疗mTNBC。后续的确证性III期ASCENT研究[7]进一步结果表明,SG整体安全性良好,AE可控可管理。该研究中SG治疗的主要AE为中性粒细胞减少症和腹泻,≥3级AE发生率低。且SG相关≥3级中性粒细胞减少发生晚、消退快,较少引起发热性中性粒细胞减少,中性粒细胞减少并未导致相关停药。SG相关腹泻主要为轻中度,无4级腹泻发生,也未发生腹泻相关停药。与化疗相比,SG相关剂量降低和停药率低,无治疗相关死亡。亚组分析发现,老年患者(≥65岁)的AE与研究总体人群所表现的安全性特征一致。
EVER-132-001研究[8]是SG在国内获批mTNBC适应症的主要研究,其安全性数据与既往研究一致,AE整体可防可控。这提示SG在中国患者中具有和全球人群一致的安全性,为我国临床医生用药增添了信心。
而SG对于具有更差预后特征的多元化人群的安全性也在今年ESMO大会公布的一项美国真实世界研究[9]中得到了验证。该研究中SG展现出了与其他临床研究一致的AE特征,患者整体耐受性良好,且研究显示,粒细胞集落刺激因子(G-CSF)的使用对于SG疗效无影响,为SG的临床用药安全性再添新证。
知行合一,重视ADC不良反应预防和管理
尽管ADC总体上安全性良好,但临床医生用药期间仍需密切关注ADC可能引起的AE,并积极采取预防和治疗措施。由中山大学附属第一医院林颖教授参与编写的《中国乳腺癌抗体药物偶联物安全性管理专家共识》(以下简称《共识》)[2] 对ADC药物安全性管理的方方面面都制定了相应规范,以期为临床管理提供指导。

图1. 《中国乳腺癌抗体药物偶联物安全性管理专家共识》
拿SG为例,针对其引起的中性粒细胞减少和腹泻,共识指出,粒细胞集落刺激因子(G-CSF)为治疗中性粒细胞减少的常规用药。中性粒细胞减少伴发热或存在重复性感染的患者必须立即开始抗感染治疗。根据患者风险程度选择经验性抗生素治疗,高危患者应进行抗真菌预防。

图2. 共识对ADC相关中性粒细胞减少监测管理的推荐
《共识》对ADC药物相关腹泻也提出了管理建议,推荐在治疗期间密切监测,并根据需要给予液体和电解质。开始治疗前推荐预先使用止吐剂。若无禁忌证,可以使用阿托品对任何严重程度的早发型腹泻进行预处理和控制。在出现迟发型腹泻时,应评估感染原因,若未发现其他诱因,立即使用洛哌丁胺[2]。

图3. 共识对ADC相关腹泻监测管理的推荐
血小板减少是T-DM1减量甚至停药的首要原因,针对这一AE,《共识》推荐,在ADC治疗期间,应常规监测血小板计数,若出现血小板减少,应及时按说明书调整T-DM1剂量或停药。血小板减少≥2级时给予升血小板药物,血小板减少4级时可考虑输注血小板。必要时请血液科会诊[2]。

图4. 共识对ADC相关血小板减少管理的推荐
在HER2 ADC中,T-DXd的ILD相关死亡最高(1.7%~2.2%)[2]。《共识》指出,在T-DXd和T-DM1治疗期间,应监测并及时评估呼吸道症状、体征以及影像学相对于基线期的变化,并告知患者可能的风险以及出现症状后立即报告的必要性。接受ADC治疗的患者一旦疑诊ILD或非感染性肺炎,应严格进行ADC剂量调整或终止用药,并考虑立即开始糖皮质激素治疗,同时请呼吸科和影像科会诊[2]。

图5. 共识对ADC相关肺不良反应管理的推荐
SG广泛布局,不断拓宽获益人群
期待ADC带来更多亮眼表现
得益于整体良好的安全性,不少ADC药物也正在深入对联合治疗的探索。如,Ⅲ期ASCENT-04研究探索了SG联合免疫治疗药物帕博利珠单抗的疗效与安全性,Ⅲ期ASCENT-05研究则进一步对新辅助治疗后未取得病理学完全缓解(non-pCR)的eTNBC患者在辅助治疗阶段进行了SG联合帕博利珠单抗的探索。在新辅助治疗领域,SG联合免疫治疗(帕博利珠单抗)的研究也正在如火如荼地进行中,目前研究处于II期阶段,期待该领域相关成果的出炉。此外,鉴于SG在TNBC二线治疗中的出色表现,目前SG正积极探索将治疗前移至晚期一线治疗以及早期新辅助/辅助治疗阶段。
除TNBC治疗领域外,SG在HR+/HER2-乳腺癌中也有相应布局,并取得了初步结果——基于TROPiCS-02研究的阳性结果,SG已经获得FDA批准用于治疗既往接受过内分泌治疗且接受过≥2线系统治疗的不可切除局部晚期或转移性HR+/HER2-乳腺癌。Ⅲ期亚洲临床研究EVER-132-002旨在对比SG与医生选择的标准化疗用于治疗亚洲HR+/HER2-转移性乳腺癌患者的疗效;Ⅲ期SASCIA研究评估了SG在HER2阴性高危乳腺癌患者辅助强化治疗的疗效和安全性。
表1. SG在乳腺癌领域布局的临床研究
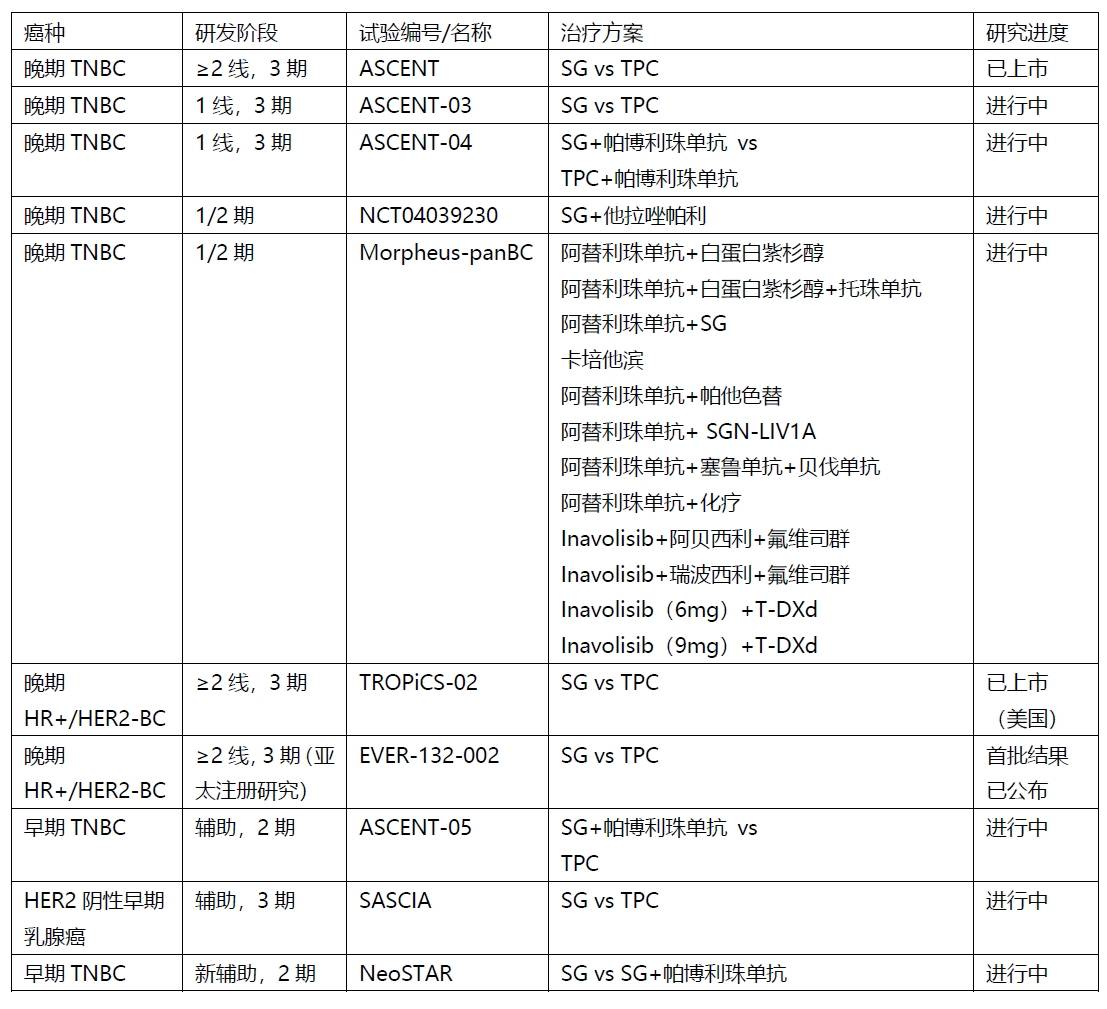
独立于乳腺癌,目前SG还在积极探索尿路上皮癌、肺癌等其他癌种领域,期待随着更多数据的披露,SG不断扩宽适应症,使这一兼具疗效、安全性的“魔法子弹”惠及更多患者。
小结
在精准治疗时代,ADC作为一种“魔法子弹”可精准靶向肿瘤细胞,治疗前景广阔,期待更多ADC及ADC联合治疗方案为乳腺癌患者带来更好的治疗效果以及更佳的预后。同时也期待临床医生与时俱进地汲取新兴知识,加强对《中国乳腺癌抗体药物偶联物安全性管理专家共识》的学习,将不同ADC的不良反应了然于心,并能做到对不良反应的早期识别、评估、管理、监测。只有掌握正确管理ADC药物安全性的方式,才能真正发挥出这一“魔法子弹”最大的效应,为更多乳腺癌患者带来获益。
排版编辑:Jessica
[1] 林云, 张妍, 陈曦. 靶向Trop2的抗体偶联药物治疗三阴性乳腺癌的研究进展[J]. 中国肿瘤临床, 2023, 50(18): 946-950.
[2] 中国医师协会肿瘤医师分会乳腺癌学组, 中国抗癌协会国际医疗交流分会. 中国乳腺癌抗体药物偶联物安全性管理专家共识[J]. 中华肿瘤杂志, 2022, 44(9):913-927.
[3] Dumontet C, Reichert JM, Senter PD, Lambert JM, Beck A. Antibody–drug conjugates come of age in oncology. Nat Rev Drug Discov 2023;22:641-61.
[4] Krop I, Juric D, Shimizu T, et al. Abstract GS1-05: Datopotamab deruxtecan in advanced/metastatic HER2-breast cancer: Results from the phase 1 TROPION-PanTumor01 study[J]. Cancer Research, 2022, 82(4_Supplement): GS1-05-GS1-05.
[5] Yin Y, Wu X, Ouyang Q, et al. Updated efficacy and safety of SKB264 (MK-2870) for previously treated metastatic triple negative breast cancer (mTNBC) in Phase 2 study. 2023 SABCS, PS08-08.
[6] Bardia A, Mayer IA, Vahdat LT, et al. Sacituzumab Govitecan-hziy in Refractory Metastatic Triple-Negative Breast Cancer. N Engl J Med. 2019 Feb 21;380(8):741-751.
[7] Bardia A, Tolaney SM, Loirat D,et al. Sacituzumab Govitecan Versus Treatment of Physician's Choice in Patients With Previously Treated Metastatic Triple-Negative Breast Cancer: Final Data From the Phase 3 ASCENT Study. 2022 ASCO. 1071.
[8] Bardia A, Tolaney SM, Punie K, et al. Biomarker analyses in the phase Ⅲ ASCENT study of Sacituzumab govitecan versus chemotherapy in patients with metastatic triple-negative breast cancer. Ann Oncol, 2021, 32(9):1148-1156.
[9] Kalinsky K, et al. Real-world (RW) use patterns, effectiveness, and tolerability of sacituzumab govitecan (SG) for second-line (2L) and later treatment of metastatic triple-negative breast cancer (mTNBC). 2023 ESMO 393P.
[10] 257P-Health-related quality of life (HRQoL) in the ASCENT study of sacituzumab govitecan (SG) in metastatic triple-negative breast cancer (mTNBC).ESMO 2021.











 苏公网安备32059002004080号
苏公网安备32059002004080号


