
世人万千种,有人住高楼,有人在深沟,有人光万丈,有人一身锈。乳腺癌也如同世人,结局各不相同,需要临床医师根据乳腺癌分期分级分型对其结局进行预测,从而采用不同的治疗方案,避免治疗不足或治疗过度。病理科医师通常采用美国癌症联合委员会TNM分期标准、诺丁汉组织学分级标准、分子分型标准对乳腺癌进行分期分级分型。不过,这些标准大多为定性而非定量,且未考虑肿瘤微环境非癌症因素。
2023年11月27日,英国《自然》旗下《自然医学》在线发表美国芝加哥西北大学范伯格医学院、美国癌症学会、芝加哥小约翰斯特罗格医院、埃默里大学、国家癌症研究所的研究报告,首次采用人工智能对全国乳腺浸润癌患者人群肿瘤微环境癌症因素和非癌症因素进行大数据综合分析,开发出一种新的人工智能工具,可精准预测乳腺癌患者结局,避免不必要的化疗。
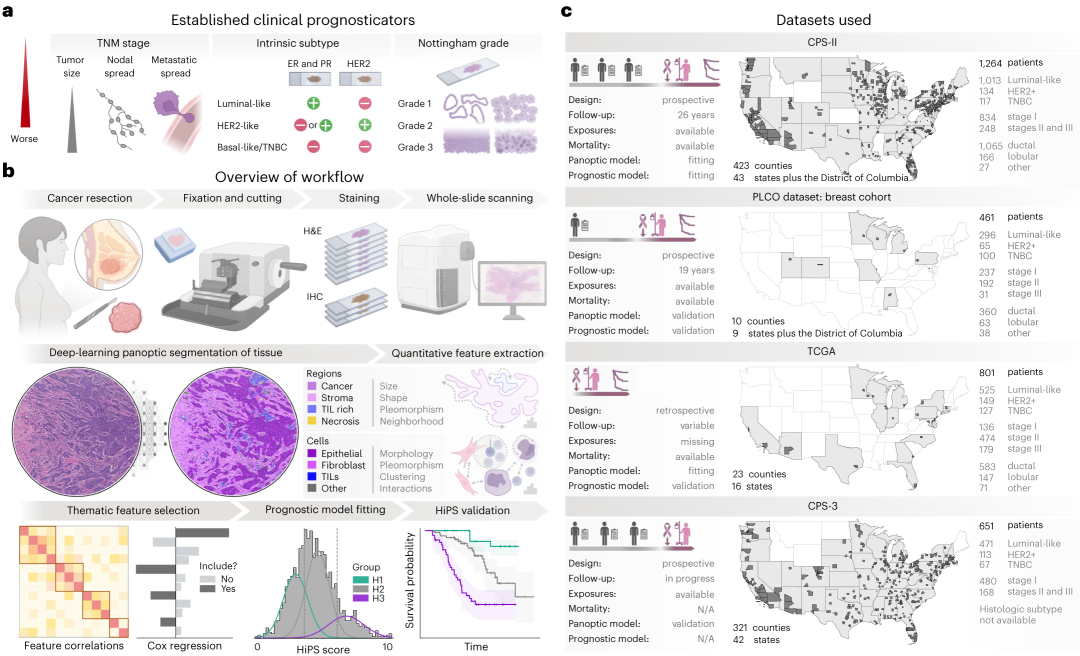
首先,该研究对癌症预防研究II(CPS-II)来自美国哥伦比亚特区以及43个州423个县的1264例乳腺癌患者病理数据和长达26年随访数据进行分析,采用人工智能深度学习准确绘制细胞和组织结构图,定量分析上皮细胞、基质细胞、免疫细胞及其空间分布与相互作用的26种特征,开发出对乳腺肿瘤微环境形态所致死亡风险的综合预后评分:组织组学预后特征(HiPS)。
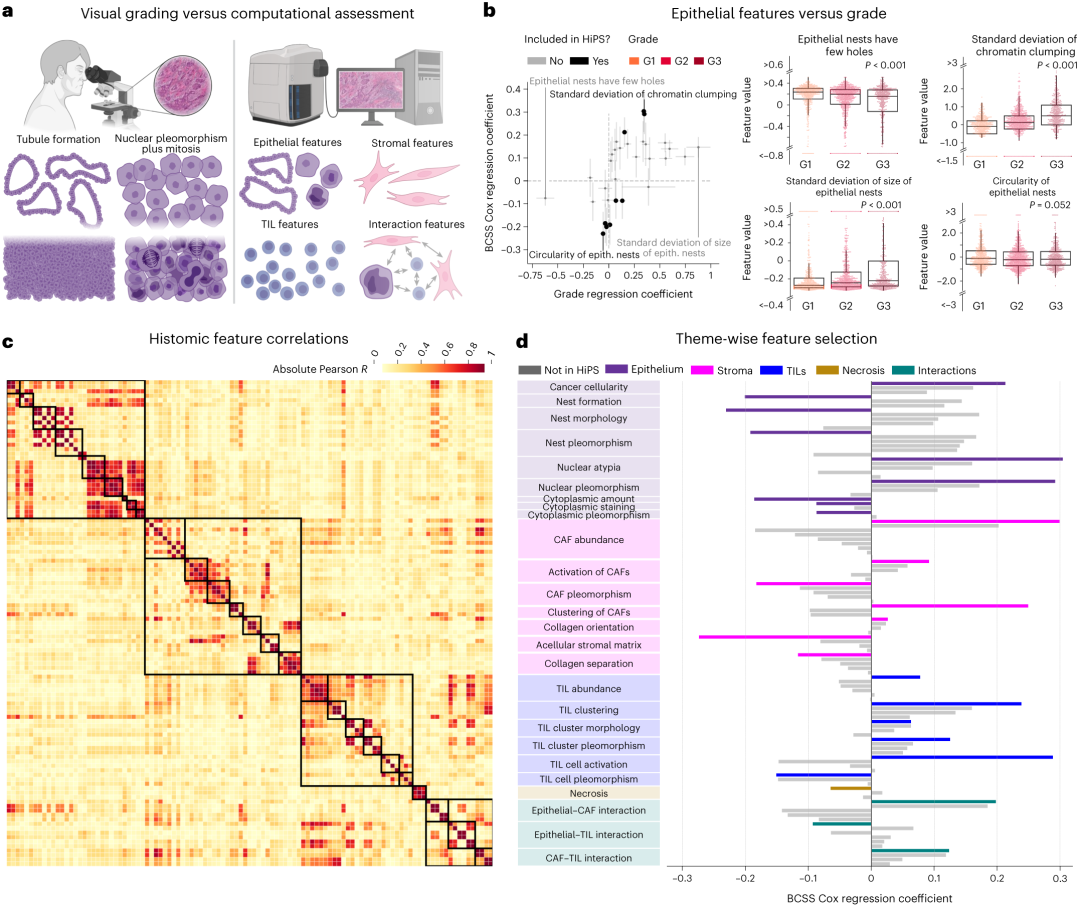 随后,该研究采用来自3个独立队列的数据进行验证,包括前列腺肺结直肠卵巢癌研究(PLCO)461例乳腺癌患者、癌症预防研究3(CPS-3)651例乳腺癌患者、癌症基因组图谱(ACS)801例乳腺癌患者。为了实现该目标,该研究还创建了由几大洲医学生和病理科医师组成的国际网络,这些志愿者在几年的时间里通过网站提供这些数据,使人工智能模型能够更可靠地解释乳腺癌组织图像。
随后,该研究采用来自3个独立队列的数据进行验证,包括前列腺肺结直肠卵巢癌研究(PLCO)461例乳腺癌患者、癌症预防研究3(CPS-3)651例乳腺癌患者、癌症基因组图谱(ACS)801例乳腺癌患者。为了实现该目标,该研究还创建了由几大洲医学生和病理科医师组成的国际网络,这些志愿者在几年的时间里通过网站提供这些数据,使人工智能模型能够更可靠地解释乳腺癌组织图像。
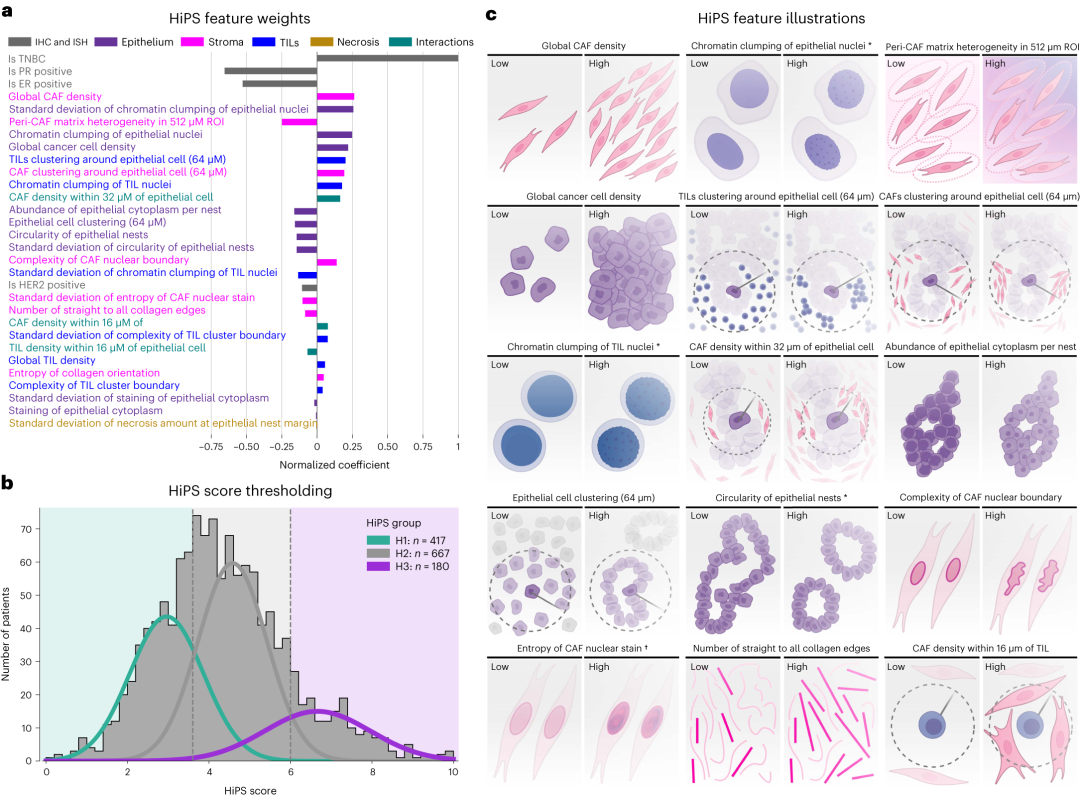
结果发现,HiPS对于预测患者生存结局,始终优于病理科医师,无论TNM分期及其相关因素如何,而主要取决于肿瘤微环境基质细胞和免疫细胞的特征,尤其对于雌激素受体阳性乳腺癌和HER2阳性乳腺癌。对于预后评分较好的低风险患者,即使不化疗,生存结局也较好;对于预后评分较好的高风险患者,即使减少化疗的持续时间或强度,对生存结局影响也不大。
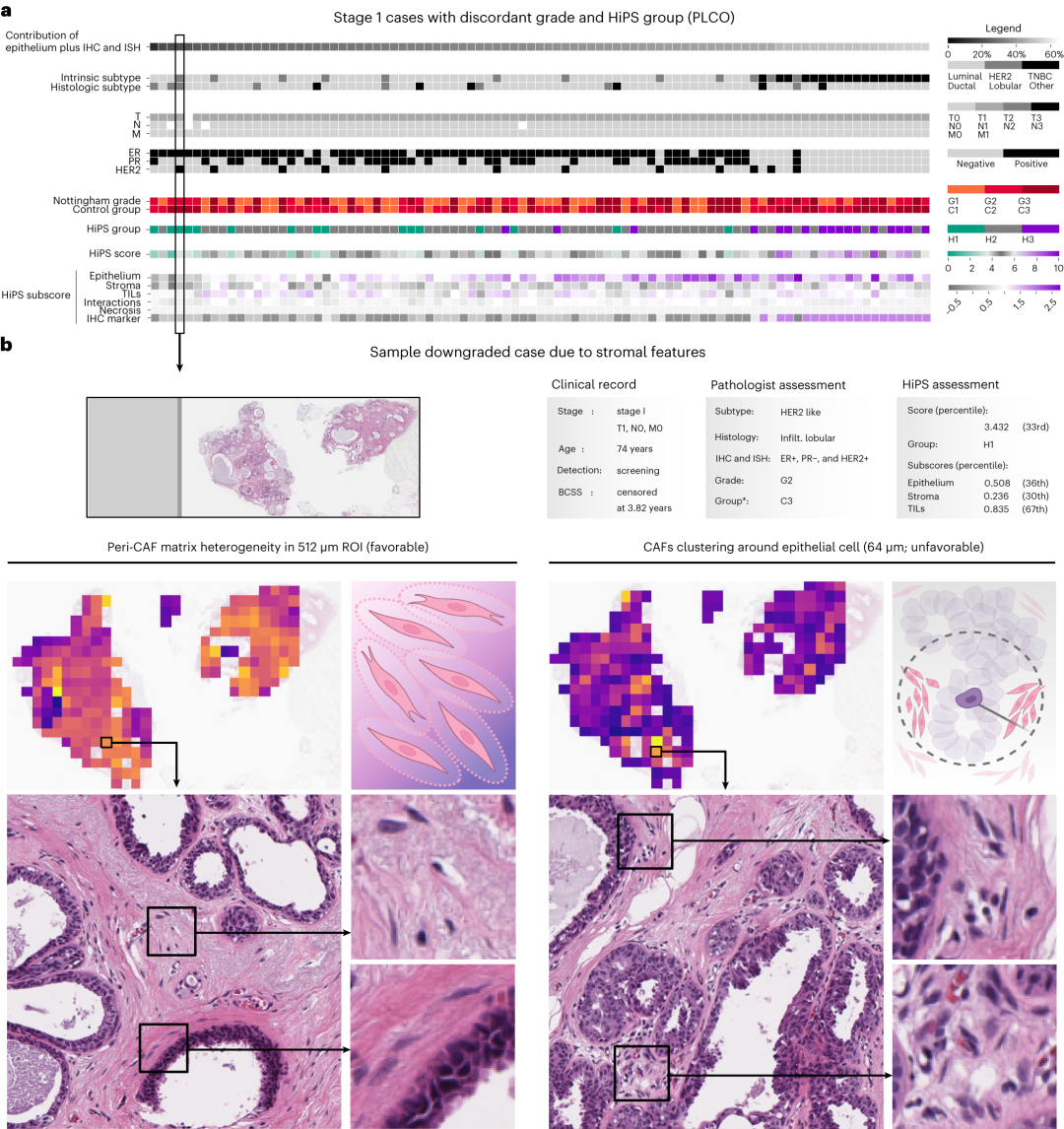
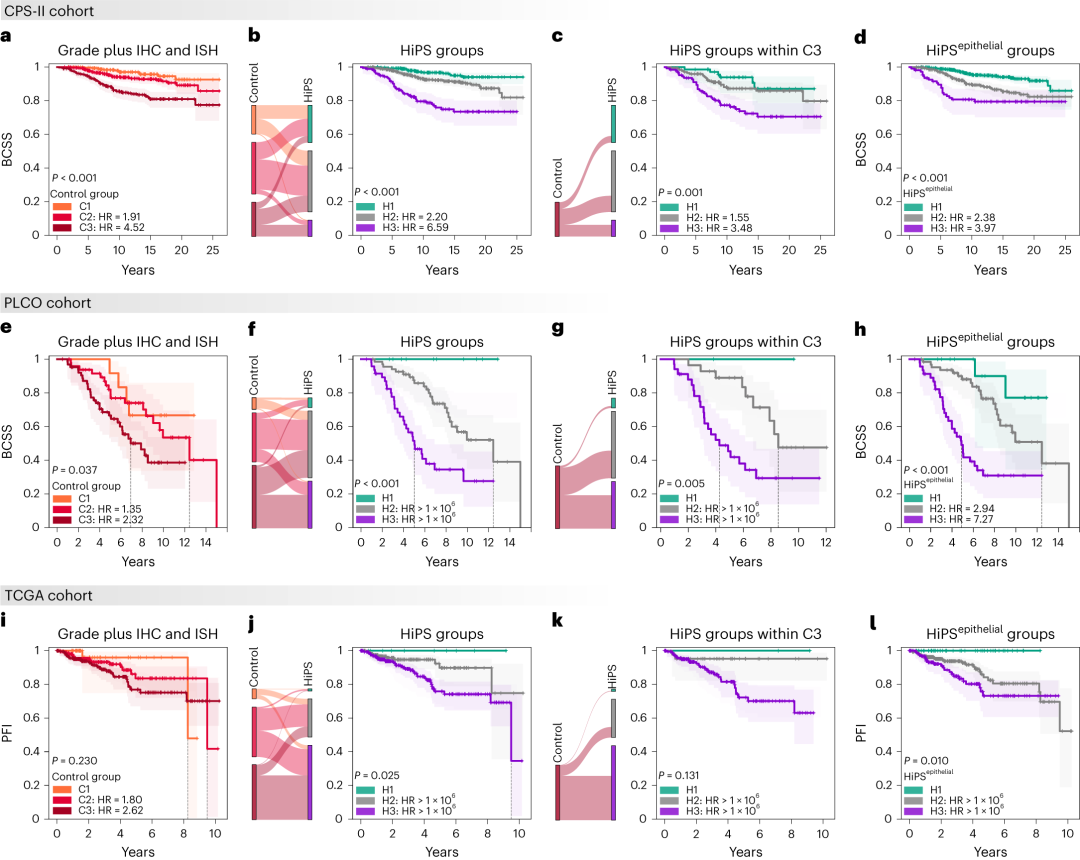
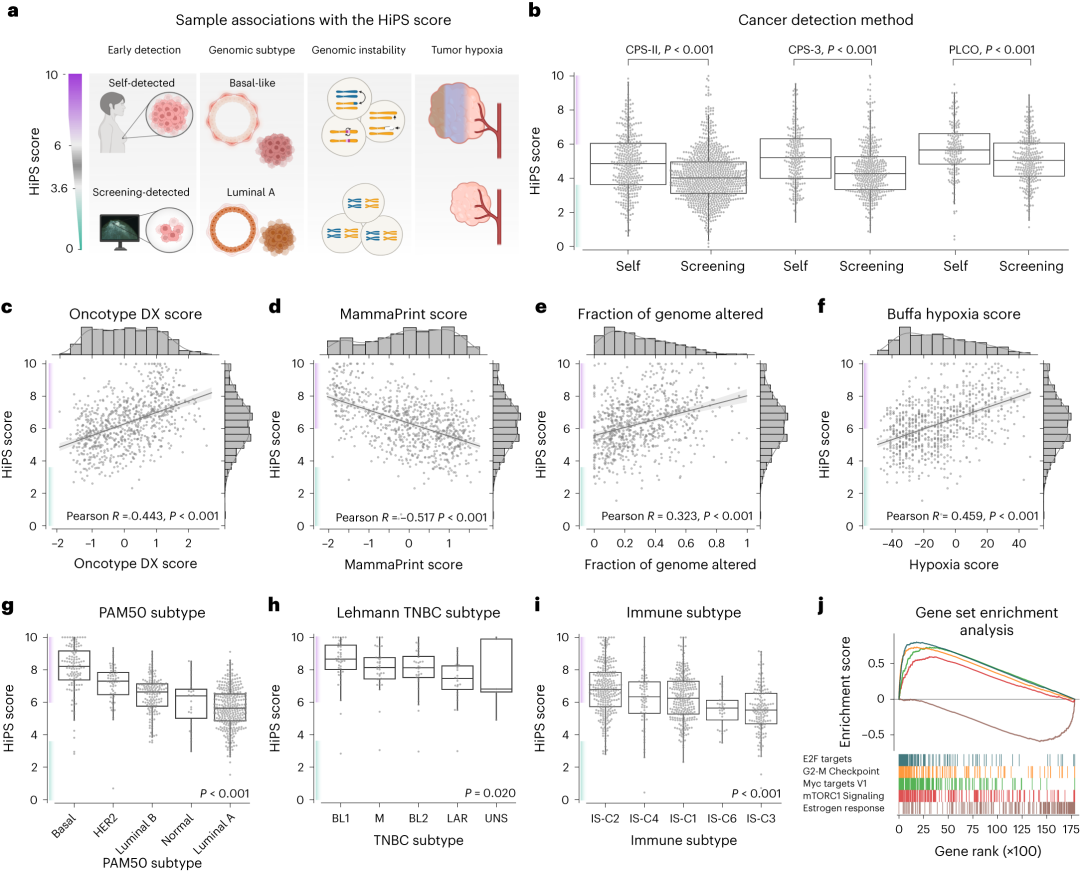
因此,该研究结果表明,HiPS是一种经过严格验证的生物学新指标,有助于病理科医师和临床医师对患者进行更精准的预后,避免不必要的化疗。
Nat Med. 2023 Nov 27. IF: 82.9
A population-level digital histologic biomarker for enhanced prognosis of invasive breast cancer.
Amgad M, Hodge JM, Elsebaie MAT, Bodelon C, Puvanesarajah S, Gutman DA, Siziopikou KP, Goldstein JA, Gaudet MM, Teras LR, Cooper LAD.
Northwestern University Feinberg School of Medicine, Chicago, IL, USA; American Cancer Society, Atlanta, GA, USA; John H. Stroger, Jr. Hospital of Cook County, Chicago, IL, USA; Emory University School of Medicine, Atlanta, GA, USA; National Cancer Institute, Bethesda, MD, USA.
Breast cancer is a heterogeneous disease with variable survival outcomes. Pathologists grade the microscopic appearance of breast tissue using the Nottingham criteria, which are qualitative and do not account for noncancerous elements within the tumor microenvironment. Here we present the Histomic Prognostic Signature (HiPS), a comprehensive, interpretable scoring of the survival risk incurred by breast tumor microenvironment morphology. HiPS uses deep learning to accurately map cellular and tissue structures to measure epithelial, stromal, immune, and spatial interaction features. It was developed using a population-level cohort from the Cancer Prevention Study-II and validated using data from three independent cohorts, including the Prostate, Lung, Colorectal, and Ovarian Cancer trial, Cancer Prevention Study-3, and The Cancer Genome Atlas. HiPS consistently outperformed pathologists in predicting survival outcomes, independent of tumor-node-metastasis stage and pertinent variables. This was largely driven by stromal and immune features. In conclusion, HiPS is a robustly validated biomarker to support pathologists and improve patient prognosis.
PMID: 38012314
DOI: 10.1038/s41591-023-02643-7
排版编辑:肿瘤资讯-Astrid











 苏公网安备32059002004080号
苏公网安备32059002004080号


