内分泌治疗(ET)和细胞周期蛋白依赖性激酶4/6抑制剂(CDK4/6i)是HR+乳腺癌的标准治疗方法。然而,关于ET潜在神经认知影响的研究数据并不一致,并且对于CDK4/6i而言数据较少。一项药物警戒研究便探索了ET和CDK4/6i治疗是否与神经认知障碍(NCI)相关[1],为临床治疗和管理予以启示。
背景
ET显著提高了乳腺癌患者的生存率,ET包括芳香酶抑制剂(AI)(阿那曲唑、来曲唑、依西美坦、选择性雌激素受体调节剂和降解剂(SERM 和 SERD)(他莫昔芬、氟维司群)等。随着新型药物的开发与与应用,CDK4/6i的出现彻底改变了高危和转移性HR+乳腺癌的辅助和一线治疗,二者联合使用,通过作用于细胞周期检查点提高ET疗效,使患者获得更长生存期。
但ET需要接受较长的治疗时间,患者可能面临长期不良事件(AE)的风险。许多研究报告了 ET 的神经认知障碍(NCI)。然而,目前的研究结论并不一致,且关于 CDK4/6i对认知影响的数据有限。
因此,研究者使用世界卫生组织 (WHO) 药物警戒数据库 VigiBase ® 中报告的神经认知症状,进行了不相称性分析,以评估单独或与 CDK4/6i 联合使用的 NCI 和 ET 之间的关联。在二次分析中,描述了ETs和CDK4/6i报告的NCI病例的临床特征。
方法
VigiBase ® 是最大的药物警戒数据库,已被开发用于检测药物(包括癌症治疗)与 AE 之间的潜在关联。当 NCI 症状与 ET 和 CDK4/6i 的可归因性被定义为可疑/相互作用/伴随时,使用 WHODrug Global 词典纳入病例。严重 AE 被定义为导致死亡、危及生命、需要住院治疗或延长现有住院治疗、导致持续或严重残疾,或根据报告者的判断。
如前所述,研究者使用了标准化的 MedDRA 查询和与 NCI 相关的高级组术语:“痴呆”、“精神障碍”、“认知和注意力障碍和障碍”、“谵妄”、“痴呆和遗忘状况”以及“思维和感知障碍”。由于缺乏描述药物诱发的NCI的具体术语,为了避免纳入神经或精神疾病,研究者将查询重点放在症状上,并排除了与神经或精神疾病相关的所有首选术语(PTs)。研究者还将(EMM 和 VLB)研究中包含的每个 PT 分类为《精神疾病诊断与统计手册》第五版(DSM-5)定义的六种 NCI 模式之一:社会认知、语言、执行功能、复杂注意力、学习和记忆以及知觉运动功能。
分析包括ET(“来曲唑”、“阿那曲唑”、“依西美坦”、“他莫昔芬”、“托瑞米芬”和“氟维司群”)和CDK4/6i(“哌柏西利”、“阿贝西利”和“瑞波西利”)。一种药物可能与多种 PT 相关,为了最大限度地降低 ET 和 CDK4/6i 的非乳腺癌适应症的风险,研究人群仅限于女性。
在研究者的初步分析中,首先计算了根据年龄调整的报告比值比(ROR),以确定NCI与每个ET之间的潜在关联。其次,研究者计算了根据年龄调整的 LOR,以确定 NCI 与每个 CDK4/6i之间的潜在关联。在初步分析中,研究者限制了从VigiBase ® 中用CDK4/6i报告的第一次AE之日(2014年1月1日)到数据提取之日(2022年3月16日)的病例和非病例提取时间。用定量变量的均值和定性变量的比例总结了病例特征。
对于主要和次要分析,研究者报告了95%的可信区间(CI),较低的ROR置信区间>1表示药物与AE之间存在关联。为了有效解释信号,仅当目标药物/AE 对至少有 5 份报告时,才计算 RR。
结果
2014 年 1 月 1 日至 2022 年 3 月 16 日,研究者确定了 262,366 份与 NCI 相关的报告,其中 2,583 份涉及 ET,1,943 份涉及 CDK4/6i(图1)。共有3,400份报告来自美洲(75%),971份来自欧洲(21%),52份来自亚洲(1%)。报告最多的PT是“记忆障碍”(27%)、“健忘症”(9%)、“认知障碍”(6%)、“注意力障碍”(6%)和“言语障碍”(5%)。在排除没有年龄信息的病例后,研究者在年龄调整后的初步分析中纳入了2,093份关于ET的报告和1,686份关于CDK4/6i的报告。
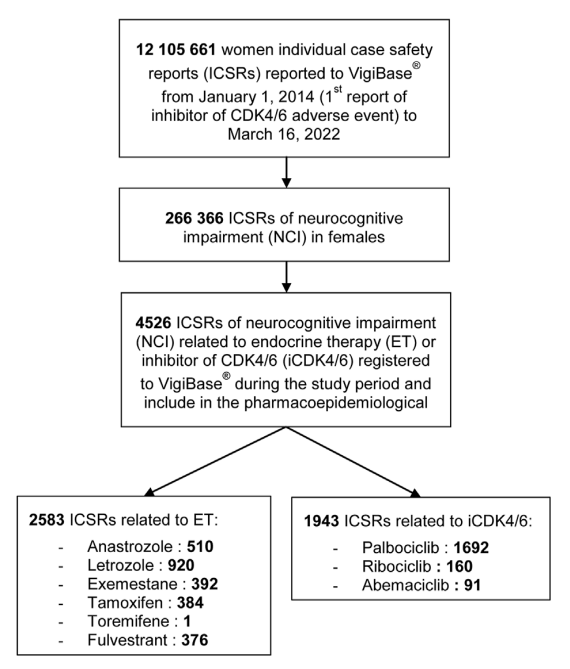 图1 药物警戒研究的流程图
图1 药物警戒研究的流程图
接受 ET 和/或 CDK4/6i 治疗的患者的 NCI 报告涉及所有年龄组:23% 的女性年龄超过 75 岁(n = 800),26% 在 65 至 74 岁之间(n = 884),29% 在 45 至 64 岁之间(n = 1,009),5% 在 18 至 44 岁之间(n = 158)。17%的报告缺少年龄(n = 595)。根据世界卫生组织的分类,57%的与NCI相关的报告被认为是严重的,三分之一的严重NCI患者中断了治疗。
关于ET,阿那曲唑(aROR 1.52;95% CI:1.37-1.67)、来曲唑(aROR 1.37;95% CI:1.27-1.47)、依西美坦(aROR 1.37;95% CI:1.22-1.53)、他莫昔芬(aROR 1.25;95% CI:1.12-1.40)与较高的 NCI 报告相关(表1)。
表1 神经认知功能障碍与个体内分泌治疗和CDK4/6抑制剂的不相称性分析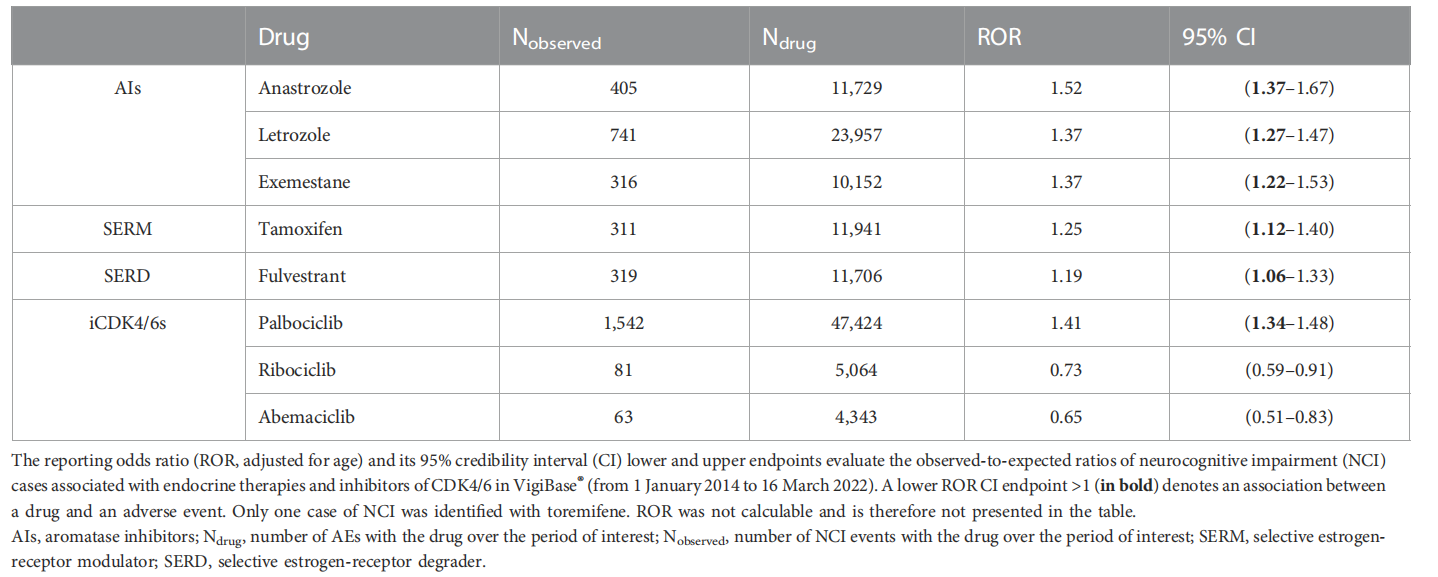
关于CDK4/6i,只有哌柏西利(aROR 1.41;95% CI:1.34–1.48)与较高的NCI报告显著相关。未发现瑞波西利(aROR 0.73;95% CI:0.59-0.91)和阿贝西利(aROR 0.65;95% CI:0.51-0.83)的信号。
在4,524份报告中,分别有84份和31份报告存在已知与NCI相关的合并疾病和合并治疗。由于数量少,未进行排除合并疾病和合并治疗的敏感性分析。
为了更好地描述在初步分析中发现的具有ET和CDK4/6i的NCI病例,研究者计算了六种NCI模式中每一种的aRO。来曲唑和依西美坦与较高的语言报告(aROR 2.11;95% CI:1.89-2.36;aROR 2.18;95% CI:1.84-2.57)以及学习和记忆障碍(aROR 1.54;95% CI:1.22-1.94 和 aROR 1.78;95% CI:1.28-2.48)相关。哌柏西利与较高的语言、学习和记忆障碍报告显著相关(aROR 2.74;95% CI:2.55-2.94;aROR 1.31;95% CI:1.10-1.57)。没有药物与较高的执行功能或社会认知障碍报告相关。
讨论
雌激素受体在乳腺癌细胞和中枢神经系统上均有表达。雌二醇参与中枢神经传递,可能对轴突生长产生影响。由于下丘脑、杏仁核或海马等认知功能相关区域的雌二醇激活减少,ET 可能导致 NCI。
这些结果提供了进一步的证据,表明所有 ET 类别都可能与乳腺癌患者的 NCI 相关。研究者对 AI 的结果与使用神经认知测试的研究的荟萃分析一致,发现 AI 与乳腺癌患者的语言和学习/记忆障碍之间存在关联。
根据随机临床试验中对他莫昔芬与 AI 进行比较的神经心理学评估,几项研究表明,他莫昔芬可能比 AI 更能导致 NCI。在TEAM试验[2]中,接受他莫昔芬辅助治疗的女性的信息处理速度比依西美坦治疗的女性慢(p = 0.02;Cohen's d = 0.36)。同样,在 BIG-1-98 试验[3]中,接受辅助他莫昔芬治疗的女性的总体认知能力比接受来曲唑治疗的女性差 (p = 0.04,Cohen's d = 0.40)。
CDK4/6i是否影响中枢神经系统尚不清楚。细胞周期蛋白 D 抑制可能会改变神经发生并导致 NCI。然而,这并不能解释为什么研究者研究中的信号被分离到哌柏西利。需要进一步的研究来确定 BDNF/TRK 通路的抑制是否介导哌柏西利治疗患者的 NCI。
结论
这项药物警戒研究探索了乳腺癌患者 ET 和 NCI 之间的关联。研究者强调了分离到哌柏西利的CDK4/6i的新信号,这需要进一步研究。NCI 影响了所有暴露的年龄组,主要涉及学习、记忆和语言,必须进一步考虑乳腺癌治疗对患者神经认知的影响。
[1] Prevost R, Chretien B, et al. Neurocognitive impairment in females with breast cancer treated with endocrine therapy and CDK4/6 inhibitors: a pharmacovigilance study using the World Health Organization's database. Front Pharmacol. 2023 Oct 20;14:1278682. doi: 10.3389/fphar.2023.1278682.
[2] Schilder CM, Seynaeve C, et al. Effects of tamoxifen and exemestane on cognitive functioning of postmenopausal patients with breast cancer: results from the neuropsychological side study of the tamoxifen and exemestane adjuvant multinational trial. J Clin Oncol. 2010 Mar 10;28(8):1294-300. doi: 10.1200/JCO.2008.21.3553.
[3] Phillips KA, Ribi K, Sun Z, et al. Cognitive function in postmenopausal women receiving adjuvant letrozole or tamoxifen for breast cancer in the BIG 1-98 randomized trial. Breast. 2010 Oct;19(5):388-95. doi: 10.1016/j.breast.2010.03.025.
排版编辑:肿瘤资讯-olivia











 苏公网安备32059002004080号
苏公网安备32059002004080号


