
吴浦嫄, 王涛, 陈宝俊, 等. 化疗联合程序性死亡蛋白1抗体治疗在食管鳞状细胞癌新辅助治疗真实世界中的疗效及安全性[J]. 中华肿瘤杂志, 2023, 45(2):170-174.
DOI: 10.3760/cma.j.cn112152-20210806-00586.
目的
评估真实世界中新辅助化疗联合程序性死亡蛋白1(PD-1)抗体治疗对局部晚期可切除、边界或潜在可切除食管鳞状细胞癌(简称鳞癌)的有效率和安全性。
方法
2020年4月至2021年3月在南京大学医学院附属鼓楼医院行化疗联合PD-1抗体新辅助治疗的局部晚期可切除、边界或潜在可切除食管鳞癌患者28例,根据美国癌症联合会第8版临床TNM分期标准,Ⅱ期、Ⅲ期、ⅣA期、ⅣB期和分期不明者分别有1、15、10、1和1例。治疗方案为紫杉类药物与铂类药物或氟尿嘧啶的双药化疗联合PD-1抗体治疗。2个周期后对患者进行疗效评估,并对适合手术者行手术治疗。
结果
28例患者中,分别有1、21、5和1例患者完成了1、2、3、4个周期化疗联合PD-1抗体治疗。客观缓解率为71.4%(20/28),疾病控制率为100%(28/28)。3级以上不良反应发生率为21.4%(6/28),其中中性粒细胞减少3例,白细胞减少1例,血小板减少1例,免疫性肝炎1例。无治疗相关死亡。23例患者完成了手术治疗,R0切除率为87.0%(20/23),其中13例患者术后病理分期降至Ⅰ期,病理完全缓解率为17.3%(4/23),原发灶病理完全缓解率为21.7%(5/23)。4例在完成新辅助治疗后行根治性放化疗,1例达到部分缓解后拒绝后续治疗。
结论
对于局部晚期可切除、边界或潜在可切除食管鳞癌患者,新辅助化疗联合PD-1抗体治疗有效率高,安全性良好,是一种有潜力的治疗方式。
【关键词】食管肿瘤;新辅助治疗;免疫治疗;疗效;安全性;真实世界研究
新辅助放化疗序贯手术是目前局部晚期可切除食管鳞状细胞癌(简称鳞癌)的国际推荐,但三联治疗后仍有49%的患者会发生肿瘤复发与转移。新辅助化疗在可切除食管鳞癌中的地位一直存在争议,一些头对头比较新辅助放化疗与新辅助化疗治疗后食管鳞癌患者长期生存的研究也在进行中。在临床上,新辅助放化疗具有客观缓解率(objective response rate, ORR)和病理完全缓解(pathological complete response, pCR)率高的优势,但亦存在耗时长、花费高、对食管手术解剖存在潜在影响等缺点,因此探索安全有效且短平快、费用低的新辅助治疗模式一直是食管癌临床研究的热点。
程序性死亡蛋白1(programmed death-1, PD-1)抗体已经改变了晚期食管鳞癌的二线治疗格局,而化疗联合PD-1抗体也在一线治疗中表现出明显的优势。在此基础上,越来越多的研究集中在食管鳞癌围手术期的PD-1抗体联合治疗,主要涉及术前放化疗联合PD-1抗体、术前化疗联合PD-1抗体等。在本研究中,我们回顾性分析了28例术前化疗联合PD-1抗体治疗的食管鳞癌患者的临床和随访资料,旨在评估该治疗方案的安全性、近期疗效、手术pCR及降期情况,为进一步深入研究奠定基础。


1.病例资料:
纳入标准:(1)经胃镜病理诊断为食管鳞状细胞癌。(2)治疗前经多学科团队(multidisciplinary team, MDT)评估为可切除、边界或潜在可切除的食管鳞癌。(3)美国东部肿瘤协作组(Eastern Cooperative Oncology Group, ECOG)体力状态评分为0~1分。(4)根据实体瘤疗效评价标准(response evaluation criteria in solid tumours, RECIST)1.1有可测量病灶。(5)完成新辅助化疗联合PD-1抗体治疗2个周期,行疗效评价并评估手术的可能性,后续行手术治疗或其他治疗。(6)签署知情同意书。纳入2020年4月至2021年3月在南京大学医学院附属鼓楼医院治疗的符合纳入标准的食管鳞癌患者28例,其中男24例,女4例,中位年龄为66岁,四分位数间距(interquartile range, IQR)为63~70岁。本研究符合《世界医学大会赫尔辛基宣言》的原则。
2.新辅助治疗方法:
化疗采用含紫杉类药物、铂类药物或氟尿嘧啶的双药化疗方案,包括紫杉醇脂质体(135~175 mg/m2)或白蛋白紫杉醇(175 mg/m2)联合奈达铂(75 mg/m2)或洛铂(30 mg/m2)或氟尿嘧啶(1800 mg/m2,72 h持续静脉滴注)3周方案。28例患者中,27例采用紫杉类和铂类药物双药化疗,1例患者因肾功能不全采用紫杉类药物和氟尿嘧啶双药化疗。在紫杉类药物使用方面,12例患者采用紫杉醇脂质体治疗,16例患者采用白蛋白紫杉醇治疗。PD-1抗体治疗,使用特瑞普利单抗19例,信迪利单抗4例,帕博利珠单抗2例,卡瑞利珠单抗1例,替雷利珠单抗1例,纳武利尤单抗1例,均按照标准剂量使用。
3.近期疗效评价:
依据RECIST 1.1标准对新辅助化疗联合PD-1抗体治疗后的近期疗效进行评价,根据靶病灶在治疗前后的变化分为完全缓解(complete response, CR)、部分缓解(partial response, PR)、疾病稳定(stable disease, SD)和疾病进展(progressive disease, PD)。
4.安全性评价:
依据常见不良反应标准(Common Terminology Criteria for Adverse Events, CTCAE)4.0评价新辅助治疗的不良反应。根据术中出血量、手术时间、手术并发症等情况,评估新辅助化疗联合PD-1抗体治疗后手术的可行性与安全性。
5.pCR率及分期:
收集患者的手术病理资料,包括pCR情况、病理分期、程序性死亡蛋白配体1(programmed death-ligand 1, PD-L1)综合阳性评分(combined positive score, CPS)等。
6.随访:
2年内每3个月随访1次,2~5年每6个月随访1次,中位随访时间为8.2个月(IQR:5.8~10.5个月)。随访内容包括患者的症状问询、体格检查、血液学和影像学检查。无失访患者。
7.统计学方法:
应用SPSS 16.0软件进行统计分析。连续变量采用中位数及IQR表示。计数资料的组间比较采用Fisher精确概率法。采用Kaplan-Meier法计算中位随访时间。显著性检验均为双侧检验,检验水准α=0.05。


1.患者的临床特征:
28例食管鳞癌患者中,肿瘤位于胸上、中、下段分别有4、16和8例;组织学分级G1、G1-2、G2、G2-3、G3和Gx分别有1、1、10、5、6和5例;根据美国癌症联合会(American Joint Committee on Cancer, AJCC)第8版临床TNM分期标准,T2期、T3期、T4期和Tx期分别有3、17、5和3例,N1期、N2期、N3期和cNx期分别有5、13、5和5例;Ⅱ期、Ⅲ期、ⅣA期、ⅣB期和分期不明者分别有1、15、10、1和1例。16例患者经过MDT讨论R0切除困难,但预计新辅助治疗降期后可R0切除。20例患者进行了肿瘤组织PD-L1 CPS检测,其中PD-L1 CPS≥10分的患者占35.0%(7/20)。
2.治疗完成情况与方案可行性:
28例患者中,分别有1、21、5和1例患者完成了1、2、3、4个周期化疗联合PD-1抗体治疗。23例(82.1%)患者完成了手术治疗,其中22例完成了新辅助治疗及手术治疗,1例在疗效评价为SD后改行新辅助同步放化疗,重新评估达临床CR后行手术治疗。4例患者在完成新辅助治疗后病情稳定,行根治性放化疗。1例患者达到PR后拒绝手术及后续治疗。
6例接受了3~4个周期化疗联合PD-1抗体治疗的患者中,5例因2个周期治疗后MDT评估认为仍存在手术无法R0切除的风险,因此增加了1~2个周期治疗;1例因等待手术时间长担心肿瘤复发,而增加了1个周期治疗。3例患者后续行手术治疗,2例后续行同步放化疗,1例达到PR与手术标准,但患者及家属拒绝手术及后续治疗。
3.新辅助治疗的近期疗效评价:
28例患者均进行了影像学近期疗效评价,其中CR 3例,PR 17例,SD 8例。ORR为71.4%(20/28),疾病控制率(disease control rate, DCR)为100.0%(28/28),89.3%(25/28)的患者靶病灶缩小。在13例PD-L1 CPS<10分的患者中,8例达到PR或CR;在7例PD-L1 CPS≥10分的患者中,4例达到PR或CR,两组差异无统计学意义(P=1.000)。在6例接受了3~4个周期化疗联合免疫治疗的患者中,PR 3例,SD 3例。
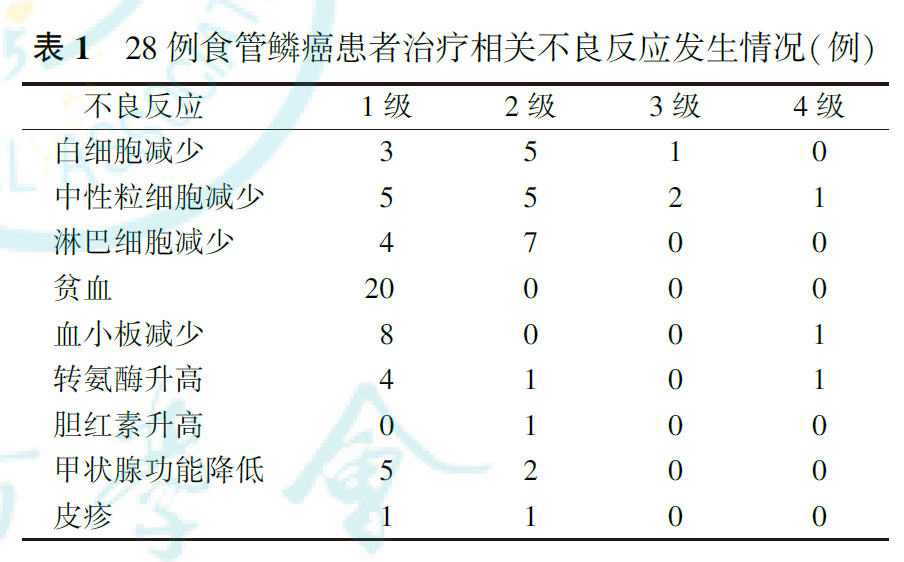
4.治疗安全性评价:
28例患者均进行了安全性评价,结果见表1。常见的治疗相关不良反应有贫血、中性粒细胞减少、淋巴细胞减少、白细胞减少、血小板减少和转氨酶升高,发生率分别为71.4%(20/28)、46.4%(13/28)、39.3%(11/28)、32.1%(9/28)、32.1%(9/28)和17.9%(5/28)。常见的免疫相关不良反应有甲状腺功能降低,发生率为25.0%(7/28)。3级及以上不良反应发生率为21.4%(6/28),其中中性粒细胞减少3例,白细胞减少1例,血小板减少1例,免疫性肝炎1例。无治疗相关死亡。
在22例接受了2个周期化疗联合PD-1抗体治疗的患者中,5例发生了3级及以上不良反应,未见3级及以上免疫相关不良反应。在6例接受了3~4个周期化疗联合PD-1抗体治疗的患者中,1例出现4级免疫性肝炎,未见其他3级及以上不良反应。两组患者3级及以上不良反应发生情况、3级及以上免疫相关不良反应发生情况,差异均无统计学意义(P值分别为1.000和0.214)。
5.手术及术后病理评价:
在23例行手术治疗的患者中,从治疗开始至手术的中位时间为67 d(IQR: 60~83 d),中位手术时长为240 min(IQR: 185~300 min),中位术中出血量为200 ml(IQR: 200~300 ml),中位清扫淋巴结数目为17枚(IQR: 13~22枚)。其中,1例患者术后出现吻合口瘘,经治疗后好转,未发生其他手术相关并发症,无手术相关死亡。
23例行手术治疗患者的R0切除率为87.0%(20/23)。术后病理分期为Ⅰ期13例,Ⅱ期1例,ⅢA期5例,ⅢB期4例;T0期5例,T1期8例,T2期8例,T3期2例;N0期14例,N1期5例,N2期4例。pCR率为17.3%(4/23),原发灶pCR率为21.7%(5/23),两者差异无统计学意义(P=1.000)。在10例PD-L1 CPS<10分的患者中,病理分期降至Ⅰ期、达到pCR与原发灶pCR者分别有3、1和2例;在5例PD-L1 CPS≥10分的患者中,分别有3、1和1例,两组差异均无统计学意义(P=0.329,P=1.000,P=1.000)。其中,1例PD-L1 CPS<10分的患者,在近期疗效评价为SD后改用新辅助同步放化疗,重新评估达CR后进行手术,术后病理提示达到pCR。在6例接受了3~4个周期化疗联合免疫治疗的患者中,3例行手术治疗,2例患者为非R0切除,1例患者术后病理分期为ⅢA期(T2N1M0G2)。此外,10例紫杉醇脂质体治疗的手术患者中无pCR者,13例白蛋白紫杉醇治疗的手术患者中有4例达到pCR,但两组差异均无统计学意义(P=0.104)。
6.复发转移情况:
在随访期内,20例R0切除的患者均未出现复发转移,3例非R0切除的患者均出现了疾病进展,其中纵隔淋巴结转移2例,腹膜后淋巴结转移1例。4例后续进行根治性放化疗的患者中,1例出现了疾病进展,为腹膜后淋巴结转移。本组患者的中位无病生存时间尚未达到。


目前,新辅助化疗联合免疫治疗已经成为食管癌术前治疗研究的热点之一。紫杉类和铂类药物联合PD-1抗体一线治疗晚期食管鳞癌的ORR为69.3%~72.1%,本研究中ORR为71.4%。本研究的pCR率为17.3%,低于新辅助放化疗的33.3%~49%和新辅助放化疗联合免疫治疗的55.6%,而高于新辅助化疗的3.8%。目前,食管癌新辅助治疗后pCR是否可以转化为生存获益仍然存在争议。本研究中对患者的随访时间较短,中位无病生存时间尚未达到,还需要进一步延长随访时间,才有望揭示新辅助化疗联合PD-1抗体治疗对食管鳞癌患者长期生存的影响。
在一项对28例食管鳞癌患者的前瞻性研究中,采用白蛋白紫杉醇+卡铂双药方案联合PD-1单抗治疗2个周期后手术,ORR为88.8%,DCR为100%,手术率为96.4%,R0切除率为100%,pCR率为33.3%。另一项对38例食管鳞癌的回顾性研究显示,采用TP方案(紫杉醇+顺铂)联合PD-1单抗新辅助治疗后,pCR率为34.2%。NICE研究显示,白蛋白紫杉醇+卡铂化疗联合卡瑞利珠单抗新辅助治疗后,pCR率为42.5%。本研究结果显示,pCR率为17.3%,但值得注意的是,本组患者中达到pCR的4例患者均采用了白蛋白紫杉醇治疗,这提示不同的紫杉醇剂型联合PD-1单抗可能存在疗效差异,需要进一步深入研究。本研究与其他相关研究的另一个不同之处在于本研究为真实世界回顾性研究,纳入研究的人群临床分期晚,接近40%为Ⅳ期患者,50%以上为经MDT讨论认为R0切除困难的患者,大多为病灶较大的潜在可切除患者,这部分患者中87.0%的患者经过化疗联合免疫治疗可以使肿瘤降期达到R0切除的目标。此外,我们在本研究中尝试在真实世界多种PD-1单抗并存的情况下,寻找较为通用的疗效预测指标,结果显示,PD-L1 CPS≥10分的患者降至Ⅰ期的比例、pCR率与PD-L1 CPS<10分的患者差异无统计学意义,但由于本研究样本量小,这一结果还需要开展大样本研究加以证实。
在食管癌新辅助治疗的副作用方面,JCOG 9907研究(新辅助化疗)、CROSS研究(新辅助放化疗)、NEOCRTEC 5010研究(新辅助放化疗)和PALACE-1研究(新辅助放化疗联合免疫治疗)显示,3~4级不良反应发生率分别为8%、20%、61.5%和65%,后3项研究中均有5级不良反应发生。本研究结果显示,3~4级不良反应发生率为21.4%,且无5级不良反应发生。本研究3~4级不良反应发生率略高于JCOG 9907研究的双药新辅助化疗,但低于NEOCRTEC 5010研究的新辅助放化疗和PALACE-1研究的新辅助放化疗联合免疫治疗,提示该疗法具有较好的安全性。本研究的新辅助治疗虽然联合了PD-1单抗,但总体免疫相关不良反应发生率不高,出现1例4级免疫性肝炎,经激素对症处理后好转。
研究显示,在可切除的食管鳞癌患者中,新辅助放化疗或新辅助化疗后完成手术者约占81.8%~94%;在不可切除的食管癌患者中,转化治疗后的手术率为41.7%。而本研究中的患者分期偏晚,57.1%的患者在治疗前MDT讨论认为R0切除困难,新辅助治疗后78.6%(22/28)的患者完成了手术,且无严重手术并发症及手术相关死亡,提示本研究的治疗方案具有良好的可行性。本研究中有1例在疗效评价为SD后改行新辅助同步放化疗,重新评估达临床CR后行手术治疗,术后病理达到pCR,提示如果采用新辅助化疗联合免疫治疗未达到预期手术目标,仍可以采用新辅助同步放化疗后手术达到临床治愈的效果。
尽管在目前大多数相关研究中,新辅助化疗联合免疫治疗食管鳞癌的周期数为2个周期,但最佳周期数、化疗与免疫治疗的顺序、是否需要免疫诱导治疗等问题仍无定论。一项可切除食管鳞癌新辅助化疗联合免疫治疗的回顾性研究显示,3~4个周期新辅助治疗后的pCR率为47.9%,显著高于2个周期的12.5%(P=0.0003),但未报道两组患者治疗及手术安全性的比较,也尚无长期随访结果。本研究由于例数较少,且行3~4个周期化疗的患者多为2个周期疗效不理想的患者,因此尚无法揭示周期数与疗效、不良反应的关系。
本研究存在一些局限性。本研究为单中心回顾性研究,样本量少,使用的化疗方案和PD-1抗体不完全统一,随访时间短。另外,本研究为真实世界研究,纳入了部分分期偏晚的边界或潜在可切除的局部晚期患者,故R0切除率或pCR率等指标可能存在偏倚。
总之,本研究初步证实化疗联合PD-1抗体新辅助治疗局部晚期食管鳞癌安全性良好、有效率高,结论还需要后续开展大样本前瞻性临床研究进行进一步验证。
免责声明本文仅供专业人士参看,文中内容仅代表中华肿瘤杂志立场与观点,不代表肿瘤资讯平台意见,且肿瘤资讯并不承担任何连带责任。若有任何侵权问题,请联系删除。
排版编辑:肿瘤资讯-Kate











 苏公网安备32059002004080号
苏公网安备32059002004080号


