
王士旭, 柯岩, 刘雨蒙, 等. 内镜下早期食管癌及癌前病变识别人工智能YOLOv51模型的建立及临床验证[J]. 中华肿瘤杂志, 2022, 44(5):395-401.
DOI: 10.3760/cma.j.cn112152-20211126-00877
目的
以人工智能深度学习的方法,构建基于YOLOv5l模型的内镜图像早期食管癌及癌前病变的识别模型,以提高内镜下早期食管癌及癌前病变的诊断水平。
方法
收集2019年6月至2021年7月中国医学科学院肿瘤医院1126例患者的白光成像(WLI)、窄带光成像(NBI)和卢戈液染色(LCE)的内镜食管图像13009幅,包括低级别上皮内瘤变、高级别上皮内瘤变、限于黏膜层的食管鳞癌、良性食管病变及正常食管。通过计算机随机函数方法,分为训练集(1025例患者的11547幅图像)和验证集(101例患者的1 462幅图像)。以训练集训练、构建YOLOv5l模型,以验证集验证该模型,同时由2名高年资和2名低年资内镜医师分别对验证集进行诊断,比较YOLOv5l模型与内镜医师的诊断结果。
结果
在验证集中,YOLOv5l模型在WLI、NBI和LCE模式下诊断早期食管癌及癌前病变的准确度、灵敏度、特异度、阳性预测值(PPV)和阴性预测值(NPV)分别为96.9%、87.9%、98.3%、88.8%和98.1%, 98.6%、89.3%、99.5%、94.4%和98.2%,93.0%、77.5%、98.0%、92.6%和93.1%。NBI模式下的准确度高于WLI模式(P<0.05),LCE模式下的准确度低于WLI(P<0.05)。YOLOv5l模型在WLI、NBI和LCE模式下诊断早期食管癌及癌前病变的准确度与2位高年资内镜医师(分别为96.9%、98.8%和94.3%,97.5%、99.6%和91.9%;均P>0.05)相当,但明显高于2位低年资内镜医师(分别为84.7%、92.9%和81.6%,88.3%、91.9%和81.2%;均P<0.05)。
结论
所构建的YOLOv5l模型在内镜WLI、NBI和LCE模式下诊断早期食管癌及癌前病变中具有较高的准确度,可以辅助低年资内镜医师提高诊断水平、减少漏诊。
【关键词】食管肿瘤,早期;癌前病变;人工智能;诊断;内镜
早期食管癌缺乏特异性症状及内镜下表现,大多数食管癌患者就诊时已是中晚期,中晚期食管癌预后差,患者的5年生存率不到20%。早期食管癌可通过内镜下治疗达到根治效果,患者的5年生存率可超过90%。因此,早诊断、早治疗是提高食管癌患者生存率的重要措施,而早诊断、早治疗的关键是提高内镜筛查早期食管癌及癌前病变的准确度,减少漏诊率。早期食管癌及癌前病变黏膜变化细微,在内镜白光成像(whitelight imaging, WLI)模式下形态学表现不明显,单纯依靠WLI诊断较困难。窄带光成像(narrow-bandimaging,NBI)是一种图像增强技术,早期食管癌及癌前病变在NBI模式下呈茶褐色改变,但缺乏经验的内镜医师在NBI模式下诊断早期食管癌及癌前病变的灵敏度仍不足53%。卢戈液染色(lugolchromoendoscopy,LCE)利用恶性组织失去富含糖原的颗粒而不染色使病变呈现白色或者粉红色的原理识别病变,但是一些良性病变,如食管胃黏膜异位、食管炎也可呈现不染色区,导致其特异度较低(40%~95%)。虽然近10余年来内镜检查辅助诊断早期食管癌及癌前病变的技术有很大提高,但由于受到内镜操作医师的认知能力、知识储备、操作技术甚至主观态度等的影响,诊断水平差异较大。有研究显示,即使在三级医疗中心,也有约6.4%的漏诊。近年来,人工智能(artificialintelligence,AI)辅助消化道疾病诊断技术取得了一定进展,有望成为内镜医师双眼之外的"第三只眼",客观、实时地辅助内镜医师检测病变,提高癌变的早诊率。目前,大多数AI辅助病变识别的研究集中在提高图像分割和分类的准确性上,提高检测速度和改进实时检测算法的研究较少,而内镜检查对实时病变识别要求较高。既往的目标检测算法多是采用二级分类的方法,需要神经网络生成目标候选区域,然后进行分类。YOLO(youonly lookonce)是一种基于深度神经网络的对象识别技术和定位算法,采用一级分类方法,即神经网络只需要看1次图片就能输出结果,其最大的特点是运行速度快,可以用于实时系统。YOLO到目前已发布了5个版本,即YOLOv1~YOLOv5,其中YOLOv5又包含了YOLOv5s、YOLOv5m、YOLOv5l和YOLOv5x等不同深度和宽度的模型。轻量级的YOLOv5l模型,可以同时预测多个检测目标和类别,无需复杂的设计过程,减少了参数数量和运行成本,降低了模型权重,运行速度明显提高,具有定位精度高、检测速度快的特点。在本研究中,我们基于YOLOv5l模型构建了早期食管癌及癌前病变的AI辅助诊断模型,旨在提高早期食管癌及癌前病变的诊断水平,减少漏诊率,提高内镜检查质量。
一、数据库的建立
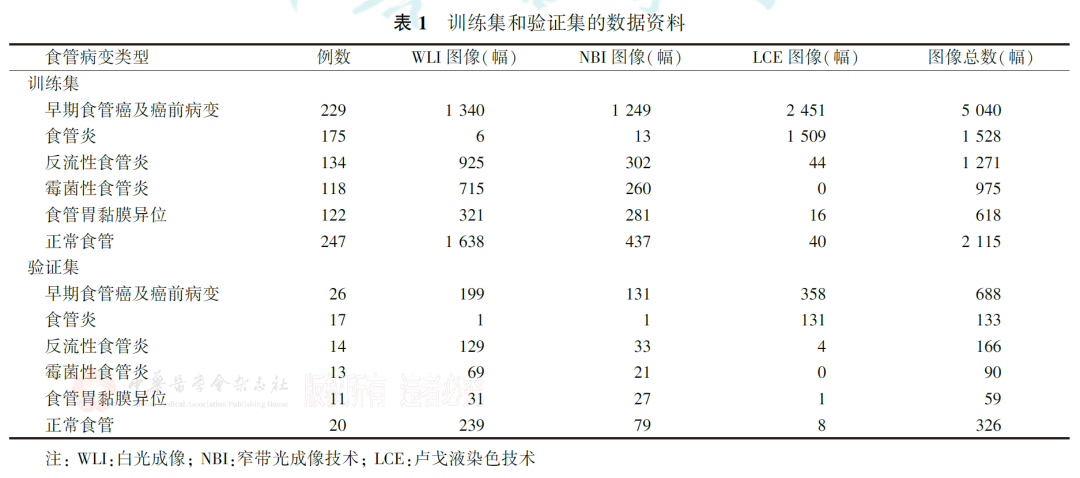
选取2019年1月至2021年7月中国医学科学院肿瘤医院内镜科行胃镜检查时所拍摄的1126例患者的13009幅WLI、NBI(非放大)和LCE图像,其中早期食管癌及癌前病变255例5728幅图像,食管炎192例1661幅图像,反流性食管炎148例1437幅图像,霉菌性食管炎131例1065幅图像,食管胃黏膜异位133例677幅图像,正常食管267例2441幅图像。低级别上皮内瘤变、高级别上皮内瘤变和早期食管癌图像均经内镜黏膜下剥离术术后病理证实。食管炎在本研究中特指在WLI模式下无明显异常或黏膜略粗糙、碘染色不着色,但经活检病理或内镜下切除后病理证实的炎性病变。排除了有食管放化疗史或手术史的患者;进展期食管癌及食管黏膜下占位患者;Barrett食管患者;图像重影、散光、模糊、出血、含有黏液影响病变识别的患者。拍摄图像主要采用日本奥林巴斯株式会社生产的GIF-H260、GIF-H260Z、GIF-HQ290、GIF-H290电子胃镜系统。通过计算机随机函数方法,在各病种中随机选取约90%的患者,即1025例患者的11547幅图像作为训练集,剩余101例患者的1462幅图像作为验证集。训练集和验证集的数据资料见表1。
二、模型的构建和验证
1.数据增强:
以病理为基础,由2名内镜医师对食管癌、高级别上皮内瘤变、低级别上皮内瘤变及食管炎图像进行拉框标注,1名高年资内镜医师最终审核完成。另外,计算机工程师还通过裁剪、旋转、平移、随机变换对比度及色度等在线增强技术对图像进行预处理,以增加样本的多样性。
2.构建并训练YOLOv51模型:
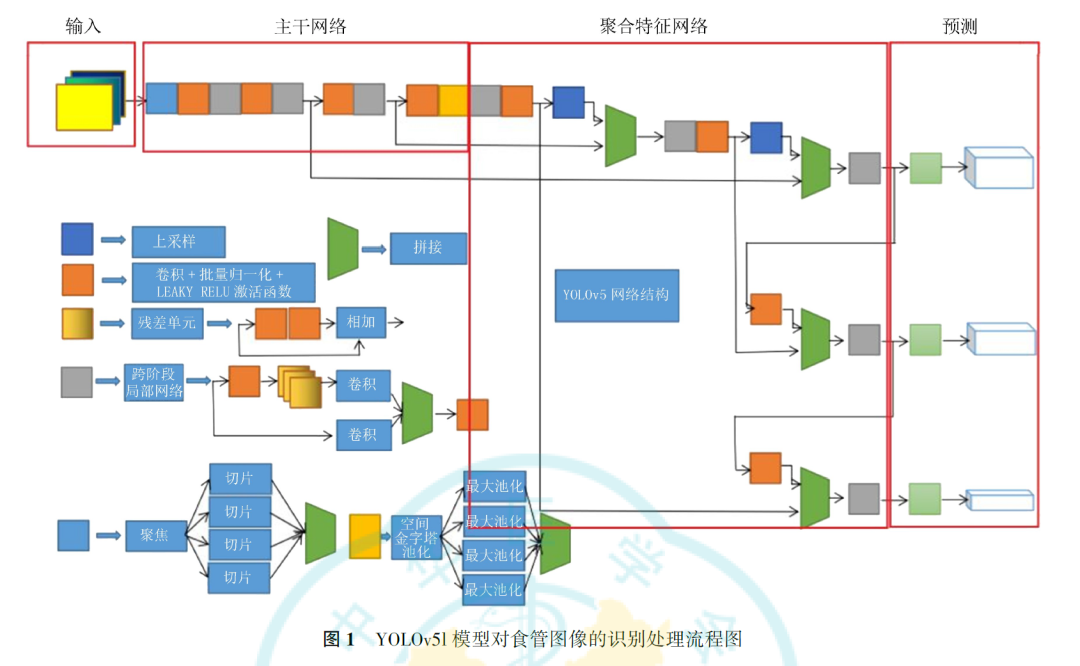
YOLOv51模型由输入端、主干网络(Backbone)、聚合特征网络(Neck)、预测(Prediction)4部分组成。首先在输入端将输入的食管图像调整为608×608×3的图像,然后将图像传入模型的Backbone部分,经过聚焦切片操作变成304×304×12的特征图,再经过1次64个卷积核的卷积操作变成304×304×64的特征图,对特征图进行一系列的卷积、批量归一化、激活函数和跨阶段局部网络操作获取高维特征,最终通过空间金字塔池化操作进行多尺度融合。在Neck部分,通过特征金字塔+路径聚合网络结构将Backbone不同阶段的特征图进行拼接融合。最后,在Prediction部分获取Neck部分的3个特征图进行卷积输出,其结果包含目标框的坐标信息和每个分类的置信度大小,根据得到的目标框进行阈值调节和非极大值抑制完成目标框的筛选(图1)。采用GoogleTensorflow FrameWork为AI框架,训练服务器配置为Ubantu18.4 64bit OS,IntelIi7-7800X CPU,Nvidia2080Ti×2 GPU。
3.YOLOv5l模型验证:
对验证集的图像进行数字编码,并保证编码的唯一性和可溯源性,以供后期比对YOLOv5l模型的输出结果和内镜医师的判读结果。应用YOLOv5l模型对验证集图像进行病变性质识别。
三、内镜医师的判读
由2名内镜操作>10年(高年资组)和2名内镜操作<3年(低年资组)的内镜医师,分别独立对验证集图像进行性质判断,记录诊断时间。只有标注医师、审核医师及计算机工程师对验证集的影像学和组织学诊断知情,而4名进行判读的内镜医师不知情。
四、统计学方法
应用SPSS20.0软件进行统计分析。组间率的比较采用χ2检验,检验水准α=0.05。
1.YOLOv5l模型的验证结果:
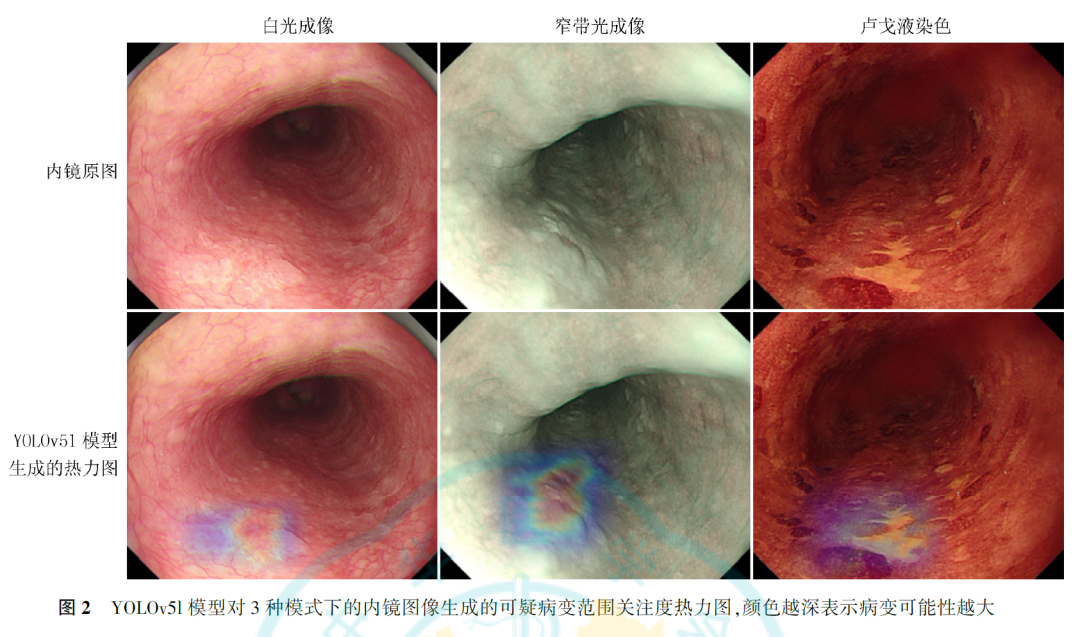
YOLOv5l模型完成验证集1462幅图像的诊断共用时251.93s,平均每幅图像用时0.17s。在验证集中,YOLOv5l模型在WLI模式下诊断早期食管癌及癌前病变的准确度、灵敏度、特异度、阳性预测值(positivepredictive value, PPV)和阴性预测值(negativepredictive value,NPV)分别为96.9%、87.9%、98.3%、88.8%和98.1%,在NBI模式下诊断早期食管癌及癌前病变的准确度、灵敏度、特异度、PPV和NPV分别为98.6%、89.3%、99.5%、94.4%和98.2%,在LCE模式下诊断早期食管癌及癌前病变的准确度、灵敏度、特异度、PPV及NPV分别为93.0%、77.5%、98.0%、92.6%和93.1%。NBI模式下的准确度和特异度高于WLI(均P<0.05),LCE模式下的准确度和特异度低于WLI(均P<0.05)。YOLOv5l模型识别病变后输出可疑病变范围关注度热力图见图2,红色表示病变可能性较大,蓝色表示病变可能性较小。在WLI、NBI和LCE模式下,YOLOv5l模型均可准确判断病变范围,并对病变较重区域产生更高关注度。
2.内镜医师对验证集图像的诊断结果:
2位低年资医师完成验证集图像的诊断分别需要160和205min,2位高年资医师分别需要115和130min。2位低年资医师在WLI、NBI和LCE模式下诊断食管癌及癌前病变的准确度分别为84.7%、92.9%、81.6%和88.3%、91.9%、81.2%,2位高年资医师则分别为96.9%、98.8%、94.3%和97.5%、99.6%、91.9%。
3.YOLOv5l模型与内镜医师诊断效能比较:
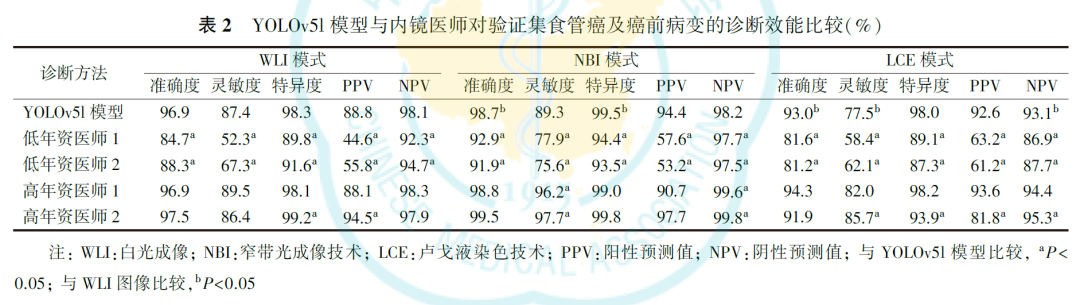
YOLOv5l模型完成验证集图像的诊断共用时251.93s,约为低年资医师平均用时的1/43,约为高年资医师平均用时的1/29,诊断时间大大缩短。YOLOv5l模型在WLI、NBI和LCE模式下诊断食管癌及癌前病变的准确度、灵敏度、特异度、PPV及NPV均高于2位低年资医师(均P<0.05)。YOLOv5l模型在WLI、NBI和LCE模式下的准确度、在WLI和LCE模式下的灵敏度、在WLI模式下的NPV、在NBI模式下的特异度和PPV与2位高年资医师相当(均P>0.05),在NBI模式下的灵敏度和NPV低于2位高年资医师(均P<0.05),在WLI和LCE模式下的特异度及PPV与1位高年资医师相当(均P>0.05),但低于另1位高年资医师(P<0.05,表2)。
内镜筛查是食管癌早发现、早诊断、早治疗的重要手段,是降低食管癌死亡率、提高预后的重要策略。然而,早期食管癌及癌前病变形态学不明显、内镜医师诊断水平差异较大、内镜检查的质量控制体系尚不完善、我国内镜诊疗技术发展不均衡等原因导致我国食管癌的早诊率仍然处于较低水平。
近年来,AI辅助消化内镜诊断方面发展迅速,为肿瘤的早诊断、早治疗提供了新方向,深度卷积神经网络已在病变检出中显示出了较好的结果,特别是在结肠息肉检出等领域。与结肠息肉检出相比,早期食管癌或癌前病变异质性较高,形态学表现更为多样化,其他良性病变如食管炎、食管胃黏膜异位等,也会干扰早期食管癌或癌前病变的诊断,因此AI在早期食管癌及癌前病变的检出方面技术难度大、发展速度慢。在本研究中,我们利用YOLOv5l模型及数据增强等技术,对内镜下早期食管癌及癌前病变的病变性质诊断进行了初步探索。
早期食管癌及癌前病变内镜下形态变化多样,可表现为黏膜红区、糜烂灶、斑块、结节、黏膜粗糙、局部黏膜增厚等,一些食管良性病变如食管炎、食管胃黏膜异位、反流性食管炎亦可能有上述内镜下表现,因此内镜下发现可疑区域并进行鉴别是后续诊疗的基础。在既往的一些AI辅助早期食管癌及癌前病变诊断的研究中,没有纳入良性病变训练,导致有一半的假阳性是由正常结构和良性病变所致,病例选择上的偏倚在一定程度上影响了AI模型的临床适用性。我们认为,上消化道部位识别是病变识别的基础,同时纳入良性病变训练是AI辅助内镜诊断早期食管癌及癌前病变走向临床所必需的。本研究是我科开展的AI辅助内镜诊断系列研究之一,我们前期已完成AI辅助上消化道部位识别研究,为了评估YOLOv5l模型诊断病变性质的性能,结合临床实际,我们纳入了与早期食管癌及癌前病变黏膜背景相似的良性食管病变(包括食管炎、反流性食管炎、霉菌性食管炎及食管胃黏膜异位)和正常食管图像,结果显示,在WLI、NBI和LCE成像中,YOLOv5l模型识别早期食管癌及癌前病变的准确度和特异度均高于93%,诊断能力良好。
WLI、非放大成像是最常见的内镜成像方式,是内镜下筛查早期食管癌及癌前病变的基础,而部分早期食管癌及癌前病变在内镜WLI成像中形态学表现不明显,不同观察者之间的差异变化较大、主观性强,仅靠WLI内镜筛查可能会造成大量漏诊。虽然LCE可能会给受检者带来食管炎、食管痉挛、胸痛等不良反应,在食管早癌筛查中使用率较低,但由于NBI和LCE成像具有较高灵敏度,欧洲胃肠病学会指南推荐二者联合用于食管癌筛查。目前,AI在LCE及多种模式综合诊断中的效能尚鲜有文献报道。在本研究中,我们评价了AI在WLI、NBI和LCE成像模式对食管病变性质识别的效能,结果显示,NBI模式下的准确度和特异度高于WLI(均P<0.05),LCE模式下的准确度和特异度低于WLI(均P<0.05),表明AI在NBI成像模式下的诊断效能最好,在LCE成像模式下的诊断效能最差。尽管如此,AI在LCE成像模式下的各项诊断评价指标均高于低年资医师。在临床上,内镜医师常常难以区分食管碘染色阳性灶为食管炎还是癌前病变,主观差异性很大。相比之下,AI属于客观诊断,可能会减小这种主观可变性。因此,虽然AI在碘染色成像上表现稍差,但仍有重要临床意义。
我们经过反复测试最终选择了YOLOv5l作为病变识别模型,结果证明该模型对早期食管癌或癌前病变具有较高的病变识别准确度,可达高年资内镜医师水平。对于AI辅助内镜下食管病变的筛查,需要满足两个条件,即高准确度和实时性。我们建立的YOLOv5l模型不仅在WLI、NBI和LCE成像模式下对食管病变性质的识别准确度均达到93%以上,而且还可以准确输出食管可疑病变范围热力图,颜色越深表示病变的可能性越大。将来AI可能通过算法的完善准确地区分病变区域与非病变区域,进而指示内镜医师靶向活检,并提示内镜下的治疗范围。本研究中,YOLOv5l模型诊断1幅图像平均用时仅为0.17s,表现出实时性方面的重要优势,为其后续实时辅助诊断奠定了基础。
本研究尚存在一些不足之处。首先,本研究为一项单中心回顾性研究,同时我们还剔除了低质量图像,这可能会在一定程度上会影响所建立模型的临床适用性。在后续研究中,我们将会纳入多中心的数据进行训练、验证,继续优化算法及软件。其次,本研究纳入的早期食管癌不包括食管腺癌。在我国,超过90%的食管癌组织学类型为鳞癌,食管腺癌及与腺癌相关的良性病变Barrett食管较为少见,在AI模型训练中我们没有纳入食管腺癌和Barrett食管的图像,这可能会造成腺癌的漏诊。第三,我们建立的辅助诊断模型是基于静态图像进行训练及验证的,而动态视频包含更多空间和时间信息,基于动态视频构建的辅助诊断模型的性能可能会优于基于静态图像构建的模型,更适于在实时诊断中使用。
综上所述,我们基于YOLOv5l模型构建的AI辅助诊断模型在早期食管癌及癌前病变的性质识别上具有较高的准确度,优于低年资内镜医师的诊断水平。相信在不久的将来,随着算法的不断进步和完善,AI可真正实现辅助不同年资、不同地区的内镜医师提高早期食管癌及癌前病变的诊断水平,为消化道肿瘤的早诊断、早治疗做出贡献。
免责声明本文仅供专业人士参看,文中内容仅代表中华肿瘤杂志立场与观点,不代表肿瘤资讯平台意见,且肿瘤资讯并不承担任何连带责任。若有任何侵权问题,请联系删除。
排版编辑:肿瘤资讯-Kate











 苏公网安备32059002004080号
苏公网安备32059002004080号


